
在25℃时,若溶液中由水电离产生的c(OH—)=l×l0-14mol·L—1,满足此条件的溶液中一定可以大量共存的离子组是
A.Al3+、Na+、NO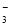 、Cl—
、Cl—
B.K+、Na+、Cl—、NO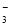
C.K+、Na+、Cl—、[Al(OH)4]—
D.K+、NH 、SO
、SO 、NO
、NO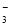
B
【解析】
试题分析:25℃时,某溶液中由水电离产生的c(OH—)=l×l0-14mol·L—1,此溶质对水的电离产生抑制,此溶液可能显酸性也可能显碱性,题目要求“一定”大量共存即既能存在于酸性也能存在于碱性溶液中,A、Al3+与OH-发生反应,不能大量存在于碱性溶液中,错误;B、四种离子彼此不反应,既能存在于酸性也能存在于碱性,大量共存,正确;C、[Al(OH)4]-与H+反应,不能大量存在于酸性溶液中,错误;D、NH4+与OH-反应,不能大量存在于碱性溶液中,错误。
考点:考查影响水电离的因素、离子共存问题。
考点分析: 考点1:离子共存 考点2:水的电离和溶液的酸碱性 试题属性

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:2014-2015重庆市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,一定有硫酸根离子
B.Na2O2与CO2反应,Na2O2是氧化剂、CO2是还原剂
C.向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是:浅绿色溶液 →白色沉淀→灰绿色沉淀→红褐色沉淀
D.称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,则放出氢气的体积(同温同压下)不相等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第一学期期末练习化学试卷(解析版) 题型:实验题
(15分)某化学探究小组拟用废铜屑制取Cu(NO3)2:,并探究其化学性质。
I.如图,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液。

(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、 、过滤。
③你认为此装置是否合理,并说明原因 。
如果不合理,同时在原装置上改进;如果合理,只需说明原因。
Ⅱ.为了探究 的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
【实验装置】

【实验操作及现象】往试管中放人研细的无水Cu(NO3)2:晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体。
【解释与结论】
(3)①红棕色气体是 。
②根据现象判断 在加热条件下可以分解,其化学反应方程式为 。
在加热条件下可以分解,其化学反应方程式为 。
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。
【实验数据】反应温度对样品的影响
实验序号 | 1 | 2 | 3 | 4 |
温度/℃ | 35 | 50 | 70 | 95 |
样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
样品中碱式碳酸铜 的质量分数/% | 90.9 | 92.7 | x | 92.0 |
(4)滤液中可能含有 ,写出检验
,写出检验 的方法 。
的方法 。
(5)95℃时,样品颜色发暗的原因:____ 。
(6)70C时,实验得到2.38 g样品,取此样品加热至分解完全(杂质不分解),得到1.76 g固体,此样品中碱式碳酸铜的质量分数是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省泰安市高二上学期期末统考高二化学试卷(解析版) 题型:填空题
有如图电解装置,图中A装置中盛1 L 2 mol· L—1AgNO3溶液,B装置中盛1L 2 mol·L—1Na2SO4溶液。通电后,湿润的KI淀粉试纸的C端变蓝色,电解一段时间后,试回答:

(1)A中发生反应的化学方程式为___________________________________________。
(2)在B装置中观察到的现象是____________________________________________。
(3)室温下,若从电解开始到时间为T时,A、B装置中共收集到气体0.168L(标准状况),若电解过程中无其他副反应发生,且溶液体积变化忽略不计。试计算:T时刻A装置溶液中c(H+)(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省泰安市高二上学期期末统考高二化学试卷(解析版) 题型:填空题
已知下列两个热化学方程式:
H2(g)+  O2(g)=H2O(1) △H=-285.8 kJ·mol-l
O2(g)=H2O(1) △H=-285.8 kJ·mol-l
C3H8(g)+5O2(g)=4H2O(l)+3CO2(g) △H =-2220.0kJ·mol-l
(1)相同条件下,实验测得H2和C3H8的混合气体共5 mol,完全燃烧生成液态水时放出热量6264.5 kJ,则混合气体中H2和C3H8的体积比为___________。
(2)已知:H2O(1)=H2O(g) △H =44.0kJ·mol-l.写出丙烷燃烧生成CO2和气态水的热化学方程式_______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省泰安市高二上学期期末统考高二化学试卷(解析版) 题型:选择题
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为CO(g)+H2O(g) CO2(g)+H2(g) △H<O。反应达到平衡后,为提高CO的转化率,下列措施中正确的是
CO2(g)+H2(g) △H<O。反应达到平衡后,为提高CO的转化率,下列措施中正确的是
A.增加压强 B.降低温度 C.增大CO的浓度 D.更换催化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省泰安市高二上学期期末统考高二化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.化学反应中的能量可能以热能的形式表现出来
B.化学反应的热效应数值与参加反应的物质多少有关
C.放热反应不一定需要加热
D.焓变是指1 mol物质参加反应时的能量变化
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省忻州市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列排列顺序正确的是
①第一电离能Na<Al<Mg ②热稳定性:H2O>HF>NH3
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力OH﹣>CH3COO﹣>Cl﹣
⑤还原性:HF<HCl<HBr<HI ⑥离子半径:Ca2+<K+<Cl-<S2-
A.①②③④ B.①④⑤⑥ C.②③④⑤ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省校高一上学期期末考试化学试卷(解析版) 题型:选择题
向Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量w和加入NaOH体积v之间的关系如图所示.则混合溶液中Al2(SO4)3和MgSO4的物质的量之比为
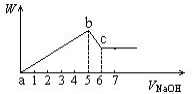
A.1:1 B.1:2 C.2:1 D.1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com