
����Ŀ���ҹ���ѧ������ɹ��ϳ������������嵪��������(N5)6(H3O)3(NH4)4Cl���� R�������� �ش��������⣺
��1����̬��ԭ�Ӽ۲���ӵĹ����ʾʽΪ_____��
��2�������ӵĻ�̬�����Ų�ʽΪ_____����_____�ֲ�ͬ�ܼ��ĵ��ӡ�
��3��R �� H��N��O ����Ԫ�صĵ縺���ɴ�С��˳����_____(��Ԫ�ط��ű�ʾ)��
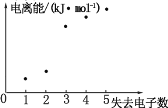
��4����ͼ��ʾ������Ԫ�� X �Ļ�̬ԭ��ʧȥ���������Ӧ�����ܵĹ�ϵ�����Ʋ� X ��R �е�_____(��Ԫ�ط���)Ԫ��ͬ���ڡ�
���𰸡�![]() 1s22s22p63s23p6 5 O>N>H Cl
1s22s22p63s23p6 5 O>N>H Cl
��������
(1)���ݺ�������Ų�ʽд���۲���ӵĹ����ʾʽ��
(2)������ԭ�Ӻ�������Ų�ʽ�������ӵĻ�̬�����Ų�ʽ�����ݵ����Ų�ʽ�ҳ���ͬ�ܼ��ĵ��ӵ���Ŀ��
(3)���ݷǽ����Ե�ǿ�����жϳ��縺�Ե�ǿ����
(4)���ݵ����ܵĶ����ͼ��ش�
(1)����7��Ԫ�أ���������Ų�ʽΪ1s22s22p3���۲���ӵĹ����ʾʽΪ![]() ��
��
(2)�����ӵĻ�̬�����Ų�ʽΪ1s22s22p63s23p6����1s��2s��2p��3s��3p5���ܼ���ͬ�ĵ��ӣ�
(3)�ǽ�����O��N��H����縺��O��N��H��
(4)������Ԫ�� X�ĵ���������5����Ϊ�ڶ���������ڵ�Ԫ�أ�ͼ����Կ�����ʧȥ2�����Ӻ�ʧȥ3������ʱ��������ϴ�˵��ʧȥ�ĵ������������ȶ��ṹ�ĵ��ӣ���X�������Ӧ����2�����ӣ�X�ĵ���������5����XΪþ����R�е�Clͬһ���ڡ�


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20��ʱ����0. 1mol/L ����ζ�20mL 0. 1mol/L ��ˮ��ͼ����ͼ��ʾ������˵����ȷ����
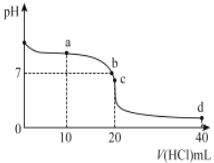
A.a��ʱ2c(Cl-)=c(NH3H2O)+c (NH4+)
B.b���ʾ���ǡ����ȫ��Ӧ
C.c��ʱc(NH4+)>c(Cl-)>c(H+ )>c(OH- )
D.a ��b��c��d����c(NH4+)+c(H+) = c(Cl-)+c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NAΪ�����ӵ�������ֵ������˵���������
A.27 g ���������� 1mol/L �� NaOH ��Һ��ת�Ƶĵ�����Ϊ 3NA
B.18g ����(��ND2)�к��еĵ�����Ϊ 10NA
C.�� 100mL0.1mol/L ������Һ�м� CH3COONa ��������Һ�պ�Ϊ���ԣ���Һ�д��������Ϊ 0.01NA
D.�ö��Ե缫��� 100mL0.1mol/L �� CuSO4 ��Һ��������������������ͬ�����µ����������ʱ�� ��·��ת�Ƶ�����Ϊ 0.04NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±����������ܽ���������ܶȻ�����(25��)��
��ѧʽ | FeS | CuS | MnS |
�ܶȻ� | 6.3��10-18 mol2��L-2 | 1.3��10-36 mol2��L-2 | 2.5��10-13 mol2��L-2 |
�����й�˵������ȷ����
A.25��ʱ��CuS ���ܽ�ȴ��� MnS ���ܽ��
B.��ȥij��Һ�е� Cu2��������ѡ�� FeS ��������
C.��Ϊ H2SO4 ��ǿ�ᣬ���Է�Ӧ CuSO4+H2S = CuS��+H2SO4���ܷ���
D.25��ʱ������ CuS ��Һ�У�Cu2����Ũ��Ϊ 1.3��10-36 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̫����Ϊ��Դ���Ȼ�ѧ���ѭ���ֽ�ˮ��һ�ָ�Ч������Ⱦ�����ⷽ��������������ͼ��ʾ����֪��Ӧ�еõ��IJ����мӹ���I2��õ�������Һ��������Ũ��I2��H2SO4��ͺ���Ũ��I2��HI�㣬������ֱ���з�Ӧ��������ѭ���ֽ����⡣����˵���������( )
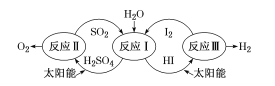
A.��ӦI�Ļ�ѧ����ʽΪ SO2+2H2O+I2=H2SO4+2HI
B.�����̽�̫����ת��Ϊ��ѧ�ܣ��ҽ�����ˮ�ֽ�����Ļ��
C.H2SO4���HI���ڼ�I2֮ǰ�ͼ�I2֮����ֳ����㣬�������ܶȡ���ɫ������ͬ
D.SO2��I2�Ƿ�Ӧ 2H2O =2H2+O2�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��Ϊ�˷�����Ѫ�� FeSO4��7H2O ����Ԫ�ص������������� KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�5Fe2����MnO4- ��8H��= 5Fe3����Mn2����4H2O��
��1��ʵ��ǰ������Ҫ��ȷ����һ�����ʵ���Ũ�ȵ� KMnO4 ��Һ 250 mL������ʱ��Ҫ�õ���������ƽ��ҩ�ס����������ձ�����ͷ�ι��⣬����____________��
��2���ζ�ǰ�Ƿ�Ҫ�μ�ָʾ��?_____(��ǡ���)��������_____��
��3��ijͬѧ��Ƶ����еζ���ʽ�У����������_____(�����)
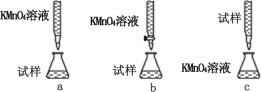
��4����ʵ��С���ȡ 12.0 g ��Ѫ��������ƿ����� 100 mL ��Һ����ȡ 25.00 mL ������Һ�� �� 0.100 mol��L-1 KMnO4����Һ�ζ��� �ﵽ�ζ��յ�ʱ�� ���ı���Һ20.00 mL�������ⲹѪ������Ԫ�ص�����������_____����ȷ�� 0.01%����
��5������С��������Һ�͵ζ�����ʱ����������ԣ��������ⲹѪ������Ԫ�غ��� ��ƫС�������ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ɵļ���ȼ�ϵ��ԭ����ͼ��ʾ������˵����ȷ����
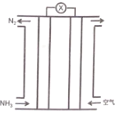
A.�������Һ�е�����������
B.��ظ�����ӦΪ��2NH3-6e-=N2+6H+
C.������ͨ�����������ͬ���������֮��Ϊ15: 4 (���������O2�������Ϊ20%)
D.�õ�ظ�Ǧ���س�磬ȼ�ϵ��������Ӧl molO2��Ǧ������2mol PbSO4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������A �� B ���������ֶ�����Ԫ����ɵ����ӻ���� ����������ͬ��A���������Ӹ�����Ϊ1 : 1�������������Ԫ����ɣ�������ܶ�Ϊ2.68gL-1 ���ҷ����и�ԭ��������������8 ���� ���Һͱ�Ϊ'�������壬����ʹ����ʯ��ˮ����ǣ�����ʹƷ����Һ��ɫ�����嶡��ʹʪ��ĺ�ɫʯ����ֽ������������A ���������̽���ʵ�顣
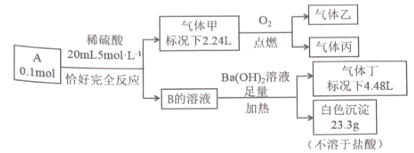
��ش�
(1)����ĵ���ʽ ______________��
(2)�����ͨ���������ᱵ��Һ�У�������Ӧ�����ӷ���ʽΪ____________��
(3)����A��ˮ��Һ�����������ӵ�ʵ�鷽��Ϊ_________________��
(4)������������һ�������� ________(�� �����ܡ� �����ܡ�) ����������ԭ��Ӧ����������д������Ϊ�����Ļ�ѧ����ʽ������������˵���������________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ĺ������кܶ��֣������������ᡢ�������⣬���кܶ������ᣬ�罹������(H2S2O5)����һ����(H2SO5) ��������(H2S2O8) �ȡ���һ������һ��һԪǿ�ᣬ��������Ӿ����������ṹʽ��ͼ��ʾ������������һ�ְ�ɫ���壬�����ֽ⣬��ǿ��ˮ�ԣ���������ˮ����ˮ�л���ˮ��õ�����������⣬��ش�����������⡣
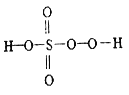
(1)��һ��������Ԫ�صĻ��ϼ���_________����������Ľṹʽ��_____________��
(2)��ҵ���Ʊ�����������Һ������֮һ���£�
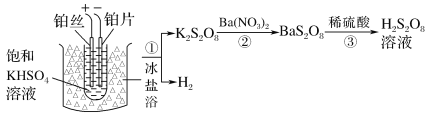
�ٵ��ʱ�����ĵ缫��ӦʽΪ______
�����������ܷ���ͭ˿���沬˿��________(������������������)��˵�����ɣ�__________��
(3)����������(Na2S2O5)����Ҫ�Ŀ�����������ҵ�������̵����е�SO2����Na2S2O5�Ĺ���Ϊ��
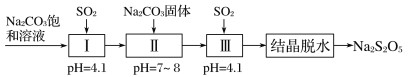
��pH��4.1ʱ������Ϊ________��Һ(д��ѧʽ)��
�ڹ����м���Na2CO3���壬���ٴγ���SO2��Ŀ����___________��
�����ѾƳ���Na2S2O5�������������ڲⶨij���Ѿ���Na2S2O5������ʱ��ȡ50.00 mL���Ѿ���Ʒ����0.010 00 mol��L��1�ĵ��Һ�ζ����յ㣬����10.00 mL���ζ���Ӧ�����ӷ���ʽΪ_______________ ������Ʒ��Na2S2O5�IJ�����Ϊ______g��L��1(��SO2��)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com