
【题目】CO、H2、CH3、OH均是清洁能源。
(1)已知部分化学键键能数据如下:
化学键 | C | O=O | C=O | C-O |
E/(kJ mol-1) | 958.5 | 497 | 745 | 351 |
2CO(g) +O2(g)==2CO2(g) △H1
H2O(g)+CO(g)==H2(g) + CO2(g) △H2 = -41 kJmol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) △H3 = -660kJmol-1
则△H1=_____ kJmol-1,反应CO(g)+2H2(g) ![]() CH3OH(g)的△H=_____ kJmol-1。
CH3OH(g)的△H=_____ kJmol-1。
(2)一定条件下,在容积为2 L的密闭容器Q中充人a mol CO与6 molH2合成甲醇:CO(g) +2H2(g) ![]() CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。

①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1___ t2(填“>”、“<”、“=”或“无法确定”)。
②X=___________(用含a、b的式子表示),p1_____p2(填“>”、“<”、“=”或“无法确定”)。
③若a =2,b=4,则压强为p1、温度为了T1时该反应的平衡常数K=______________。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正_____v(CH3OH)逆(填“>”、“<”、“=”或“无法确定”)。
(3)甲醇燃料电池是一种具有高能量转化率的绿色电池,则用磷酸溶液作电解质时,负极的电极反应式为________________________。
【答案】 -566 -107 > ![]() > 4. 5 无法确定 CH3OH+H2O-6e-==CO2↑+6H+
> 4. 5 无法确定 CH3OH+H2O-6e-==CO2↑+6H+
【解析】(1)根据化学方程式及化学键键能数据,△H1=2×958.5+497-2×745×2=-566 kJmol-1;根据盖斯定律,CO(g)+2H2(g) ![]() CH3OH(g)的△H=△H1×
CH3OH(g)的△H=△H1×![]() -△H2×2-△H3=(-566×
-△H2×2-△H3=(-566×![]() +41×2+660)kJmol-1=-107 kJmol-1。
+41×2+660)kJmol-1=-107 kJmol-1。
(2)因为CO(g)+2H2(g) ![]() CH3OH(g) △H=-107 kJmol-1<0,所以温度越高,平衡时CH3OH的含量越低,所以图1中T2>T1,故①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1>t2。②已知a mol CO与b molH2合成甲醇,故投料物质的量之比(用X表示)为:
CH3OH(g) △H=-107 kJmol-1<0,所以温度越高,平衡时CH3OH的含量越低,所以图1中T2>T1,故①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1>t2。②已知a mol CO与b molH2合成甲醇,故投料物质的量之比(用X表示)为: ![]() ;由图2知,投料比相同时,压强为P1的反应氢气平衡转化率高,又因为该反应为气体分子数减小的反应,故P1>P2。③若a=2,b=4,则压强为P1、温度为了T1时,列三段式:
;由图2知,投料比相同时,压强为P1的反应氢气平衡转化率高,又因为该反应为气体分子数减小的反应,故P1>P2。③若a=2,b=4,则压强为P1、温度为了T1时,列三段式:
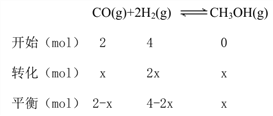
由图1,此条件下平衡时CH3OH的体积分数为40%,所以: ![]() =0.4,解得x=
=0.4,解得x=![]() ,所以平衡时n(CO)=
,所以平衡时n(CO)=![]() mol,n(H2)=
mol,n(H2)=![]() mol,又因为容积为2L,所以CO、H2、CH3OH的平衡浓度分别为:
mol,又因为容积为2L,所以CO、H2、CH3OH的平衡浓度分别为: ![]() molL-1、
molL-1、![]() molL-1、
molL-1、![]() molL-1,故K=
molL-1,故K=![]() =4.5。
=4.5。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体(设为y),此时浓度商=![]() =
=![]() ÷[
÷[![]() ×(
×(![]() )2]=
)2]= ![]() ,与K无法比较大小,不确定平衡向哪个方向移动,故无法确定ν(CH3OH)正与ν(CH3OH)逆的大小。
,与K无法比较大小,不确定平衡向哪个方向移动,故无法确定ν(CH3OH)正与ν(CH3OH)逆的大小。
(3)酸性条件下甲醇燃料电池的总反应式为:CH3OH+![]() O2=CO2+2H2O①,酸性条件下该燃料电池的正极反应式为:
O2=CO2+2H2O①,酸性条件下该燃料电池的正极反应式为: ![]() O2+6H++6e-=3H2O②,①-②得电池负极反应式为:CH3OH+H2O-6e-=CO2↑+6H+。
O2+6H++6e-=3H2O②,①-②得电池负极反应式为:CH3OH+H2O-6e-=CO2↑+6H+。


科目:高中化学 来源: 题型:
【题目】测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。某兴趣小组的实验数值结果大于57.3 kJ·mol-1(中和热),原因可能是

A. 实验装置中小烧杯杯中低于大烧杯杯口
B. 用浓硫酸代替了稀硫酸
C. 分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D. 用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、体积为2 L的密闭容器中进行反应:2A(g)![]() 3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为( )
3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为( )
A. v(B)=0.03 mol·L-1·s-1
B. v(B)=0.045 mol·L-1·s-1
C. v(C)=0.03 mol·L-1·s-1
D. v(C)=0.06 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 醋酸和碳酸钙反应:2H++CaCO3=Ca2++CO2↑+H2O
B. 铁与三氯化铁溶液反应:Fe+Fe3+=2Fe2+
C. 氢氧化钠溶液与少量二氧化硫气体:SO2+2OH-=SO32-+=H2O
D. 氯化铝溶液与足量氨水:Al3++=4NH3·H2O=AlO2-+=4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是重要的基础有机化工原料.工业中以乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:C6H5-CH2CH3(g)![]() C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
(1)向体积为VL的密闭容器中充入n mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:

600℃时,该反应的平衡常数_____________。
(2)乙苯在特定催化剂下发生氧化脱氢:
C6H5-CH2CH3(g)+1/2O2(g)![]() C6H5-CH=CH2(g)+H2O(g) ΔH1
C6H5-CH=CH2(g)+H2O(g) ΔH1
已知 H2的燃烧热ΔH= b kJ/mol,水的汽化热为c J/g,则 ΔH1=____________。
(3)在汽车上安装三元催化转化器可实现反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。

(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl+Cl-═[AgCl2]-,如图是某温度下AgCl在NaCl溶液中的溶解情况.
由以上信息可知:
①由图知该温度下AgCl的溶度积常数为_________。
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:_______________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com