
【题目】氰化钠广泛用于电镀、金的提取及有机合成中,含氰废水属于高毒类,必须对其进行处理。
(1)向NaCN溶液中通入CO2能发生反应:NaCN+H2O+CO2=HCN+NaHCO3。说明酸性:HCN___(填“>”或“<”)H2CO3。
(2)含CN-浓度较低的废水可直接用FeSO4 7H2O处理,得到一种蓝色沉淀M,M的摩尔质量为324 g mol-1,则M的化学式为_______。
(3)pH在7.510之间用铜作催化剂的条件下,用SO2-空气处理含氰废水会生成NH3、碳酸氢盐及硫酸盐,已知参与反应的SO2与O2的物质的量之比为1:1,则该反应的离子方程式为___________。
(4)工业上常用碱性氯化法处理含氰废水,其原理如下:

①第一阶段的中间体CNC1中碳元素的化合价为________。
②某工厂含氰废水中NaCN的含量为147 mg L-1,处理10m3这样的废水,理论上需要5 mol L-1的NaClO 溶液_______L。
【答案】 < Fe2[Fe(CN)6][写 Fe3(CN)6不扣分] CN-+ O2+ SO2+2OH- + H2O![]() HCO3- + NH3 + SO42- +4 15
HCO3- + NH3 + SO42- +4 15
【解析】(1)根据NaCN+H2O+CO2=HCN+NaHCO3可知,酸性:HCO3-<HCN<H2CO3,故答案为:<;
(2)含CN-浓度较低的废水可直接用FeSO4 7H2O处理,得到一种蓝色沉淀M,根据M的摩尔质量为324 g mol-1,M为六氰合铁(II)酸铁,化学式为Fe2[Fe(CN)6],故答案为:Fe2[Fe(CN)6];
(3)pH在7.510之间用铜作催化剂的条件下,用SO2-空气处理含氰废水会生成NH3、碳酸氢盐及硫酸盐,已知参与反应的SO2与O2的物质的量之比为1:1,则反应的离子方程式为CN-+ O2+ SO2+2OH- + H2O![]() HCO3- + NH3 + SO42-,故答案为:CN-+ O2+ SO2+2OH- + H2O
HCO3- + NH3 + SO42-,故答案为:CN-+ O2+ SO2+2OH- + H2O![]() HCO3- + NH3 + SO42-;
HCO3- + NH3 + SO42-;
(4)①CNC1中氯元素为-1价,N元素为-3价,根据正负化合价的代数和为0,碳元素的化合价为+4价,故答案为:+4;
②含量为147 mg L-1,处理10m3的废水中含有NaCN的质量为147 mg L-1×10×1000L=1470000 mg=1470g,物质的量为![]() =30mol。由题意CN-最终被NaClO氧化成氮气和二氧化碳,所以1molCN-被氧化化合价升高2+3=5,所以NaClO化合价也降低5价即消耗2.5mol,所以完全处理含30molCN-的废水,理论上需要消耗NaClO的物质的量为30×2.5mol=75mol,需要5 mol L-1的NaClO 溶液的体积为
=30mol。由题意CN-最终被NaClO氧化成氮气和二氧化碳,所以1molCN-被氧化化合价升高2+3=5,所以NaClO化合价也降低5价即消耗2.5mol,所以完全处理含30molCN-的废水,理论上需要消耗NaClO的物质的量为30×2.5mol=75mol,需要5 mol L-1的NaClO 溶液的体积为![]() =15L,故答案为:15。
=15L,故答案为:15。


科目:高中化学 来源: 题型:
【题目】(1)下列叙述正确的是_______________
A.汽油、柴油和植物油都是碳氢化合物
B.甲烷、乙烯和苯在工业上都可通过石油分馏得到
C.乙醇可以被氧化为乙酸.二者都能发生酸化反应
D.向鸡蛋清溶液中加人(NH4)2SO4或CuSO4都能使鸡蛋清析出,其作用原理相同
(2)现有一瓶甲、乙的混合物,已知甲、乙属于同系物,甲、乙某些性质如下,
物质 | 分子式 | 熔点(℃) | 沸点(℃) | 密度(g/cm3 ) | 水溶性 |
甲 | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
乙 | C4H8O2 | -84 | 77 | 0.90 | 可溶 |
根据物理性质.将混合物中甲、乙分离的最佳方法是______________
A. 萃取 B.蒸馏 C.加热升华 D.分液
(3)某有机物的结构简式为它可以发生反应的类型有:①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚,下列正确的有__________________

A. ①②③⑤⑥⑦ B. ①②③⑥⑧ C. ①②③④⑤⑥ D. ③④⑤⑥⑦⑧
(4)用C4H9的烷烃基取代甲苯苯环上的一个氢原子,能得到的有机物种数为_________________
A. 3种 B. 8种 C.9种 D. 12种
(5)2015年10月,中国科学屠呦呦获得了诺贝尔医学奖.获奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物.挽救了全球特别是发展中国家的数百万人的生命”,右图是青蒿素的结构,则有关青蒿素的说法中不正确的是_____________
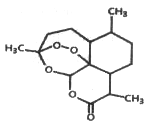
A.青蒿素在碱性条件下可发生水解反应
B.青蒿素中—O—O—有较强的氧化性
C.青蒿素易溶于水、乙醇、苯
D.青蒿素分子式为C15H22O5
(6)环扁桃酯是用于治疗心脑血管疾病的重要化合物.它的一种合成路线如下。

已知:
红外吸收光谱表明E有C=O健。F的分子式为C8H6Cl2O
①A的结构简式是____________________。
②B→D的化学方程式是___________________________________。
③能发生银镜反应的E的同分异构体有__________种。
④E→F的反应类型是___________________。
⑤X的结构筒式是_______________________。
⑥生成环扁桃酯的化学方程式是_____________________。
⑦写出由B合成 的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系.箭头上注明试剂和反应条件)___________________________
的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系.箭头上注明试剂和反应条件)___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 钠与冷水:Na+2H2O===Na++2OH-+H2↑
B. Al与稀HCl:2Al+6H+===2Al3++3H2↑
C. Fe与稀H2SO4:2Fe+6H+===2Fe3++3H2↑
D. Al与NaOH溶液:Al+OH-===AlO![]() +H2↑
+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示实验装置,烧瓶内充满氯气,底部有一层细沙(不参与反应),玻璃导管下口b处塞有一小块钠。从a口伸入一根细铁丝把钠块捅下去,再用滴管从a口滴下几滴水,恰好落在钠块上,立即剧烈反应。下列对此实验的说法中,不正确的是( )

A. 氯气应用向上排空气法收集
B. 玻璃导管只起到加入钠和水的作用
C. 反应中,烧瓶内产生大量白色烟雾
D. 烧瓶中Cl2可能参与四个氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按下列要求填空
I. (1)乙炔的电子式_______________
(2)高聚物![]() 其单体的结构简式为_______________
其单体的结构简式为_______________
(3)  的名称(系统命名法)_____________
的名称(系统命名法)_____________
II.某芳香族化合物的分子式为C7H8O
(4)根据下列实验现象确定其结构简式(要求:每小题只需给出一个答案即可)
①不能与金属钠反应,其结构简式__________________。
②能与钠反应,但遇FeCl3不显色_________________。
③能与钠反应且遇FeCl3显紫色____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)钾云母的化学式为K2H4Al6Si6O24,其简单氧化物表示形式为_____________。
(2)长石的化学式为KAlSi3Ox,x=____。
(3)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_________。
(4)向明矾水溶液中滴加过量氨水,现象是__________________________,反应的离子方程式______________________________________________,再向其中加入过量NaOH溶液,反应的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_____________。
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL 煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________。
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是______________________
(5)丁组同学利用下列各图方案制备Fe(OH)2能较长时间看到Fe(OH)2白色沉淀的是________(填序号)。


(6)戊组同学为了检验硫酸铁中含有的Fe2+应选用________(选填序号)并写出离子方程式______________
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在泡沫橡胶的制造中,发生以下反应:H2O2→2H2O+O2↑,其中,H2O2是( )
A. 氧化剂 B. 既是氧化剂又是还原剂
C. 还原剂 D. 既不是氧化剂也不是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ能量,根据如图中的能量图,回答下列问题:
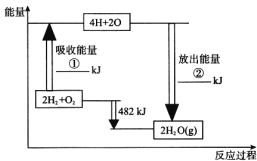
(1)分别写出①②的数值:
①__________;②__________。
(2)生成H2(Xg)中的1 mol H—O键放出__________kJ的能量。
(3)已知:H2O(l)![]() H2O(g)△H=+44 kJ mol1,试写出氢气在氧气中完全燃烧生成液态水的热化学方程式:___________________________________。
H2O(g)△H=+44 kJ mol1,试写出氢气在氧气中完全燃烧生成液态水的热化学方程式:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com