
����Ŀ����֪��1 mol�����еĻ�ѧ����Ҫ����436 kJ��������1 mol�����еĻ�ѧ����Ҫ����498 kJ������������ͼ�е�����ͼ���ش��������⣺
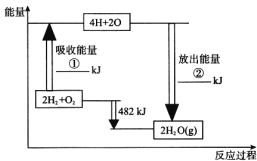
��1���ֱ�д���٢�����ֵ��
��__________����__________��
��2������H2(Xg)�е�1 mol H��O���ų�__________kJ��������
��3����֪��H2O(l)![]() H2O(g)��H��+44 kJ mol1����д����������������ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��___________________________________��
H2O(g)��H��+44 kJ mol1����д����������������ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��___________________________________��
���𰸡���1����1370 ��1 852
��2��463
��3��2H2(g)+ O2(g)![]() 2H2O��l�� ��H=482 kJ mol1
2H2O��l�� ��H=482 kJ mol1
����������1����������Ϊ����2 mol H��H�����ܵ���ֵ��1 mol O=O�����ܵ��ܺͣ�ͬ���ĵ�������������Ϊ4 mol H��2 mol O�γ�2 mol H2O(g)�ͷŵ����������γ�4 mol H��O���ͷŵ���������2���γ�4 mol H��O���ͷŵ�����Ϊ1 852 kJ��������H2(Xg)�е�1 mol H��O���ų�463 kJ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���軯�ƹ㷺���ڵ�ơ������ȡ���л��ϳ��У������ˮ���ڸ߶��࣬���������д�����
(1)��NaCN��Һ��ͨ��CO2�ܷ�����Ӧ��NaCN+H2O+CO2=HCN+NaHCO3��˵�����ԣ�HCN___(�>����<��)H2CO3��
(2)��CN-Ũ�Ƚϵ͵ķ�ˮ��ֱ����FeSO4 7H2O�������õ�һ����ɫ����M��M��Ħ������Ϊ324 g mol-1����M�Ļ�ѧʽΪ_______��
(3)pH��7.510֮����ͭ�������������£���SO2-�������������ˮ������NH3��̼�����μ������Σ���֪���뷴Ӧ��SO2��O2�����ʵ���֮��Ϊ1:1����÷�Ӧ�����ӷ���ʽΪ___________��
(4)��ҵ�ϳ��ü����Ȼ������������ˮ����ԭ�����£�

�ٵ�һ�ε��м���CNC1��̼Ԫ�صĻ��ϼ�Ϊ________��
��ij���������ˮ��NaCN�ĺ���Ϊ147 mg L-1������10m3�����ķ�ˮ����������Ҫ5 mol L-1��NaClO ��Һ_______L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1 g���ȼ����(N2H4)����ȼ������N2(g)��H2O(g)ʱ���ų�16.7 kJ����������÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
A��N2H4+O2![]() N2+2H2O ��H=534.4 kJ��mol1
N2+2H2O ��H=534.4 kJ��mol1
B��N2H4(g)+O2(g)![]() N2(g)+2H2O(g) ��H=534.4 kJ��mol1
N2(g)+2H2O(g) ��H=534.4 kJ��mol1
C��N2H4(g)+O2(g)![]() N2(g)+2H2O(g) ��H=+534.4 kJ��mol1
N2(g)+2H2O(g) ��H=+534.4 kJ��mol1
D��![]() N2H4(g)+
N2H4(g)+![]() O2(g)
O2(g)![]()
![]() N2(g)+H2O(g) ��H=16.7 kJ��mol1
N2(g)+H2O(g) ��H=16.7 kJ��mol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����Ҫͨ����ܽ��е���
�ٵ���ڵ��۵�Ƣܵ绯ѧ��ʴ
A.�٢�B.�ڢ�C.�ڢ�D.ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. �����£�23 g NO2����NA����ԭ��
B. ��״���£���22.4 L NO��11.2 L O2��Ϻ��Եõ�NA��NO2����
C. ���³�ѹ�£�1 L 0. 1mol/L HF��Һ�к���0.1NA��H+
D. 0.1 mol���ǻ��к��е��ӵ���ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ըϺ������Ƭ���������ʳƷ����ѡ����հ�װ����Ӧ���ó�����װ�������Ӧ�ó���������� �� ��
A. ���� B. ������̼ C. ���� D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������aFe2(SO4) 3��b(NH4) 2SO4��cH2O]�㷺���ڳ�����������ˮ����ҵѭ��ˮ�ľ��������ȡ�ij����������������������������ƣ��������Ϊԭ�ϣ���������¹���������ȡ������李�

��ش��������⣺
��1������������Һ��H2SO4�ữ����ҪĿ����_________________������A����Ҫ�ɷ���_______________��
��2���������������ʺϵ�������B��________����Ӧ�����ӷ���ʽ ��
a��NaClO b��H2O2 c��KMnO4 d��K2Cr2O7
��3�������ס��ҵ����Ʒֱ��ǣ���______________����___________________��
��4�����������У�����֮��ͼ�������֮ǰ����ȡ������Һ����Fe2+�Ƿ���ȫ���������������Լ� �ܷ������Ե�KMnO4��Һ�� (��ܡ����ܡ�)�����ǣ� �����������Ի�ʽ˵����
��5���������������NH4+�ķ�����____________________________��
��6����ȡ14.00 g��Ʒ����������ˮ���Ƴ�100 mL��Һ���ֳ����ȷݣ�������һ���м�������NaOH��Һ������ϴ�ӵõ�2.14 g����������һ����Һ�м���0.05 mol Ba (NO3) 2��Һ��ǡ����ȫ��Ӧ�����������淋Ļ�ѧʽΪ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ʹ�õ�Ũ�����������������һ��Ϊ36.5%���ܶ�Ϊ1.19g/cm3��
��1�����Ũ��������ʵ���Ũ��Ϊ���٣�
��2����ʹ�ø���������250mL1.00mol/L���ᣬ����Ҫ��������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com