
 某研究人员应用如图所表示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.请完成下列问题:
某研究人员应用如图所表示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.请完成下列问题:分析 (1)浓硫酸具有吸水性,可用于干燥气体;
(2)干燥的氯气通入B,不能使干燥的有色布条褪色,再通入湿润的有色布条,布条褪色,证明干燥氯气不具有漂白性,次氯酸具有漂白性;
(3)反应:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中Mn元素的化合价降低,MnO2属于氧化剂,Cl元素化合价升高,HCl属于还原剂,根据元素化合价的升降结合化学方程式进行计算.
解答 解:(1)浓硫酸具有吸水性,可用于除去氯气中的水蒸气,
故答案为:除去Cl2中的水蒸气;
(2)通入Cl2后,集气瓶B中干燥的有色布条不褪色,可说明干燥的氯气不能使有色布条褪色,集气瓶C中湿润的有色布条,可说明湿润的氯气能使有色布条褪色,
故答案为:干燥的Cl2不能使有色布条褪色(或干燥的Cl2无漂白性);湿润的Cl2能使有色布条褪色(或湿润的Cl2有漂白性);氯气能和水反应,湿润的Cl2有漂白性;
(3)①反应:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中Mn元素的化合价降低,MnO2属于氧化剂,Cl元素化合价升高,HCl属于还原剂,Cl2是氧化产物,氧化剂的氧化性强于氧化产物的氧化性,即MnO2>Cl2,故答案为:MnO2;Cl2;MnO2;Cl2;
②浓盐酸中氯元素一部分转化为氯气,一部分转化为氯化锰,在反应中盐酸显示出来的性质是还原性和酸性,故答案为:B;
③MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,若产生22.4L即1molCl2,则反应中转移的电子2mol,生成氯化锰1mol,若产生2.24L即0.1molCl2,则反应中转移的电子为0.2mol,数目是0.2NA,生成氯化锰是0.1mol,12.6g,故答案为:0.2NA;12.6.
点评 本题考查氧化还原反应,题目难度不大,注意根据化合价变化的角度较大该题,氧化还原反应中得失电子的数目等于化合价变化的数目.


 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:选择题
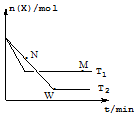 一定温度下,向某密闭容器中通入X,发生反应:4X(g)?2Y(g)+Z(g)△H,在温度分别为T1、T2 的条件下X的物质的量n(X) 随时间t的变化曲线如图所示.下列有关叙述错误的是( )
一定温度下,向某密闭容器中通入X,发生反应:4X(g)?2Y(g)+Z(g)△H,在温度分别为T1、T2 的条件下X的物质的量n(X) 随时间t的变化曲线如图所示.下列有关叙述错误的是( )| A. | △H<0 | |
| B. | 平衡时Z的产率:T2<T1 | |
| C. | M、N、W三点对应的混合气体的平均相对分子质量:W>M>N | |
| D. | M点的正反应速率大于N点的逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
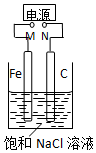
| A. | M接电源正极,N接电源负极,将C电极换成Cu电极,电解质溶液换成CuSO4溶液,则可实现在铁上镀铜 | |
| B. | M接负极,N接正极,在溶液中滴人酚酞试液,C电极周围溶液变红 | |
| C. | M接负极,N接正极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 | |
| D. | M接负极,N接正极,当两极产生气体总量为22.4 L(标准状况)时,生成1molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子有7个σ键和1个π键 | |
| B. | 丙烯分子中有3个碳原子在同一直线上 | |
| C. | 丙烯分子中3个碳原子都是sp3杂化面上 | |
| D. | 丙烯分子存在非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到平衡时,X与Y 的浓度相等 | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 以X浓度变化表示的反应速率为0.01 mol/(L•s) | |
| D. | 若升高温度Y的转化率减小,则正反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
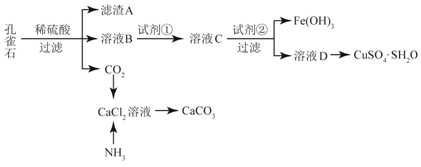
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤⑥⑧ | B. | ③⑤⑧ | C. | ②④ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 5:3 | C. | 3:2 | D. | 7:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com