
【题目】反应![]() 在一容积可变的密闭容器中进行,试回答:
在一容积可变的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率__________(填“增大”“不变”或“减小”,下同)。
(2)将容器的体积缩小一半,其反应速率__________。
(3)保持体积不变,充入![]() 使体系压强增大,其反应速率__________。
使体系压强增大,其反应速率__________。
(4)保持压强不变,充入![]() 使容器的体积增大,其反应速率__________。
使容器的体积增大,其反应速率__________。
【答案】不变 增大 不变 减小
【解析】
(1)改变纯固体的量,对反应速率无影响;
(2)将容器的体积缩小一半,气体的浓度变大,反应速率加快;
(3)保持体积不变,充入N2使体系压强增大,反应体系中各物质的浓度不变;
(4)保持压强不变,充入N2使容器的体积增大,反应体系中气体的浓度减小。
(1)因铁是固体,增加铁的量,不能改变反应速率,答案为不变;
(2)容器的体积缩小一半,容器内各气体物质的浓度都增大,浓度越大,化学反应速率越快,答案为增大;
(3)体积不变,冲入![]() 使压强增大, 但各物质的浓度不变,所以反应速率不变,答案为不变;
使压强增大, 但各物质的浓度不变,所以反应速率不变,答案为不变;
(4)保持压强不变,冲入![]() 使容器的体积增大,各气体物质的浓度都减小,浓度越小,反应速率越小,答案为减小。
使容器的体积增大,各气体物质的浓度都减小,浓度越小,反应速率越小,答案为减小。


科目:高中化学 来源: 题型:
【题目】对于可逆反应mA(g)+nB(s)![]() pC(g)+qD( g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是
pC(g)+qD( g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是
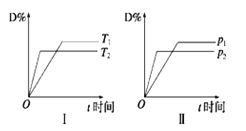
A.化学方程式中化学计量数:p+q> m+n
B.降温可使化学平衡向正反应方向移动
C.使用合适的催化剂可使D%有所增加
D.加入少量的B,正反应速率加快,有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有硫酸钠和碳酸钠混合溶液10.0 mL,加入足量氯化钡溶液,充分反应后,经过滤、洗涤和干燥,得到白色沉淀1.451 g。将沉淀与过量盐酸反应,得到112 mL 二氧化碳气体(在标准状况下)。求原混合溶液中硫酸钠和碳酸钠的物质的量浓度分别是多少?________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积).下列分析正确的是
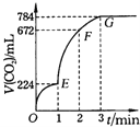
A.OE、EF、FG三段中,该反应用CO2表示的平均反应速率之比为2:6:7
B.EF段,用盐酸表示该反应的平均反应速率为2.4mol/(Lh)
C.G点表示收集的CO2的量最多
D.OE段表示的平均速率最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
①C2H2(g)+![]() O2(g)
O2(g)![]() 2CO2(g)+H2O(l) ΔH1=-1 301.0 kJ·mol-1
2CO2(g)+H2O(l) ΔH1=-1 301.0 kJ·mol-1
②C(s)+O2(g)![]() CO2(g) ΔH2=-393.5 kJ·mol-1
CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH3=-285.8 kJ·mol-1
H2O(l) ΔH3=-285.8 kJ·mol-1
则反应④2C(s)+H2(g)![]() C2H2(g)的ΔH为( )
C2H2(g)的ΔH为( )
A. -228.2 kJ·mol-1B. +228.2 kJ·mol-1
C. +1301.0 kJ·mol-1D. +621.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+ O2(g)![]() 2SO3(g)能量变化如右图所示。 已知1mol SO2(g)完全转化为1mol SO3(g)放热99 kJ。请回答:
2SO3(g)能量变化如右图所示。 已知1mol SO2(g)完全转化为1mol SO3(g)放热99 kJ。请回答:
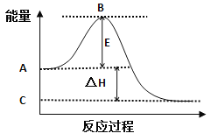
(1)E的大小对该反应的△H _______(填“有” 或“无”)影响。该反应常用V2O5作催化剂,加入V2O5会使图中B点_________(填“升高”、“降低”或“不变”),原因是____________________。
(2)V2O5 的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物,四价钒化合物再被氧气氧化。写出该催化循环机理的两个化学方程式:______、_______。
(3)已知单质硫的标准燃烧热为296kJ·mol-1,则常温常压下,由单质硫和氧气经两步反应,若生成3mol SO3(g),放出的总热量为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热(不与外界发生热交换)的恒容容器中,发生反应:2A(g)+B(s) ![]() C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤C(g)的物质的量浓度不变
⑥容器内A、C、D三种气体的浓度之比为2:1:1 ⑦某时刻v(A)=2v(C)且不等于零
⑧单位时间内生成n mol D,同时生成2n mol A
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的原料都是来源于石油化工,回答下列问题。
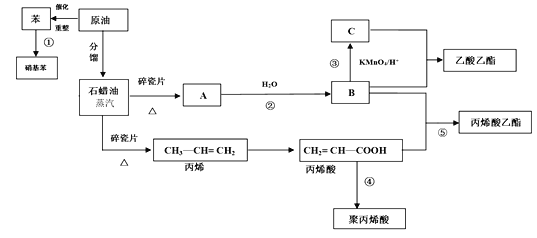
(1)丙烯酸中的官能团的名称为_______。
(2)反应①的化学方程式_______;反应⑤的化学方程式_______。
(3)丙烯酸(CH2 = CH—COOH)可能发生的反应有_______(填序号)
A.加成反应 B.取代反应 C.加聚反应 D.中和反应 E.氧化反应
(4)聚丙烯酸的结构简式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com