
【题目】在容积为2 L的恒容密闭容器中充入1 mol CO2(g)和3.5 mol H2(g),在一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol。该反应的平衡常数K与温度T的关系如图1所示,CO2的转化率如图2所示,下列说法错误的是
CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol。该反应的平衡常数K与温度T的关系如图1所示,CO2的转化率如图2所示,下列说法错误的是

A. 在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系
B. 该温度下,平衡常数K=0.25
C. 其他条件不变下,图2中x可表示温度或压强或投料比c(CO2)/c(H2)
D. 用二氧化碳合成甲醇体现了碳减排理念
【答案】C
【解析】
在容积为2 L的恒容密闭容器中充入1 mol CO2(g)和3.5 mol H2(g),在一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol,
CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol,
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始(mol) 1 3.5 0 0
反应(mol) 0.5 1.5 0.5 0.5
平衡(mol) 0.5 2 0.5 0.5
据此分析解答。
A.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0,为放热反应,升高温度,平衡逆向移动,平衡常数K减小,因此在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系,故A正确;
CH3OH(g)+H2O(g) ΔH<0,为放热反应,升高温度,平衡逆向移动,平衡常数K减小,因此在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系,故A正确;
B.根据上述分析,该温度下,平衡常数K=![]() =
=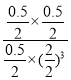 = 0.25,故B正确;
= 0.25,故B正确;
C.根据CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0,温度升高,平衡逆向移动,二氧化碳的转化率降低,与图像相符;压强增大,平衡正向移动,二氧化碳的转化率增大,与图像不符;投料比c(CO2)/c(H2)增大,二氧化碳的转化率减小,与图像相符;因此图2中x不可以表示压强,故C错误;
CH3OH(g)+H2O(g) ΔH<0,温度升高,平衡逆向移动,二氧化碳的转化率降低,与图像相符;压强增大,平衡正向移动,二氧化碳的转化率增大,与图像不符;投料比c(CO2)/c(H2)增大,二氧化碳的转化率减小,与图像相符;因此图2中x不可以表示压强,故C错误;
D.用二氧化碳合成甲醇,能够减少二氧化碳的排放量,体现了碳减排理念,故D正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物瑞德西韦(Remdesivir)对新型冠状病毒感染者有潜在的治疗效果:K为药物合成的中间体,其合成路线如图所示:
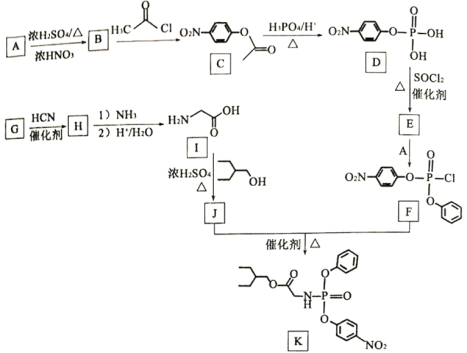
已知以下信息
①![]()
②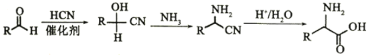
回答下列问题:
(1)B的化学名称为____________。
(2)J中含有官能团的名称为____________。
(3)由B生成C的反应类型为____________。
(4)由G生成H的化学反应方程式____________。
(5)E中含两个Cl原子,则E的结构简式____________。
(6)X是C的同分异构体,写出任意一个满足下列条件的X的结构简式____________。
①苯环上含有硝基且苯环上只有一种氢原子;
②遇FeCl3溶液发生显色反应:
③1mol的X与足量金属Na反应可生成2gH2。
(7)设计由苯甲醇(![]() )为原料合成化合物
)为原料合成化合物![]() 的路线____________(其他试剂任选)。
的路线____________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种新型高分子材料的结构简式如图,对此高聚物叙述正确的是( )
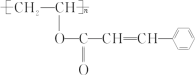
A.化学式为(C11H11O2)n
B.可以发生水解反应、氧化反应,不能发生取代反应
C.1mol该有机物分子最多能和4molH2发生加成反应
D.该高分子材料是由两种单体经酯化后加聚而成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)NH3的电子式______。
(2)氯化铵水溶液显酸性,其原因为______(用离子方程式表示),0.1mol/L的氨水中加入少量的NH4Cl固体,溶液的pH______(填“升高”或“降低”);若加入少量的明矾固体后,请尝试从平衡移动的角度解释溶液中NH4+浓度的变化原因______。
(3)硝酸铵加热分解可得到N2O(g)和H2O(g),250℃时,硝酸铵在密闭容器中分解达到平衡,该温度下反应的平衡常数表达式为______;若有1mol硝酸铵完全分解,转移的电子数为______mol。
(4)3H2(g)+N2(g)2NH3(g)△H=-92kJ/mol,若反应放出9.2kJ 热量,则参加反应的氢气分子数目为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的气化是高效、清洁地利用煤炭的重要途径之一.
(1)在25℃、101kPa时,H2与O2化合生成1molH2O(g)放出241.8kJ的热量,其热化学方程式为______.
又知:①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
②CO(g)+![]() O2(g)═CO2(g)△H=-283.0kJ/mol
O2(g)═CO2(g)△H=-283.0kJ/mol
焦炭与水蒸气反应是将固体煤变为气体燃料的方法,C(s)+H2O(g)═CO(g)+H2(g)△H=______kJ/mol.
(2)CO可以与H2O(g)进一步发生反应:CO(g)+H2O(g)CO2(g)+H2(g)△H<0在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0.
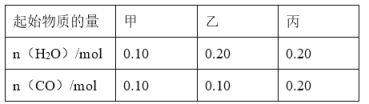
①该反应的平衡常数表达式为______.
②平衡时,甲容器中CO的转化率是______;容器中CO的转化率:乙______甲;丙______甲.(填“>”、“=”或“<”)
③丙容器中,通过改变温度,使CO的平衡转化率升高,则温度______(填“升高”或“降低”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=________。
(2)丙溶液中存在的电离平衡为______________(用电离平衡方程式表示)。
(3)常温下,用水稀释0.1 mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是________(填序号)。
①n(H+) ②c(H+) ③ c(CH3COOH)/c(CH3COO-) ④c(OH-)
(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为___________。
(5)某同学用甲溶液分别滴定20.00 mL乙溶液和20.00 mL丙溶液,得到如图所示的两条滴定曲线,请回答有关问题:
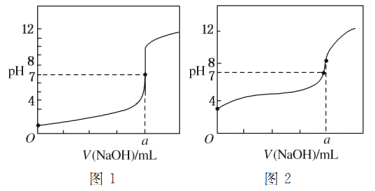
①甲溶液滴定丙溶液的曲线是________(填“图1”或“图2”)曲线。
②a=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用新型甲醇燃料电池作电源电解硫酸铜溶液,下列有关说法不正确的是( )
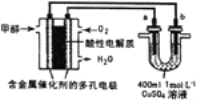
A.甲醇一极的电极反应式为CH3OH-6e-+H2O= CO2↑+6H+
B.若a为粗钢,b为精铜,消耗标准状况下224mL O2,则a极质量减少1.28g
C.若a. b均为石墨,a极反应为:2H2O-4e-= 4H+ +O2↑
D.若a为石墨,b为铜,消耗标准状况下224mLO2,则电解后CuSO4溶液的pH为1(忽略溶液体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其中一种理论为厌氧细菌可促使SO42-与H2反应生成S2-,加速钢管的腐蚀,其反应原理如图所示。下列说法正确的是
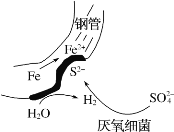
A.正极的电极反应式为O2+4e-+2H2O=4OH-
B.钢管腐蚀的直接产物中含有FeS、Fe(OH)2
C.SO42-与H2的反应可表示为4H2+SO42--8e- S2-+4H2O
S2-+4H2O
D.在钢管表面镀锌或铜可减缓钢管的腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com