
����Ŀ�����Ǻϳ����ᡢ��κ͵��ʵĻ���ԭ�ϣ��ش��������⣺
��1��NH3�ĵ���ʽ______��
��2���Ȼ��ˮ��Һ�����ԣ���ԭ��Ϊ______�������ӷ���ʽ��ʾ����0.1mol/L�İ�ˮ�м���������NH4Cl���壬��Һ��pH______������������������������������������������������볢�Դ�ƽ���ƶ��ĽǶȽ�����Һ��NH4+Ũ�ȵı仯ԭ��______��
��3������識��ȷֽ�ɵõ�N2O��g����H2O��g����250��ʱ����������ܱ������зֽ�ﵽƽ�⣬���¶��·�Ӧ��ƽ�ⳣ������ʽΪ______������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ______mol��
��4��3H2��g��+N2��g��2NH3��g����H=-92kJ/mol������Ӧ�ų�9.2kJ ��������μӷ�Ӧ������������ĿΪ______��
���𰸡�![]() NH4++H2ONH3H2O+H+ ���� ���������������������������������ӷ�Ӧ���ٽ�һˮ�ϰ��ĵ��룬��Һ�е�NH4+��Ũ������ K=c��N2O����c2��H2O�� 4 0.3NA
NH4++H2ONH3H2O+H+ ���� ���������������������������������ӷ�Ӧ���ٽ�һˮ�ϰ��ĵ��룬��Һ�е�NH4+��Ũ������ K=c��N2O����c2��H2O�� 4 0.3NA
��������
��1������ԭ�Ӻ���ԭ�ӹ��õ��ӶԵ����дNH3�ĵ���ʽ��
��2���Ȼ��ˮ��Һ��ˮ�������ԣ��ݴ�д���ӷ���ʽ��0.1mol/L�İ�ˮ�м���������NH4Cl���壬��ͬ����ЧӦ�Ե���ƽ���Ӱ���ж���Һ��pH�仯��������������������������������Ӷ�ˮ����ƽ���Ӱ���ж�NH4+Ũ�ȵı仯��ԭ��
��3��������識��ȷֽ�ɵõ�N2O(g)��H2O(g)��д250��ʱ����������ܱ������зֽ�Ļ�ѧ����ʽ���ݴ�д���¶��·�Ӧ��ƽ�ⳣ������ʽ��������立ֽⷽ��ʽ�����������ӵ����ʵ����Ĺ�ϵ������ת�Ƶĵ�������
��4����3H2(g)+N2(g)2NH3(g)��H=-92kJ/mol��ʵ�����ĵ����������ʵ�����ų������Ĺ�ϵ���ɼ���ų�9.2kJ ����ʱ�μӷ�Ӧ������������Ŀ��
��1�������ǹ��ۻ����Nԭ�Ӻ�Hԭ��֮���Թ��ۼ����ϣ��������ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��2���Ȼ�淋�ˮ��Һ�������ԣ���ԭ��ΪNH4++H2ONH3H2O+H+��0.1molL-1�İ�ˮ�м���������NH4Cl���壬�����Ũ����������һˮ�ϰ��ĵ��룬����������Ũ�ȼ�С����Һ��pH���ͣ������������������������������������ӷ�Ӧ���ٽ�һˮ�ϰ��ĵ��룬��Һ�е�NH4+��Ũ������
�ʴ�Ϊ��NH4++H2ONH3H2O+H+�� ���ͣ� ���������������������������������ӷ�Ӧ���ٽ�һˮ�ϰ��ĵ��룬��Һ�е�NH4+��Ũ������
��3������立ֽ�����N2O��H2O���ﵽƽ�⣬˵��Ϊ���淴Ӧ����ѧ��Ӧ����ʽΪ��NH4NO3![]() N2O+2H2O��250��ʱ��ˮΪ����״̬����ƽ�ⳣ��K=c(N2O)��c2(H2O)��NH4NO3��NH4+��NԪ�ػ��ϼ�Ϊ-3�ۣ�NO3-�е�NԪ�صĻ��ϼ�Ϊ+5�ۣ���Ӧ��NԪ�صĻ��ϼ�Ϊ+1�ۣ��������з�Ӧ��NԪ����-3������Ϊ+1�ۣ��˷�Ӧ��ÿ�ֽ�1mol����泥�ת�Ƶ�����Ϊ4mol��
N2O+2H2O��250��ʱ��ˮΪ����״̬����ƽ�ⳣ��K=c(N2O)��c2(H2O)��NH4NO3��NH4+��NԪ�ػ��ϼ�Ϊ-3�ۣ�NO3-�е�NԪ�صĻ��ϼ�Ϊ+5�ۣ���Ӧ��NԪ�صĻ��ϼ�Ϊ+1�ۣ��������з�Ӧ��NԪ����-3������Ϊ+1�ۣ��˷�Ӧ��ÿ�ֽ�1mol����泥�ת�Ƶ�����Ϊ4mol��
�ʴ�Ϊ��K= c(N2O)��c2(H2O)��4��
��4��3H2(g)+N2(g)2NH3(g)��H=-92kJ/mol����֪�ų�92kJ����ʱ����������Ϊ3mol���ʵ���Ӧ�ų�9.2kJ ��������μӷ�Ӧ������Ϊ0.3mol��������Ϊ0.3NA��
�ʴ�Ϊ��0.3NA��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ѧ�м��ֳ������ʵ�ת����ϵ����ͼ�����ֲ���δ�г�����A��һ�ֽ������ʣ�D��һ�ַǽ������嵥�ʡ�
��ش��������⣺

��1��A��C�Ļ�ѧʽ�ֱ�ΪA_________��C_________��
��2��F��Ũ��Һ��A��Ӧ�����У�F���ֵ����������з�Ӧ��H2SO4���ֵ�������ȫ��ͬ����_____��
A��C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O
CO2��+2SO2��+2H2O
B��Fe+H2SO4�TFeSO4+H2��
C��Cu+2H2SO4��Ũ��![]() CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O
D��FeO+H2SO4�TFeSO4+H2O
��3��д����ӦE+H2O2��F�Ļ�ѧ����ʽ��____________��
��4������ӦF+D��Eת�Ƶ�����Ϊ6.02��1023��������D������Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ��þ�ĺϽ�4.6 g��ȫ����Ũ���ᣬ����Ӧ�����ᱻ��ԭֻ����4 480 mL NO2�����336 mL��N2O4����(�������������㵽��״��)���ڷ�Ӧ�����Һ�У���������������������Һ�����ɳ���������Ϊ (����)
A.9.02 gB.8.51 gC.8.26 gD.7.04 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�ص�ԭ����������ij�ֳ������ϼ۵Ĺ�ϵͼ������ԭ��������������Ӧ��Ԫ�أ�������˵����ȷ����

A.31d��33d����ͬ�ֺ���
B.��̬�⻯����ȶ��ԣ�a>d>e
C.��ҵ�ϳ��õ�ⷨ�Ʊ�����b
D.a��b�γɵĻ����ﲻ���ܺ����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش���������:
(1)���з�Ӧ���ڷ��ȷ�Ӧ����_______��
A.��Ƭ��ϡH2SO4��Ӧ��ȡH2B.̼��Ƹ��·ֽ�������ƺͶ�����̼ C.�������������������ֽ�D.Ba(OH)2��8H2O��NH4Cl���巴Ӧ
(2)һ�������£�2L�ܱ�������SO2��O2��Ӧ5min����SO2��SO3���ʵ����ֱ�Ϊ0.1 mol��0.3mol����SO2��ʼ���ʵ���Ũ��Ϊ___����O2��ʾ���ʱ��û�ѧ��Ӧ����Ϊ______��
(3)�û���̿��ԭ��������������йط�ӦΪC(s)+2NO(g)![]() N2(g)+CO2(g)��ij�о�С��������ܱ������м���һ�����Ļ���̿��NO������(T��)�����·�Ӧ������˵��������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��־����________(��ѡ����ĸ)
N2(g)+CO2(g)��ij�о�С��������ܱ������м���һ�����Ļ���̿��NO������(T��)�����·�Ӧ������˵��������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��־����________(��ѡ����ĸ)
A.����̿���������ֲ��� B.v��(N2)=2v��(NO) C.����������ѹǿ���ֲ��� D.�����ڻ��������ܶȱ��ֲ��� E.�����ڻ�������ƽ����Է����������ֲ��� F.������CO2��Ũ�ȱ��ֲ���
(4)���÷�Ӧ6NO2+8NH3=7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ���������û�ѧ�ܣ�װ����ͼ��ʾ��

��A�缫�ĵ缫��ӦʽΪ_______________��
�����й��ڸõ�ص�˵����ȷ����___________(��ѡ����ĸ)��
A.���Ӵ��Ҳ�缫�������غ��������缫 B.���ӽ���ĤΪ�����ӽ���Ĥ����OH-���Ҳ���Һ���������Һ C. ����4.48L NO2������ʱ��ת�Ƶ��ӵ����ʵ���Ϊ0.8mol
(5)�ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̡���֪: 1molN2��3molH2��Ӧ����2molNH3ʱ�ų�����93kJ���Ը��ݱ������м������ݼ���a����ֵ_______��
��ѧ�� | H��H | N��H | N��N |
����kJ/mol | 436 | a | 945 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú�������Ǹ�Ч����������ú̿����Ҫ;��֮һ��
��1����25����101kPaʱ��H2��O2��������1molH2O��g���ų�241.8kJ�����������Ȼ�ѧ����ʽΪ______��
��֪����C��s��+O2��g���TCO2��g����H=-393.5kJ/mol
��CO��g��+![]() O2��g���TCO2��g����H=-283.0kJ/mol
O2��g���TCO2��g����H=-283.0kJ/mol
��̿��ˮ������Ӧ�ǽ�����ú��Ϊ����ȼ�ϵķ�����C��s��+H2O��g���TCO��g��+H2��g����H=______kJ/mol��
��2��CO������H2O��g����һ��������Ӧ��CO��g��+H2O��g��CO2��g��+H2��g����H��0�ڼס��ҡ������������ܱ������У���ʼʱ�����±�����Ͷ�ϣ���800��ʱ�ﵽƽ��״̬��K=1.0��
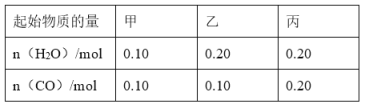
���÷�Ӧ��ƽ�ⳣ������ʽΪ______��
��ƽ��ʱ����������CO��ת������______��������CO��ת���ʣ���______�ף���______�ף���������������=������������
���������У�ͨ���ı��¶ȣ�ʹCO��ƽ��ת�������ߣ����¶�______��������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300 ��ʱ,��2 mol A��2 mol B������������2 L�ܱ������У��������·�Ӧ:3A(g)+B(g) ![]() 2C(g)+2D(g)��H=Q��2 minĩ�ﵽƽ��,����0.8 mol D��
2C(g)+2D(g)��H=Q��2 minĩ�ﵽƽ��,����0.8 mol D��
(1)300 ��ʱ,�÷�Ӧ��ƽ�ⳣ������ʽΪ:K=______����֪K300 ��<K350 ��,����H______0(����>������<��)��
(2)���¶Ȳ���,��С�����ݻ�,��A��ת����________(��������������С������������),ԭ����_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú̿ȼ��ʱ��������SO2��NO�Ի���Ӱ�켫��
(1)ʹ�������Դ����Ч����SO2�ȵ��ŷš�ú��Һ�����ִ���Դ��ҵ���ص��ƹ����Դ�ۺ����÷����������Һ������Ϊ��ú����CH3OH����֪�Ʊ��״����йػ�ѧ��Ӧ��ƽ�ⳣ�����£�
i��CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)����H1����a kJ/mol
CH3OH(g)��H2O(g)����H1����a kJ/mol
ii��CO2(g)��H2(g) ![]() CO(g)��H2O(g) ��H2����b kJ/mol
CO(g)��H2O(g) ��H2����b kJ/mol
iii��CO(g)��2H2(g) ![]() CH3OH(g)����H3
CH3OH(g)����H3
��H3��________��
(2)���ܱ������н��з�Ӧi���ı��¶�ʱ���÷�Ӧ�е��������ʶ�Ϊ��̬����ʼ�¶ȡ������ͬ(T1 �桢2 L�ܱ�����)����Ӧ�����в������ݼ��±���
��Ӧʱ�� | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
��Ӧ��� �º��� | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
��Ӧ��� �Ⱥ��� | 0 min | 0 | 0 | 2 | 2 |
�ٴﵽƽ���Ӧ��Աȣ�ƽ�ⳣ��K(��)________K(��)(�>����<��������ͬ)��ƽ��ʱCO2��Ũ��c(��)________c(��)��
�ڶԷ�Ӧ�����������������£���30 minʱֻ�ı��¶�ΪT2 �棬�ٴ�ƽ��ʱH2�����ʵ���Ϊ2.5 mol����T1________T2(�>����<������)��
����30 minʱֻ���������ٳ���1 mol H2(g)��1 mol H2O(g)����ƽ��________�ƶ�(�����������)��
(3)�о���Ա���֣���ú̿��O2/CO2��������ȼ�գ��ܹ�����ȼúʱNO���ŷţ���Ҫ��ӦΪ��2NO(g)��2CO(g)=N2(g)��2CO2(g)����һ���¶��£���2 L�ĺ����ܱ������г���0.1 mol NO��0.3 mol CO�����÷�Ӧ����ͼΪ�����ڵ�ѹǿ(p)����ʼѹǿ(p0)�ı�ֵ(p/p0)��ʱ��ı仯���ߡ�
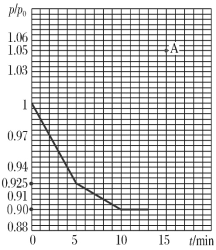
��0��5 min�ڣ��÷�Ӧ��ƽ����Ӧ����v(NO)��________��ƽ��ʱN2�IJ���Ϊ________��
����13 minʱ������������ٳ���0.06 mol CO2��15 minʱ�ٴδﵽƽ�⣬��ʱ������![]() /
/![]() �ı�ֵӦ��ͼ��A���________(��Ϸ������·���)��
�ı�ֵӦ��ͼ��A���________(��Ϸ������·���)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״�����Т�6.72LCH4����3.01x1023��HCl����13.6gH2S����0.2molNH3�����ж���������Ĺ�ϵ��С�����ʾ����ȷ����( )
A.���:�ܣ��٣��ڣ���
B.�ܶ�:�٣��ܣ��ۣ���
C.�������ܣ��٣��ۣ���
D.��ԭ����:�ڣ��ܣ��ۣ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com