
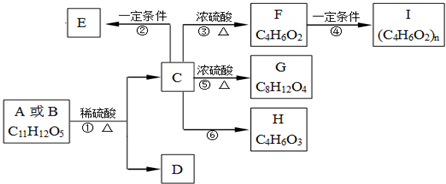
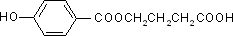 ,B为
,B为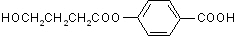 ,D为
,D为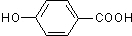 ,C发生缩聚反应生成高聚物E为
,C发生缩聚反应生成高聚物E为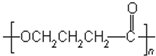 ,F发生加聚反应生成高聚物I为
,F发生加聚反应生成高聚物I为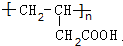 ,
,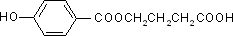 ,B为
,B为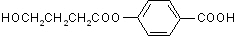 ,D为
,D为 ,C发生缩聚反应生成高聚物E为
,C发生缩聚反应生成高聚物E为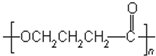 ,F发生加聚反应生成高聚物I为
,F发生加聚反应生成高聚物I为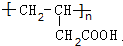 ,
, ,D中所含官能团的名称是:羟基和羧基,
,D中所含官能团的名称是:羟基和羧基,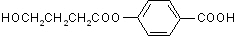 ,
,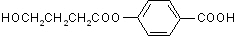 ;
;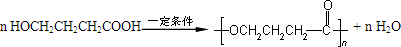 ;
;| △ |
 ;OHCCH2CH2COOH+2Cu(OH)2
;OHCCH2CH2COOH+2Cu(OH)2| △ |
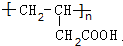 ,I中不含不饱和键,所以不可使溴水褪色,故错误;
,I中不含不饱和键,所以不可使溴水褪色,故错误; ,D在一定条件下可以发生缩聚反应形成高聚物,故正确;
,D在一定条件下可以发生缩聚反应形成高聚物,故正确;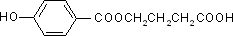 ,B为
,B为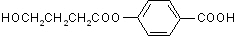 ,二者互为同分异构体,等质量的A与B,物质的量相等,每摩尔物质都消耗3molNaOH,故正确;
,二者互为同分异构体,等质量的A与B,物质的量相等,每摩尔物质都消耗3molNaOH,故正确; ,对应的同分异构体中①核磁共振氢谱显示有四种峰,峰面积之比为:1:1:2:2,说明含有4种H原子且这四种H原子数目之比为1:1:2:2,②与FeCl3溶液发生显色反应,说明含有酚羟基,③发生银镜反应,但不能水解,应含有醛基,不含酯基,
,对应的同分异构体中①核磁共振氢谱显示有四种峰,峰面积之比为:1:1:2:2,说明含有4种H原子且这四种H原子数目之比为1:1:2:2,②与FeCl3溶液发生显色反应,说明含有酚羟基,③发生银镜反应,但不能水解,应含有醛基,不含酯基,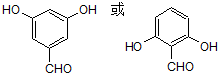 ,
,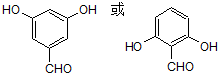 .
.


科目:高中化学 来源: 题型:
| A、焓是一个物理量,符号为H,单位为mol?L可以测量 |
| B、焓变就是反应热,二者没有区别 |
| C、公式△H--T△S中的△H是反应的焓变 |
| D、焓变△H只有大小,没有正负之分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| B、锌与18.4mol?L的H2SO4溶液反应:Zn+2H+=Zn2++H2↑ |
| C、用NaOH溶液吸收氯气:C12+2OH-=Cl-+ClO-+H2O |
| D、稀H2SO4与Ba(OH)2溶液反应:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
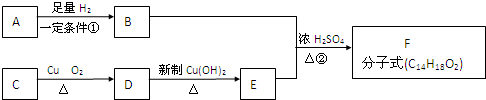
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | a | b | c |
| 合金质量(mg) | 510 | 765 | 918 |
| 气体体积(mL) | 560 | 672 | 672 |
查看答案和解析>>
科目:高中化学 来源: 题型:
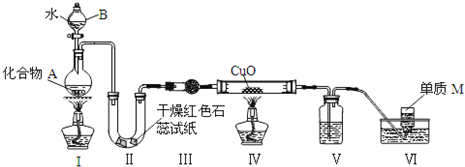
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 答案 | 实验方法 |
| 检验Cl2 | A、焰色反应(透过蓝色的钴玻璃) | |
| 检验氨气 | B、先加盐酸,再加氯化钡溶液 | |
| 检验K+ | C、淀粉碘化钾试纸 | |
| 检验SO42- | D、湿润的红色石蕊试纸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com