
 ,D为
,D为 、C为
、C为 ,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
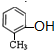 、
、 ,A发生加成反应生成B,B结构简式可能为
,A发生加成反应生成B,B结构简式可能为 ,
, ,据此分析解答.
,据此分析解答. ,D为
,D为 、C为
、C为 ,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
,A、C为同分异构体,且A中含有羟基,A中还含有甲基,甲基和羟基可能位于邻位、间位或对位,所以A的结构简式可能为
 、
、 ,A发生加成反应生成B,B结构简式可能为
,A发生加成反应生成B,B结构简式可能为 ,
, 、
、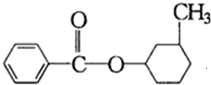 或
或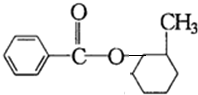 ,
, 、
、 或
或 ,
, 、
、 或
或 ;
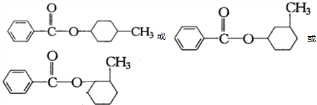
; ,与E互为同分异构体且属于芳香族化合物,说明E的同分异构体中含有苯环,其同分异构体中如果含有酯基,则只有一种结构,如果含有酚羟基和甲基,则有邻、间、对三种结构,所以符合条件的E同分异构体有
,与E互为同分异构体且属于芳香族化合物,说明E的同分异构体中含有苯环,其同分异构体中如果含有酯基,则只有一种结构,如果含有酚羟基和甲基,则有邻、间、对三种结构,所以符合条件的E同分异构体有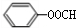 、
、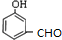 、
、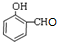 、
、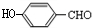 ,
, 、
、 、
、 、
、 ;
; ,
, ,
, ;
; .
.


科目:高中化学 来源: 题型:
| A、1个金属原子失去电子的多少 |
| B、1摩金属失去电子的多少 |
| C、原子失去电子能力的大小 |
| D、1摩金属与水反应放出H2的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在H2O2+Cl2→2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子 |
| B、9克甲基中含有的电子数为10NA |
| C、常温常压下,46克二氧化氮和四氧化二氮混合物中含3NA个原子 |
| D、1mol含五个碳原子的有机物,最多形成4mol碳碳单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
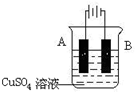
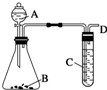 某同学用如图所示装置探究SO2的性质及其有关实验.
某同学用如图所示装置探究SO2的性质及其有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
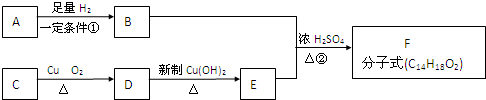
 )是其中的一种,它可以从茉莉花中提取.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取.一种合成路线如下: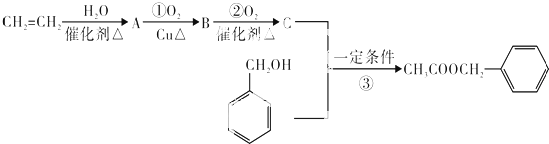
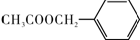 )的说法正确的是
)的说法正确的是查看答案和解析>>
科目:高中化学 来源: 题型:
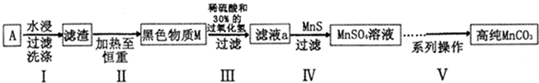
查看答案和解析>>
科目:高中化学 来源: 题型:
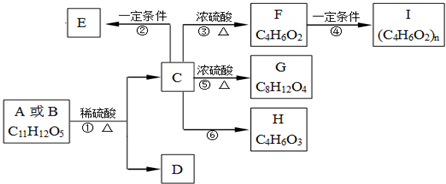
查看答案和解析>>
科目:高中化学 来源: 题型:
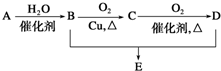 有机物A的产量是衡量一个国家石油工业发展水平的标志,可发生以下系列转化,B、D是生活中常见的两种有机物,下列说法不正确的是( )
有机物A的产量是衡量一个国家石油工业发展水平的标志,可发生以下系列转化,B、D是生活中常见的两种有机物,下列说法不正确的是( )| A、A的结构简式为CH2=CH2 |
| B、1molB物质可以与足量Na反应生成0.5molH2 |
| C、B、D、E三种物质可以用饱和Na2CO3溶液鉴别 |
| D、由B、D制备E浓H2SO4只作吸水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物在常温下均呈气态,在周期表中Z与W左右相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的最外层电子数相同.请回答下列问题:
已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物在常温下均呈气态,在周期表中Z与W左右相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的最外层电子数相同.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com