
【题目】写出下列物质在水溶液中的电离方程式:
(1)HClO___________________________________________________
(2)Ba(NO3)2______________________________________________
A层:(3)NaHSO4____________________________________________
NH3·H2O_____________________________________________________
B层:(3)H2CO3______________________________________________
Fe(OH)3____________________________________________________
【答案】HClO![]() H++ClO- Ba(NO3)2=Ba2++2NO3- NaHSO4=Na++H++SO42- NH3·H2O
H++ClO- Ba(NO3)2=Ba2++2NO3- NaHSO4=Na++H++SO42- NH3·H2O![]() NH+4+OH- H2CO3
NH+4+OH- H2CO3![]() H++HCO3- HCO3-
H++HCO3- HCO3-![]() H++CO32- Fe(OH)3
H++CO32- Fe(OH)3![]() Fe3++3OH-
Fe3++3OH-
【解析】
用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式,离子所带电荷数一般可根据它们在化合物中的化合价来判断,所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等,书写电离方程式时要先判断是强弱电解质,强电解质用“=”,而弱电解质用“![]() ”,据此分析判断。
”,据此分析判断。
(1)HClO为弱电解质,其电离方程式为:HClO![]() H++ClO-,
H++ClO-,
故答案为:HClO![]() H++ClO-;
H++ClO-;
(2)Ba(NO3)2为强电解质,其电离方程式为:Ba(NO3)2=Ba2++2NO3-,
故答案为:Ba(NO3)2=Ba2++2NO3-;
A层:(3)NaHSO4为强电解质,其电离方程式为:NaHSO4=Na++H++SO42-,
故答案为:NaHSO4=Na++H++SO42-;
(4)NH3·H2O为弱电解质,其电离方程式为:NH3·H2O![]() NH+4+OH-,
NH+4+OH-,
故答案为:NH3·H2O![]() NH+4+OH-;
NH+4+OH-;
B层:(3)H2CO3为二元弱酸其电离方程式分两步进行,分别为:H2CO3![]() H++HCO3-,HCO3-
H++HCO3-,HCO3-![]() H++CO32-,
H++CO32-,
故答案为:H2CO3![]() H++HCO3-,HCO3-
H++HCO3-,HCO3-![]() H++CO32-;
H++CO32-;
(4)Fe(OH)3为弱电解质,其电离方程式为:Fe(OH)3![]() Fe3++3OH-,
Fe3++3OH-,
故答案为:Fe(OH)3![]() Fe3++3OH-。
Fe3++3OH-。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效消毒剂,可用如下反应制得:2NaClO3+Na2SO3+H2SO4![]() 2ClO2↑+2Na2SO4+H2O,下列说法正确的是( )
2ClO2↑+2Na2SO4+H2O,下列说法正确的是( )
A. 该反应属于复分解反应
B. NaClO3被还原,发生还原反应
C. 反应中Na2SO3作氧化剂
D. 生成6.75 g ClO2时,转移0.2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3 +4NaOH +3NaClO=2Na2FeO4+3NaCl +5H2O
(1)用单线桥在方程式中标出电子转移的情况:___;
(2)Na2FeO4中铁元素的化合价是___价,Na2FeO4具有较强的___(填“氧化性”或“还原性”)
(3)实验室欲配制250mL0.1 molL-1NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器为____,下列操作配制的溶液浓度偏低的是___;
A.称量NaOH时,将NaOH放在纸上称重
B.配制前,容量瓶中有少量蒸馏水
C.配制时,NaOH未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线
(4)在容量瓶的使用方法中,下列操作正确的是___。
A.容量瓶用水洗净后,再用待配溶液洗涤
B.使用容量瓶前检验是否漏水
C.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线下1~2cm处,用胶头滴管加蒸馏水至刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从废旧锂离子二次电池(主要成分为![]() ,还含有少量石墨和金属钢売、铝箔等杂质)中回收钴和锂的工艺流程如下:回答下列问题:
,还含有少量石墨和金属钢売、铝箔等杂质)中回收钴和锂的工艺流程如下:回答下列问题:

(1)![]() 的电子式为__________。“碱浸”的目的是____________。
的电子式为__________。“碱浸”的目的是____________。
(2)“酸浸”过程中![]() 发生反应的离子方程式为______________,浸渣中含有的主要成分是_______________________。
发生反应的离子方程式为______________,浸渣中含有的主要成分是_______________________。
(3)“萃取净化”除去的杂质离子除![]() 外,还有________(填离子符号)
外,还有________(填离子符号)
(4)“苯取分离“中钴、锂的萃取率与平衡时溶液![]() 的关系如图所示,
的关系如图所示,![]() 一般选择5左右,理由是_____________________________________。
一般选择5左右,理由是_____________________________________。

(5)“沉锂“中![]() 的溶解度随温度变化的曲线如图所示:
的溶解度随温度变化的曲线如图所示:
①根据平衡原理分析![]() 在水中的溶解度随温度变化的原因______________。
在水中的溶解度随温度变化的原因______________。
②为获得高纯![]() ,提纯操作依次为热过滤、_______、烘干。
,提纯操作依次为热过滤、_______、烘干。
③若“沉锂”中![]() ,加入等体积等浓度
,加入等体积等浓度![]() 溶液,则此时沉锂率为________________。(已知
溶液,则此时沉锂率为________________。(已知![]() 的
的![]() 为
为![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3),主要用作半导体硅的掺杂源或有机合成催化剂,还用于高纯硼或有机硼的制取。某兴趣小组用氯气和硼为原料,采用下列装置(部分装置可重复使用)制备BCl3。

已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸;②2B+6HCl ![]() 2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
请回答下列问题:
(1)A装置可用氯酸钾固体与浓盐酸反应制氯气,反应的化学方程式为___________。
(2)装置从左到右的接口连接顺序为a→___________________→j。
(3)装里E中的试剂为___________,如果拆去E装置,可能的后果是____________。
(4)D装置中发生反应前先通入一段时间的氯气,排尽装置中的空气。若缺少此步骤,则造成的结果是_____。
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式________,硼酸也可用电渗析法制备,“四室电渗析法”工作原理如图所示:

则阳极的电极反应式__________________,分析产品室可得到H3BO3的原因________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列6种物质
①![]() ②
②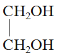 ③
③![]()
④CH3-CH=CH-CH3 ⑤![]() ⑥
⑥![]()
(1)用于制造炸药TNT的是____(填序号)。
(2)具有两性的是______(填序号)。
(3)有机物①的沸点比②______(填“高”或“低”)
(4)有机物④的名称是___________
(5)有机物④形成的高聚物结构简式为__________________
(6)检验有机物⑥中官能团的试剂是_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,电流表指针发生偏转,同时A极质量减少,B极上有气泡产生,C为电解质溶液,

下列说法错误的是
A. B极为原电池的正极
B. A、B、C可能分别为Zn、Cu、稀盐酸
C. C中阳离子向A极移动
D. A极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“点击化学”是指快速、高效连接分子的一类反应,例如铜催化的Huisgen环加成反应:

我国科研人员利用该反应设计、合成了具有特殊结构的聚合物F并研究其水解反应。合成线路如下图所示:

已知:
![]()
(1)①的反应类型是___________,化合物  的官能团的名称为_____________。
的官能团的名称为_____________。
(2)关于B和C,下列说法不正确的是____________(填字母序号)。
a.利用红外光谱法可以鉴别B和C b.B可以发生氧化、取代、消去反应
c.可用溴水检验C中含有碳碳三键
(3)B生成C的过程中还有另一种生成物X,分子式为C3H6O,核磁共振氢谱显示只有一组峰,X的结构简式为______________________。
(4)D生成E的化学方程式为___________________________________________________。
(5)有机物M是有机物C的同系物,其相对分子质量比C大14,写出一种满足下列条件的M的同分异构体N的结构简式是________________________。
a.除苯环外,不含其它的环状结构,不考虑立体异构;
b.能与FeC13溶液发生显色反应;
c.1mol N最多与6mol Br2(浓溴水)反应。
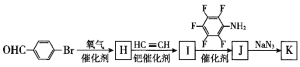
(6)为了探究连接基团对聚合反应的影响,设计了单体K( ) 其合成路线如下,写出H、J的结构简式:H____________、J_______________。
) 其合成路线如下,写出H、J的结构简式:H____________、J_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素存在于黑香豆、香蛇鞭菊、野香荚兰、兰花中,具有新鲜干草香和香豆香,是一种口服抗凝药物。实验室合成香豆素的反应和实验装置如下:

可能用到的有关性质如下:
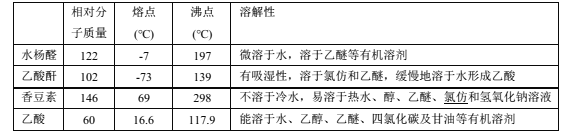
合成反应:
向三颈烧瓶中加入95%的水杨醛38.5g、新蒸过的乙酸酐73g和1g无水乙酸 钾,然后加热升温,三颈烧瓶内温度控制在145~150℃,控制好蒸汽温度。此时,乙酸开始蒸出。当蒸出量约15g时,开始滴加15g乙酸酐,其滴加速度应与乙酸蒸出的速度相当。乙酸酐滴加完毕后,隔一定时间,发现气温不易控制在120℃时,可继续提高内温至208℃左右,并维持15min至半小时,然后自然冷却。
分离提纯:
当温度冷却至80℃左右时,在搅拌下用热水洗涤,静置分出水层,油层用10%的 碳酸钠溶液进行中和,呈微碱性,再用热水洗涤至中性,除去水层,将油层进行减压蒸馏,收集150~160℃/1866Pa馏分为粗产物。将粗产物用95%乙醇(乙醇与粗产物的质量比为1:1)进行重结晶,得到香豆素纯品35.0g。
(1)装置a的名称是_________。
(2)乙酸酐过量的目的是___________。
(3)分水器的作用是________。
(4)使用油浴加热的优点是________。
(5)合成反应中,蒸汽温度的最佳范围是_____(填正确答案标号)。
a.100~110℃ b.117.9~127.9℃ c.139~149℃
(6)判断反应基本完全的现象是___________。
(7)油层用10%的碳酸钠溶液进行中和时主要反应的离子方程式为______。
(8)减压蒸馏时,应该选用下图中的冷凝管是_____(填正确答案标号)。
a.直形冷凝管 b.球形冷凝管
b.球形冷凝管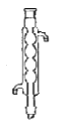 c.蛇形冷凝管
c.蛇形冷凝管
(9)本实验所得到的香豆素产率是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com