
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题。

(1)第三周期元素中非金属性最强的元素的原子结构示意图是___。
(2)②③⑦最高价氧化物对应水化物的酸性由强到弱的顺序是___(填化学式)。
(3)下列可以判断⑤和⑥金属性强弱的是___(填序号)。
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
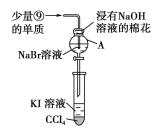
①仪器A的名称是___,A中发生反应的离子方程式是___。
②棉花中浸有NaOH溶液的作用是___(用离子方程式表示)。
③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到___。该实验必须控制⑨单质的加入量,否则得不出溴的非金属性比碘强的结论。理由是___。
④第ⅦA族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐_____(填“增大”或“减小”),得电子能力逐渐减弱。
【答案】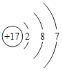 HNO3>H2CO3>H2SiO3 cd 分液漏斗 2Br-+Cl2=Br2+2Cl- Cl2+2OH-=H2O+Cl-+ClO- 溶液分层,下层液体为紫红色 氯气能够氧化溴离子和碘离子,氯气必须少量,否则干扰检验结果 增大
HNO3>H2CO3>H2SiO3 cd 分液漏斗 2Br-+Cl2=Br2+2Cl- Cl2+2OH-=H2O+Cl-+ClO- 溶液分层,下层液体为紫红色 氯气能够氧化溴离子和碘离子,氯气必须少量,否则干扰检验结果 增大
【解析】
由元素在周期表的位置可知,元素①~⑨分别为H、C、N、O、Na、Al、Si、S、Cl,结合元素周期律和物质的性质分析解答。
(1)第三周期元素中非金属性最强的元素是Cl,其原子结构示意图是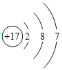 ;
;
(2)元素非金属性越强,其最高价氧化物对应水化物的酸性越强,则②③⑦最高价氧化物对应水化物的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3;
(3)a.根据单质的熔点不能判断金属性强弱,故a错误;
b.化合价高低不能作为比较金属性的依据,故b错误;
c.Na与水反应比Al剧烈,说明金属性:Na>Al,可以比较,故c正确;
d.元素的金属性越强,最高价氧化物对应水化物的碱性越强,可以比较,故d正确;
答案选cd;
(4)①A为分液漏斗,A中发生氯气与NaBr的氧化还原反应,离子方程式为2Br-+Cl2=Br2+2Cl-;
②NaOH溶液用于吸收氯气,离子方程为Cl2+2OH-=H2O+Cl-+ClO-;
③溴与KI反应生成碘单质,碘单质易溶于四氯化碳。将A中液体滴入试管内,充分振荡、静置,可观察到溶液分层,下层呈紫色;若通入过量氯气,剩余的氯气能够进入试管先于Br2氧化碘离子,干扰溴与碘离子的反应,所以氯气必须少量,否则干扰检验结果;
④同主族元素从上到下,原子核外电子层数增加,原子半径增大,故得到电子能力减弱。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】某实验小组在T1温度下,容积为1 L的恒容密闭容器中,同时通入0.1 mol CO(g)和0.1 mol H2O(g),发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=a kJ· mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
CO2(g)+H2(g) △H=a kJ· mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
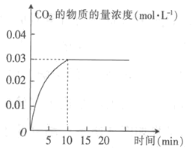
(1)0~10min内,CO的平均反应速率为_______________。
(2)T1温度下,该反应的平衡常数K为________(用分数表示)。
(3)①已知:
I.H2的燃烧热△H=-285.8 kJ· mol-1;
II.CO的燃烧热△H=-283 kJ· mol-1;
III.H2O(g)=H2O(l) △H=-44 kJ· mol-1。
则a=_______。
②反应达到平衡后,下列措施能使平衡向正反应方向移动的是__________(填字母)。
A 升高温度 B 增大压强 C 通入H2O(g) D 移走CO2(g)
(4)T1温度下,某时刻另一实验小组测得反应容器中有关数据为c(CO)=0.6 mol·L-1、c(H2O)=1.6 mol·L-1,c(H2)=0.4 mol·L-1,c(CO2)=0.4 mol·L-1,则该反应在下-时刻将____(填“向正反应方向进行”“向逆反应方向进行”或“达到平衡”),判断依据是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物 A 的相对分子质量为 62。为进一步测定 A 的化学式,现取 6.2 g A 完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重5.4 g 和 8.8 g(假设每步反应完全)。
(1)该有机物的实验式是_____;分子式是_____。
(2)红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有 2 个吸收峰且峰面积之比为 1∶2,推断该有机物的结构简式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d四种短周期元素在周期表中的位置如图所示,a和b分别位于周期表的第2列和第13列,下列叙述正确的( )
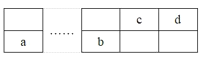
A.离子半径b>d
B.b可以和强碱溶液发生反应
C.c的最简单氢化物的稳定性强于d的
D.a的最高价氧化物对应水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2.0 L的密闭容器内,物质D在T ℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是

A. 从反应开始到第一次达到平衡时,A物质的平均反应速率为0.0667 mol/(L·min)
B. 该反应的化学方程式为2D(s) 2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B)
C. 已知:反应的H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
D. 若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的框架图,请回答下列问题:
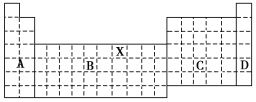
(1)写出元素X在周期表中位置___。
(2)若将此元素周期表分为A、B、C、D区,其中全部是金属元素的区域为___区。
(3)所含元素最多的周期是___,所含元素最多的族是___。
(4)硬度最大的单质是____,密度最小的金属是____。(用物质的名称填写)
(5)在原子序数为1~18号元素中,请用化学式填写。
与水反应最剧烈的金属元素是___;与酸、碱都反应的金属是___;最高价氧化物对应水化物酸性最强的酸是___;原子半径最大的金属与原子半径最小的非金属形成的化合物是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1 的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线②代表滴定CH3COOH溶液的曲线
B. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1
C. 在相同温度下,A、B、C三点溶液中水的电离程度: A<C<B
D. D点溶液中:c(Cl-)+ 2c(H+)=2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要用质量分数为98%、密度为1.84g/cm3的浓硫酸配制1.0 mol·L-1的稀硫酸溶液450mL,请回答下列问题
(1)需要用量筒量取的浓硫酸的体积为__________mL。
(2)下面操作造成所配稀硫酸溶液浓度(填“偏高”、“偏低”或“无影响”)
①用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶__________。
②向容量瓶加水定容时眼睛俯视液面__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目。____________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______,MnO![]() +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com