
【题目】某学习小组利用反应:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O H2C2O4来探究“外界条件对化学反应速率的影响”。实验时,先分别量取KMnO4酸性溶液、H2C2O4溶液,然后倒入大试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
(1)该反应是溶液之间发生的不可逆反应,改变压强对其反应速率的影响是______(填序号)。
A.可能明显加快 B.可能明显减慢 C.几乎无影响,可以忽略
(2)甲同学设计了如下实验
实验编号 | H2C2O4溶液 | KMnO4溶液 | 温度/℃ | ||
浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积(mL) | ||
a | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
B | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
c | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
①探究温度对化学反应速率影响的组合实验编号是__________,可探究温度对化学反应速率影响的实验编号是__________。
②实验a测得混合后溶液褪色的时间为40%,忽略混合前后 体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=______。
(3)在其它条件相同的情况下,乙同学用不同浓度的KMnO4酸性溶液实验,测得实验数据如下表所示:
实验编号 | 温度℃ | H2C2O4溶液 | KMnO4酸性溶液 | 褪色的时间(min) | ||
浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积(mL) | |||
1 | 25 | 0.10 | 4 | 0.2 | 8 | t1 |
2 | 25 | 0.010 | 4 | 0.2 | 8 | t2(t2<t3) |
依据表中数据,_____(填“能”或“不能”)得出“溶液褪色所需时间越短,反应速率越快”的结论,理由是__________________。
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO42-该反应有催化作用
丙同学认为假设3不合理,其理由是__________。
②丁同学用如下实验证明假设2成立:在A和B两支试管中分别加入4mL0.2mol·L-1草酸溶液,再在A试管中加入lmL0.1mol·L-1MnSO4溶液、B试管中加入1mL蒸馏水,然后在两支试管中同时分别加入1mLO.1mol·L-1KMnO4酸性溶液,A试管溶液褪色的时间明显早于B试管。在B试管中加入1mL蒸馏水的目的是:__。
③同学们认为不宜用MnCl2溶液代替MnSO4溶液对该反应进行催化探究,其原因是(用离子方程式表示)_______________。
【答案】Ca和bb和c0.000167 mol·L-1·s-1(不能两组实验中,高锰酸钾的浓度、用量不等,浓度大则反应快,但用量大则导致溶液褪色需更长时间K+、SO42-未参与该离子反应控制变量,使两个实验中草酸、高锰酸钾的浓度彼此相同2MnO4-+10Cl-+16H+ = 2Mn2+ + 5Cl2↑+8H2O
【解析】
(1)虽然产物中有CO2气体,改变压强时会改变CO2浓度,但反应不可逆,不存在影响逆反应速率的问题,故改变CO2浓度对正反应速率无影响,答案为C;
(2)①探究外因对速率的影响,通常只改变一个变量,而其它条件相同,则a和b是在相同温度下探究浓度对速率的影响,b和c是在浓度相同的情况下,探究温度对速率的影响;
②实验a测得混合后溶液褪色的时间为40s,忽略混合前后 体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=(0.010mol/L×![]() )÷40s= 0.000167 mol·L-1·s-1;
)÷40s= 0.000167 mol·L-1·s-1;
(3) 两组实验中,高锰酸钾的浓度、用量不等,浓度大则反应快,但用量大则导致溶液褪色需更长时间,故依据表中数据不能得出“溶液褪色所需时间越短,反应速率越快”的结论;
(4)①将反应5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O改写为离子方程式为5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O;可知K+、SO42-未参与该离子反应,故假设3不合理;
②丁同学向B试管中加入1mL蒸馏水是为了控制变量,使两个实验中草酸、高锰酸钾的浓度彼此相同;
③因为酸性条件下KMnO4能氧化溶液中的Cl-,发生反应的离子方程式为2MnO4-+10Cl-+16H+ = 2Mn2+ + 5Cl2↑+8H2O。


科目:高中化学 来源: 题型:
【题目】汽车尾气中的主要污染物是NO、NO2和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
[研究一]用NaOH溶液吸收NO、NO2,
⑴当n(NO)﹕n(NO2)=1时只生成一种盐,这种盐的化学式为__________
⑵当只有NO2时,生成两种盐:2NO2+2NaOH=NaNO2+NaNO3+H2O。若NaOH溶液恰好完全吸收NO2后溶液显碱性,该溶液中离子浓度由大到小的顺序是:___________。
[研究二]一定条件将CO和NO转化为无污染产物:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H
2CO2(g)+N2(g) △H
⑶已知:2C(s)+O2(g)=2CO(g);△H1=-221.0KJ/mol
C(s)+O2(g)=CO2(g);△H2=-393.5KJ/mol
N2(g)+O2(g)=2NO(g);△H3=+180.5KJ/mol。
则△H=______
⑷T℃下,在固定容积的密闭容器中,通入一定量NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) 104 mol/L | 10.0 | 4.50 | 2.00 | 1.50 | 1.00 | 1.00 |
c(CO) 103 mol/L | 3.60 | 3.05 | 2.80 | 2.75 | 2.70 | 2.70 |
①该条件下,2s内N2的平均反应速率v(N2)=_____________
②若往容器中加入一定量生石灰,CO平衡转化率_____(选填“增大”、“减小”或“不变”)
③其它条件不变,只适当升高温度,则4s时,c(NO)=c1mol/L,则c1可能是_______
a.1.10×10﹣3 b.1.25×10﹣4 c.1.00×10﹣4 d.9.00×10﹣5
【研究三】测定汽车尾气中CO的含量
⑸用CO分析仪测定:该分析仪的工作原理类似于燃料电池,其中电解质是能传导O2﹣的Y2O3和ZrO2晶体,负极的电极反应式为____________。
⑹用五氧化二碘(I2O5)固体氧化定量检测:I2O5+5CO=I2+5CO2
抽取10L汽车尾气,用足量I2O5吸收,然后配成100mL溶液,量取其中的20.00mL溶液,用0.0050mol/LNa2S2O3溶液滴定,三次平行实验平均消耗Na2S2O3溶液的体积为20.0mL,已知:2Na2S2O3+I2=Na2S4O6+2NaI,则尾气中c(CO)=___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重水(D2O)是重要的核工业原料,下列说法错误的是( )
A. 氘(D)原子核外有1个电子 B. 1H与D互称同位素
C. H2O与D2O互称同素异形体 D. 1H218O与D216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为短周期元素,这些元素原子的最外层电子数分别是1、4、6,则由这三种元素组成的化合物的化学式不可能是()
A. XYZ B. X2YZ C. X2YZ2 D. X2YZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用溴和苯在FeBr3催化下制取溴苯,得到粗溴苯后,要用如下操作提纯:
①蒸馏;②水洗;③用干燥剂干燥;④用10%的NaOH溶液洗涤。正确的操作顺序是
A. ②④②③① B. ④②③① C. ④①②③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为:r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法不正确的是
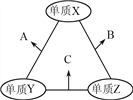
A. X元素位于ⅥA族
B. A难溶于B中
C. A和C不可能发生氧化还原反应
D. B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律分析,下列推断中正确的是( )
A. 铍原子失去电子能力比镁强 B. 砹的氢化物能够稳定存在
C. 硒化氢比硫化氢稳定 D. 氢氧化锶比氢氧化钙的碱性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com