
【题目】下列各项不属于官能团的是( )
A.NO3-B.-ClC.-CHOD.-NO2
科目:高中化学 来源: 题型:
【题目】(1)MgCl2固体中含离子总数为1.806×1024个,将其配成2000mL溶液,求:
①c(MgCl2)=_____。
②c(Cl-)=____。
(2)配制500mL含Fe3+56g的Fe2(SO4)3溶液,需要6.25mol/L的Fe2(SO4)3溶液的体积为___mL。
(3)______mL 2 mol/L的NaOH溶液中所含溶质的质量和200mL 1 mol/L的Na2SO4溶液所含溶质的质量相等。
(4)11.7克NaCl配制成100mL溶液,此溶液中c(Cl-)与标准状况下44.8升HCl配成V L溶液中的c(Cl-)相等,求V=______。
(5)含34.2g Al2(SO4)3的溶液,其体积与0.5mol/L含Na2SO4质量为142g的溶液体积相同。求该Al2(SO4)3溶液中c(SO42-)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知723 K时,2SO2(g)+O2(g)![]() 2SO3(g)ΔH=﹣QkJ·
2SO3(g)ΔH=﹣QkJ·![]() ,在相同条件下,向一密闭容器中通入2mol SO2和1 mol O2,达到平衡时放出的热量为Q1kJ;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2kJ.则Q1、Q2、Q满足的关系是( )
,在相同条件下,向一密闭容器中通入2mol SO2和1 mol O2,达到平衡时放出的热量为Q1kJ;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2kJ.则Q1、Q2、Q满足的关系是( )
A. Q2=![]() B. Q2>
B. Q2>![]() C. Q2<Q1<Q D. Q=Q1>Q2
C. Q2<Q1<Q D. Q=Q1>Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程不属于水解反应的是( )
A. 吃馒头时,经咀嚼后有甜味
B. 淀粉溶液与稀硫酸共热一段时间后,滴加碘水不显蓝色
C. 不慎将浓硝酸沾到皮肤上会出现黄色斑痕
D. 油脂与氢氧化钠溶液共热可以制得肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】手持技术的氧电化学传感器可用于测定O2含量.下图为某种氧电化学传感器的原理示意图,已知在测定O2含量过程中,电解质溶液的质量保持不变。一定时间内,若通过传感器的待测气体为a L(标准准状况),某电极增重了bg。下列说法正确的是
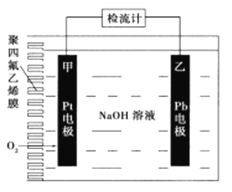
A. Pt上发生氧化反应 B. Pb上的电极反应式为4OH--4e-=O2↑+2H2O
C. 反应过程中转移OH-的物质的量为0.25bmol D. 待测气体中氧气的体积分数为0.7b/a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2O的摩尔质量是18g
B.1mol氧的质量是16g
C.氧气的摩尔质量是32gmol﹣1
D.2molH2的摩尔质量是4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合氯化铝是一种新型净水剂,其中铝的总浓度(用c表示)包括三类:主要为Al3+中的单体形态铝(用Ala表示)总浓度,主要为 [AlO4Al12(OH)24(H2O)12]7+的中等聚合形态铝总浓度(用Alb表示)和Al(OH)3胶体形态铝(用Alc表示)总浓度。
(1)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g) ΔH1=akJ·mol-1
②6AlCl(g)=4Al(s)+2AlCl3(g) ΔH2=bkJ·mol-1
则反应Al2O3(s) +3C(s)=2Al (s)+3CO(g) 说明ΔH=_______kJ·mol-1(用含a、b的代数式表示)。
_0( 填“>”或“<”)。
反应①在常压、1900℃的高温下才能进行,说明ΔH_______0(填“>”、“<”或“=”)
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝溶液中铝形态分布(百分数)如右表:
AlT/(mol·L-1) | Ala/% | Alb/% | A1c/% |
0.208 | 1.4 | 86.6 | 12.0 |
0.489 | 2.3 | 86.2 | 11.5 |
0.884 | 2.3 | 88.1 | 9.6 |
1.613 | 3.1 | 87.0 | 9.9 |
2.520 | 4.5 | 88.2 | 7.3 |
①在一定温度下,AlT越大,Al(OH)3胶体的百分含量________(填“越大”“越小”或“不变”)。
②若将c=2.520mol/L的聚合氧化铝溶液加水稀释,则稀释过程中发生的主要反应的离子方程式为_________________________________。
(3)一定条件下,向1.0mol/L的AlCl溶液中加入0.6mol/L的NaOH溶液,可制得Alb含量约为86% 的聚合氯化铝溶液。写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:_________________________。
(4)已知Al3++4X![]() 2
2![]() ,X表示显色剂,
,X表示显色剂,![]() 表示有色物质,通过比色分析得
表示有色物质,通过比色分析得
到25 ℃时Al3+浓度随时间的变化关系如图所示(初始时X的浓度为0.194 mol·L-1)。
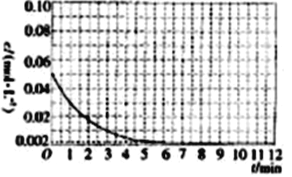
①1min时, ![]() 的浓度为___________。
的浓度为___________。
②0~3min内该反应的速率vx=________。
③第9min时,反应达到平衡,K=__________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用3.7 mol/L的硫酸与锌粒制取氢气,要加快该反应的速率,采取措施错误的是
A.加入2 mol/L的硫酸B.加入少量CuSO4
C.适当加热D.加入NaHSO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒压下,在一个容积可变的容器中发生如下反应:A(g)+B(g)![]() C(g)。
C(g)。
(1)若开始时放入1 mol A和1 mol B,达到平衡后,生成amol C。这时A的物质的量为________mol。
(2)若开始时放入3 mol A和3 mol B,达到平衡后,生成C的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com