
【题目】已知723 K时,2SO2(g)+O2(g)![]() 2SO3(g)ΔH=﹣QkJ·
2SO3(g)ΔH=﹣QkJ·![]() ,在相同条件下,向一密闭容器中通入2mol SO2和1 mol O2,达到平衡时放出的热量为Q1kJ;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2kJ.则Q1、Q2、Q满足的关系是( )
,在相同条件下,向一密闭容器中通入2mol SO2和1 mol O2,达到平衡时放出的热量为Q1kJ;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2kJ.则Q1、Q2、Q满足的关系是( )
A. Q2=![]() B. Q2>
B. Q2>![]() C. Q2<Q1<Q D. Q=Q1>Q2
C. Q2<Q1<Q D. Q=Q1>Q2
科目:高中化学 来源: 题型:
【题目】反应CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g) △H<0,达到平衡时,下列说法正确的是
CO(NH2)2(s)+H2O(g) △H<0,达到平衡时,下列说法正确的是
A. 加入催化剂,平衡常数不变
B. 减小容器体积,正反应速率增大、逆反应速率减小
C. 增大CO(NH2)2的量, CO2的转化率减小
D. 降低温度,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示构成细胞的元素、化合物,a、b、c、d代表不同的小分子物质,A、B、C代表不同的大分子物质,据图分析不正确的是( )

A. 若物质A是动、植物细胞中均含有的储能物质,则A是脂肪
B. 物质b是氨基酸,若某种B分子由n个b分子(平均相对分子质量为m)组成的2条链组成,则该B分子的相对分子质量大约为mn﹣18(n﹣2)
C. 物质c在人体细胞中共有5种,分子中的含氮碱基不同决定了c的种类不同
D. 物质d是性激素,d和胆固醇、维生素D都属于固醇类物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位.请回答下列问题:

(1)图中X是________,Ⅰ在植物细胞中主要是指___________。
(2)与Ⅳ相比,Ⅱ特有的元素是_____。
(3)鉴定Ⅳ使用_______试剂,反应呈现______色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.6gH2O的物质的量是_______mol,含有_________ 个H2O。
(2)标准状况下,11.2L的H2S气体质量为17g,则H2S的摩尔质量是_________;等物质的量的NH3与H2S质量比为___________,1.7g氨气与________mol H2O含有的电子数相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学依据资料深入探究Fe3+在水溶液中的行为。
资料:
ⅰ.Fe3+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;[Fe(H2O)6]3+发生如下水解反应:
[Fe(H2O)6]3+(几乎无色)+nH2O![]() [Fe(H2O)6-n(OH)n]3-n(黄色)+nH3O+(n=0~6);
[Fe(H2O)6-n(OH)n]3-n(黄色)+nH3O+(n=0~6);
ⅱ.[FeCl4(H2O)2]-为黄色。
进行实验:
【实验Ⅰ】
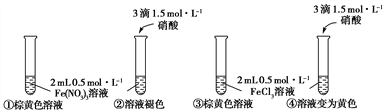
【实验Ⅱ】
分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。
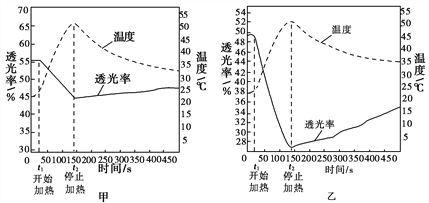
Fe(NO3)3溶液透光率随温度变化曲线 FeCl3溶液透光率随温度变化曲线
(1)实验Ⅰ中,试管②溶液褪色的原因是_________________________________________。
(2)实验Ⅰ中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是_____________________________________________________________________________。
(3)由实验Ⅱ图甲、乙可知:加热时,溶液颜色________(填“变浅”“变深”或“不变”)。
(4)由实验Ⅱ,可以得出如下结论:
【结论一】FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O![]() [Fe(H2O)6]3++4Cl-得出此结论的理由是_______________________________________________________。
[Fe(H2O)6]3++4Cl-得出此结论的理由是_______________________________________________________。
【结论二】结论一中反应的ΔH________(填“>0”或“<0”)。
(5)实验小组同学重新设计了一个实验证明(4)中结论一。实验方案:取试管①中溶液,_______________________(请描述必要的实验操作和现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某兴趣小组设计用铁粉将NO还原为N2(同时生成FeO)。

已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO2,不吸收NO。
(1)装置A中反应的离子方程式是_________________________________________。
(2)装置的连接顺序为:a→()→()→()→()→()→()→()→()→d
Ⅱ.已知:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,易水解产生大量白雾;易分解:SO2Cl2=SO2↑+Cl2↑,催化合成硫酰氯的实验装置如下图(夹持装置已省略)
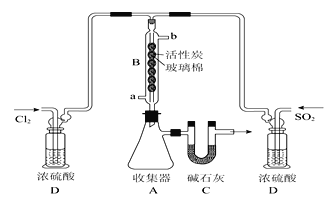
回答下列问题:
(3)仪器B的名称是____________仪器B冷却水的进口为_______(填“a”或“b”)活性炭的作用是_______________________。
(4)装置D除干燥气体外,另一个作用是__________________。若缺少D,则硫酰氯会水解,该反应的化学方程式是_________________________________。
(5)C装置的作用是________________。为了防止硫酰氯分解,某同学建议将收集器A放在__________中冷却。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com