
【题目】求25℃时以下溶液的pH
(1)pH=3的盐酸与pH=5的硫酸等体积混合后,pH=
(2)pH=10和pH=12的两种NaOH溶液等体积混合后,pH=
(3)pH=9的NaOH溶液稀释到原来的10倍后,pH= , 再稀释到原来的1000倍后,pH .
(4)pH=12的NaOH和pH=4的HCl等体积混合后,pH= .
【答案】
(1)3.3
(2)11.7
(3)8;≈7
(4)11.7
【解析】解:(1)设两种酸的体积都是1L,pH=3的盐酸与pH=5的硫酸等体积混合后,混合溶液中氢离子浓度= ![]() =5.05×10﹣4 mol/L,则混合溶液的pH=﹣lg5.05×10﹣4=3.3, 所以答案是:3.3;(2)设两种碱的体积都是1L,pH=10和pH=12的两种NaOH溶液等体积混合后,混合溶液中氢氧根离子浓度=
=5.05×10﹣4 mol/L,则混合溶液的pH=﹣lg5.05×10﹣4=3.3, 所以答案是:3.3;(2)设两种碱的体积都是1L,pH=10和pH=12的两种NaOH溶液等体积混合后,混合溶液中氢氧根离子浓度= ![]() mol/L=5.05×10﹣3 mol/L,则混合溶液中氢离子浓度=
mol/L=5.05×10﹣3 mol/L,则混合溶液中氢离子浓度= ![]() mol/L=2×10﹣12mol/L,pH=11.7,
mol/L=2×10﹣12mol/L,pH=11.7,
所以答案是:11.7;(3)强碱溶液稀释10倍是溶液的pH减小1,所以pH=9的NaOH溶液稀释到原来的10倍后,pH=8,再稀释到原来的1000倍后,溶液接近中性,则pH≈7,所以答案是:8;≈7;(4)pH=12的NaOH溶液中氢氧根浓度为0.01mol/L,pH=4的HCl中氢离子浓度为10﹣4mol/L,等体积混合后,碱过量,混合后溶液中氢氧根的浓度c(OH﹣)= ![]() =4.95×10﹣3mol/L,故氢离子浓度c(H+)=
=4.95×10﹣3mol/L,故氢离子浓度c(H+)= ![]() ≈2×10﹣11mol/L,故pH=11.7,所以答案是:11.7.
≈2×10﹣11mol/L,故pH=11.7,所以答案是:11.7.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10﹣羟基喜树碱的结构如图所示,下列关于10﹣羟基喜树碱的说法正确的是( ) 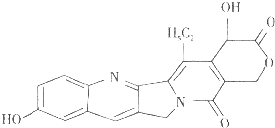
A.分子式为C20H17N2O5
B.该物质可发生消去反应
C.1mol该物质可与9molH2发生加成反应
D.1mol该物质可分别消耗Na、NaOH,Na2CO3的物质的量之比为2:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将碘水中的碘萃取出来的实验中,下列说法错误的是 ( )
A. 分液漏斗使用前要检验它是否漏水
B. 萃取剂要求不溶于水,且比水更容易使碘溶解
C. 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液
D. 若用苯作萃取剂,则分层后上层液体呈紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究.
(1)提出假设 ①该反应的气体产物是CO2 .
②该反应的气体产物是CO.
③该反应的气体产物是 .
(2)设计方案如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
查阅资料
氮气不与碳、氧化铁发生反应.实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气.请写出该反应的离子方程式: .
(3)实验步骤①按图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气.冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g.
步骤②、④中都分别通入N2 , 其作用分别为 .
(4)数据处理试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: .
(5)实验优化 学习小组有同学认为应对实验装置进一步完善.①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 .
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是 ( )
A. 酸性氧化物一定是非金属氧化物 B. 碱性氧化物一定是金属氧化物
C. SO2 溶于水能导电所以SO2 是电解质 D. Na2O是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能用胶体的知识解释的现象是( )
A. 向FeCl3溶液中加入NaOH溶液,出现红褐色沉淀
B. 石膏点豆腐
C. 一支钢笔使用两种不同牌号的墨水,易出现堵塞
D. 江河入海处,易形成沙洲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的相对分子质量184.5,其结构如图1所示,(﹣R﹣代表某种烷基),A在一定条件下还有如图2所示的反应关系,D不能发生银镜反应.
(1)C中含有的官能团为 , E→F的反应类型为;
(2)写出A的结构简式;
(3)写出C→E的化学方程式;
(4)H的同分异构体很多,其中属于酯类,含苯环,且水解产物中含有乙酸的同分异构体有种
(5)G显酸性,M(B),M(G)分别表示B、G的相对分子质量,试求:M(G)﹣M(B)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X,Y,Z三种气体的起始浓度和平衡浓度如表,下列说法错误的是( )
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,平衡常数为1600
C.其他条件不变时,增大压强可使平衡常数增大
D.改变温度可以改变该反应的平衡常数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com