
【题目】下列各装置不能达到实验目的是
A.利用①吸收多余的氨气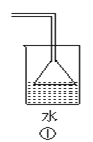
B.装置②可用于除去Cl2中的HCl
C.装置③可用于干燥氨气
D.装置④可用于排空气法收集H2、CO2、Cl2、HCl等气体
【答案】B
【解析】
A.根据氨气极易溶于水,尾气吸收时要防止倒吸;
B.根据氯气和氯化氢的性质分析判断,除杂的原则是:除去杂质不引进新的杂质,除杂剂和收集物质不反应;
C.根据氨气和碱石灰的性质判断,碱性干燥剂能干燥碱性气体;
D.根据气体的密度判断收集方法。
A.氨气极易溶于水,吸收装置中的导管下连漏斗,漏斗的边缘紧靠液面,易吸收易溶性气体,且能防止倒吸,A正确;
B. Cl2、HCl都能和氢氧化钠反应而被除去,最终得不到氯气,所以装置②不能用于除去Cl2中的HCl,B错误;
C.碱石灰是碱性物质,和氨气不反应,所以碱石灰能干燥氨气,C正确;
D. H2的密度小于空气,无条件时,和空气中的成分不反应,所以可用向下排空气法收集;CO2、Cl2、HCl气体的密度大于空气的密度,可采用向上排空气法收集,由于Cl2、HCl能污染环境,需有尾气处理装置配合,故装置短导管进气时适合收集氢气,长导管进气适合收集CO2、Cl2、HCl,D正确;
故合理选项是B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】金属钛在航天、潜海和医疗方面应用广泛。以钛铁矿[主要成分为钛酸亚铁(FeTiO3),含少量Fe2O3]为原料制备钛的工艺流程如图所示。

(1)步骤②、③、④中,均需进行的操作是_____________(填操作名称)。
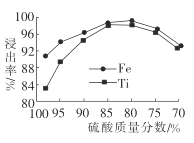
(2)滤液1中钛元素以TiO2+形式存在,步骤①中生成TiO2+的化学方程式为__________,硫酸质量分数对钛、铁浸出率的影响如图所示.据此判断,酸浸时所加硫酸的质量分数应为______(填范围)。.
(3)请结合离子方程式解释步骤④中加热水的原因:__________。
(4)电解法制备Ti的装置是以石墨为阳极,TiO2为阴极,熔融CaO为电解质。Ti在_______(填“阳极”或“阴极”)生成,____(填“能”或“不能”)将熔融CaO换成石灰乳。
(5)以绿矾为原料,可以制备重要工业原料氧化铁,基本流程如下:
![]()
①绿矾溶液中离子浓度由大到小的顺序为__________。
②FeCO3达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+ )=1.0×10-5 mol·L-1。所得FeCO3中_____(填“含”或“不含”)有Fe(OH)2。已知: {Ksp[Fe(OH)2]= 4.9×10-17}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值。下列说法正确的是( )
A.20gH218O和D2O的混合物中含有中子10NA
B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
C.1L0.1mol·L-1的Na2CO3溶液中HCO3-和CO32-离子数之和为0.1NA
D.pH=1的硫酸溶液,含有氢离子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用化学平衡移动原理解释的是
A.新制氯水长时间放置颜色变浅
B.高压比常压更有利于 SO2 转化为 SO3
C.蒸干 AlCl3 溶液无法得到无水 AlCl3
D.滴加少量 CuSO4 溶液可以加快 Zn 与稀 H2SO4 反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤和石油不仅是重要的矿物能源,更可以通过综合利用得到多种有机化工产品。
(一)乙烯是石油化工最重要的基础原料,请根据以下框图回答:
![]()
(1)乙烯分子的空间结构是_____________;C官能团名称是__________________。
(2)与乙烯和氢气的加成产物互为同系物的是_______(填写编号)。
a. C2H2 b. C6H6 c. C5H12 d. C2H6O
(3)A→B的化学方程式____________________________________。
(4)A+C→乙酸乙酯的化学方程式____________________________________。
(5) “乙烯→A”的反应类型是__________反应。下列物质在一定条件下都能与乙烯反应,其中反应类型与“乙烯→A”的不相同的是_____________(填序号)。
a.氢气 b.氯化氢 c.氧气 d.溴水
(6)实验室常用乙醇和浓硫酸共热制取乙烯,温度必须控制在_______________℃,加热时要使温度迅速上升至所需温度,其原因是____________________________________;实验时常在烧瓶中加入碎瓷片,目的是_______________________;实验室常用_________________法收集乙烯。
(二)煤焦油中可以分离出一种重要的液态烃——苯。
苯和液溴可以发生反应。根据下图装置回答:
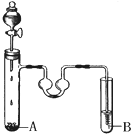
(1)现代化学认为苯分子中的碳碳键是________________________________________。
(2)反应时A试管内须放些铁丝,铁丝的作用是__________________________,A试管中发生的反应的化学方程式是 __________________________________________。
(3)双球U型管里盛放的液体是CCl4,其作用是_________________________________。
(4)当B试管盛放的是_____________(填序号),看到的现象是__________________,就可以证明该反应是取代反应。
a.硝酸银溶液 b.石蕊溶液 c.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰硫酸[M(NOSO4H)=127g·mol-1]主要用于分散染料重氮反应中取代亚硝酸钠,从而降低成本,提高产品质量。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。
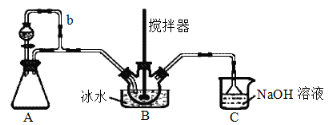
(1)装置A制取SO2,则A中反应的化学方程式为___,导管b的作用是___。
(2)SO2与装置B中盛有的浓硫酸和浓硝酸的混合液在维持体系温度不得高于20℃的条件下,反应制得NOSO4H。反应过程中,亚硝酰硫酸和硝酸的物质的量随时间的变化如图所示。反应进行到10min后,反应速度明显加快,其可能的原因是___。
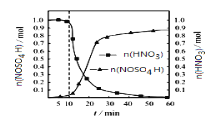
(3)装置C的主要作用是__。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是__。
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.500g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
达到滴定终点时的现象为__,亚硝酰硫酸的纯度为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.2.0gD2中含有的中子数目为0.8NA
B.4.6gC2H6O中含有C—H键的数目一定为0.6NA
C.11.2L(标准状况)由甲烷和乙烯组成的混合气体中含有氢原子数目为2NA
D.常温下,将2.8gFe置于足量的浓硝酸中,转移的电子数目—定为0.15NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化苯(基)硒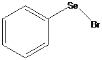 有剧毒,是一种合成有机硒化合物的重要中间体。可由乙酸基笨基硒在四氯化碳中与溴反应经乙酸处理得到,回答下列问题:
有剧毒,是一种合成有机硒化合物的重要中间体。可由乙酸基笨基硒在四氯化碳中与溴反应经乙酸处理得到,回答下列问题:
(1)Br原子核外能量高的能层符号是__________,其基态原子价电子排布式为_______。
(2)C、N、O三种原子的第一电离能由大到小的顾序为_______。
(3)乙酸分子中碳原子的杂化方式为_______。
(4) H2Se的沸点_______(填“>”“<”或“=”)H2S,原因是_______。
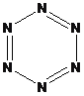
(5)晶体氮(N6)的结构如下图所示,其熔点为70℃,晶体氮中存在的作力有_______。
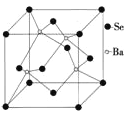
(6)BaSe可用于光电池,其晶胞结构如上图所示,晶胞参数a=0.786nm,NA代表阿伏加徳罗常数,列式计算BaSe晶胞密度为____gcm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙同学通过如下实验探究乙烯的部分化学性质。
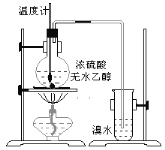
(1)实验室制乙烯的化学方程式是__________________,乙烯使溴水褪色的化学反应类型是______________。
(2)甲同学观察到当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,此黑色物质是_________;超过170℃后生成气体速度明显加快并伴有刺激性气味气体产生,这种刺激性气味气体是_________,该气体的存在不能认为溴水褪色是乙烯的加成反应造成的,原因是(用化学方程表示):________________________。
(3)乙同学经分析认为可能还有CO、CO2两种气体产生。为检验CO是否存在,他设计了如下装置。

装置a的作用是_________________,浓溴水的作用是______________,稀溴水的作用是________________。实验发现最后气体经点燃是蓝色火焰,确认有一氧化碳。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com