
����Ŀ���������ں��졢DZ����ҽ�Ʒ���Ӧ�ù㷺����������[��Ҫ�ɷ�Ϊ��������(FeTiO3),������Fe2O3]Ϊԭ���Ʊ��ѵĹ���������ͼ��ʾ��

(1)����ڡ��ۡ�����,������еIJ�����_____________(���������)��
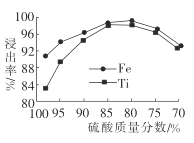
(2)��Һ1����Ԫ����TiO2+��ʽ����,�����������TiO2+�Ļ�ѧ����ʽΪ__________,���������������ѡ��������ʵ�Ӱ����ͼ��ʾ.�ݴ��ж�,���ʱ�����������������ӦΪ______(�Χ)��.
(3)�������ӷ���ʽ���Ͳ�����м���ˮ��ԭ��:__________��
(4)��ⷨ�Ʊ�Ti��װ������ʯīΪ����,TiO2Ϊ����,����CaOΪ����ʡ�Ti��_______(��������������������)���ɣ�____(������������������)������CaO����ʯ���顣
(5)���̷�Ϊԭ��,�����Ʊ���Ҫ��ҵԭ��������,������������:
![]()
���̷���Һ������Ũ���ɴ�С��˳��Ϊ__________��
��FeCO3�ﵽ�����ܽ�ƽ��ʱ,�����²����Һ��pHΪ8,c(Fe2+ )=1.0��10-5 mol��L-1������FeCO3��_____(������������������)��Fe(OH)2����֪: {Ksp[Fe(OH)2]= 4.9��10-17}
���𰸡����� FeTiO3+2H2SO4![]() FeSO4+TiOSO4+2H2O 80%~85% TiO2++ 2H2O
FeSO4+TiOSO4+2H2O 80%~85% TiO2++ 2H2O![]() H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������� ���� ���� c(SO42-)>c(Fe2+)>c(H+)>c(OH-) ����
H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������� ���� ���� c(SO42-)>c(Fe2+)>c(H+)>c(OH-) ����
��������
����������ܽ���˵õ�����TiO2+��Fe3+����Һ������Һ�м����ۻ�ԭFe3+�����˳�ȥ����������Һ��ȴ�ᾧ�����˵õ�FeSO47H2O�ͺ���TiO2+����Һ��������ˮ�ٽ�TiO2+ˮ������H2TiO3������H2TiO3����TiO2����������Ti���Դ˽����⡣
(1)���ݷ�����֪����ڡ��ۡ����У�������еIJ����ǹ��ˣ�
(2)��Ӧ��Ϊ�������Ԫ���غ��֪����ʽΪFeTiO3+2H2SO4![]() FeSO4+TiOSO4+2H2O������ͼ���֪��������������80%~85%֮��ʱ���������
FeSO4+TiOSO4+2H2O������ͼ���֪��������������80%~85%֮��ʱ���������
(3)TiO2+��ˮ��Һ�з���ˮ��TiO2++ 2H2O![]() H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������У�����H2TiO3��
H2TiO3+2H+��ˮ�ⷴӦ�����ȷ�Ӧ������ˮ�ٽ���Ӧ������Ӧ������У�����H2TiO3��
(4)��TiO2����Ti��TiԪ�ػ��ϼ۽��ͷ�����ԭ��Ӧ�������������õ��ӷ�����ԭ��Ӧ��������ʯ���飬ʯ��������ˮ���������������������õ������ѣ����Բ��ܽ�����CaO����ʯ���飻
(5)���̷���Һ���������ӻᷢ��ˮ��ʹ��Һ�����ԣ�������Һ������Ũ���ɴ�СΪc(SO42-)>c(Fe2+)>c(H+)>c(OH-)��
�ڸ������⣬pHΪ8����c(OH-)=1��10-6mol/L����Ϊc(Fe2+)c2(OH-)=1.0��10-5��(1��10-6)2 =1.0��10-17��Ksp[Fe(OH)2]������Fe(OH)2���ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ͨ����ͼ��ʾ��װ������ȡ�������밴Ҫ��ش��������⣺
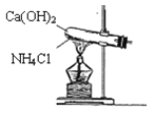
��1��ʵ������ȡ�����Ļ�ѧ��Ӧ����ʽΪ__��
��2���������Ϸ���������Ҳ�������Ʊ���������___��
�ٹ�̬�Ȼ�識��ȷֽ�
��Ũ��ˮ�м��������������
�ۼ���Ũ��ˮ
��3��NH3�Ĵ������Ļ�ѧ��Ӧ����ʽΪ__��
��4������װ��A�ռ�����ʱ��Ӧѡ�����Ľ�������___(ѡ�a����b��)����˵��ѡ�������___��
�ڴ�װ��A�е�ֹˮ�У����۲쵽��ƿ�ڲ����˺�ɫ��Ȫ����˵���������е�������___��___��
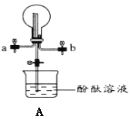
��5��ͨ��������ʲô������������ɫ��Һ���Ƿ���NH4+___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�������õIJ��ֹ�����ͼ��ʾ������˵����ȷ����( )

A. ���̢��У����ε��ᴿֻ�漰���ӡ��ᾧ����������
B. ���̢��У���ҵ�ϳ��� NaOH ��Ϊ�������õ� Mg(OH)2
C. ���̢��У�ֱ�Ӽ������� MgCl2 ��Һ���ɵõ���ˮ MgCl2
D. ���̢��У�����ѡ�� Na2SO3 ������Һ������ SO2 ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���ס����Ԫ���γɵĵ��ʺͻ��������������������Ҫ����;��
(1)���е�ԭ�ӵĵ����Ų�ͼ��ʾ��״̬�У������ɵ͵��ߵ�˳����___(����ĸ)��
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(2)P4S3����������������ӽṹ��ͼ��ʾ��
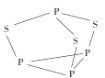
��P4S3��������ԭ�ӵ��ӻ��������Ϊ___��
��1molP4S3�����к��еŵ��ӶԵ���ĿΪ___�ԡ�
(3)��ѧ�Һϳ���һ�������ӡ�N5n+������ṹ�ǶԳƵģ�5��N�ųɡ�V���Σ�ÿ��N���ﵽ8�����ȶ��ṹ���Һ���2�������������˺��ֺϳ���һ�ֺ��С�N5n+���Ļ�ѧʽΪ��N8�������Ӿ���(�þ�����ÿ��Nԭ�Ӷ��ﵽ��8�����ȶ��ṹ)��N8�ĵ���ʽΪ___��(CN)2�м����֮��ļн�Ϊ180�㣬���жԳ��ԣ�������ÿ��ԭ�ӵ�����������8�����ȶ��ṹ����ṹʽΪ___��
(4)ֱ�������������������������������������������ͨ�����ö�����ԭ�����������ģ���ṹ��ͼ��ʾ������n�������������γɵ�������������ӵ�ͨʽΪ___��

(5)̼�����е������Ӳ�ͬ���ȷֽ��¶ȾͲ�ͬ���±�Ϊ����̼���ε��ȷֽ��¶ȺͶ�Ӧ���������ӵİ뾶�����Ž��������Ӱ뾶������̼���ε��ȷֽ��¶������ߣ�ԭ����___��
̼���� | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
�ȷֽ��¶�/�� | 402 | 900 | 1172 | 1360 |
���������Ӱ뾶/pm | 66 | 99 | 112 | 135 |
(6)ʯī�ľ����ṹ��ͼ��ʾ����֪ʯī���ܶ�Ϊ��g��cm-3��C-C���ļ���Ϊrcm��NAΪ�����ӵ�������ֵ����ʯī����IJ���d=___cm��
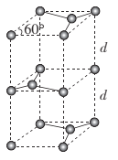
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾAlCl3��Һ��NaOH��Һ�μӹ������������Ĺ�ϵ���ߡ� �ж�����˵������ȷ���ǣ� ��
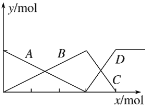
A.A�߱�ʾAl3�������ʵ����ı仯
B.x��ʾNaOH�����ʵ���
C.C�߱�ʾAl(OH)3�����ʵ����ı仯
D.D�߱�ʾAl(OH)3�����ʵ����ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��þ���Ͻ�(������������)Ͷ�뵽50ml��ϡ������Һ�У���ַ�Ӧ������ʣ�࣬��������Һ����ε���cmol/LNaOH��Һʱ���õ����������������μ�NaOH��Һ���������ͼ��ϵ��
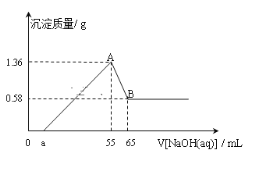
��1��ͼ��B���ʾ�����Ļ�ѧʽΪ___��AB�η�����Ӧ�����ӷ���ʽΪ___��
��2���Ͻ��н����������ʵ���Ϊ___mol��
��3��ϡ������Һ��Ũ��Ϊ___mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���H+��Mg2+��NH4+��Al3+��Fe3+��CO32����SO42����Cl���еļ��֡�������п��,������ɫ��ζ������;������NaOH��Һ,������ɫ����,�Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ��������˵������ȷ����
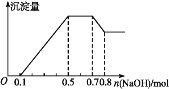
A. ��Һ�е���������H+��Mg2+��NH4+��Al3+
B. ��Һ��n(Al3+)=0.1 mol
C. ��Һ��һ������CO32��,���ܺ���SO42����Cl��
D. n(H+)��n(Al3+)��n(Mg2+)=1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͼʾ���ó��Ľ�����ȷ����(����)
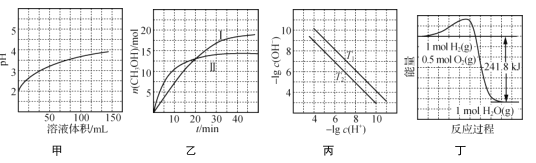
A. ͼ�ױ�ʾ1 mL pH��2ijһԪ����Һ��ˮϡ��ʱ��pH����Һ������ı仯���ߣ�˵��������ǿ��
B. ͼ�ұ�ʾ�����ܱ�����������������ͬʱ�ı��¶ȣ���ӦCO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)��n(CH3OH)��ʱ��ı仯���ߣ�˵����Ӧƽ�ⳣ��K��>K��
CH3OH(g)��H2O(g)��n(CH3OH)��ʱ��ı仯���ߣ�˵����Ӧƽ�ⳣ��K��>K��
C. ͼ����ʾ��ͬ�¶���ˮ��Һ�У�lg c(H��)����lg c(OH��)�仯���ߣ�˵��T1>T2
D. ͼ����ʾ1 mol H2��0.5 mol O2��Ӧ����1 mol H2O�����е������仯���ߣ�˵��H2��ȼ������241.8 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�װ�ò��ܴﵽʵ��Ŀ����
A.���â����ն���İ���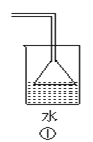
B.װ�âڿ����ڳ�ȥCl2�е�HCl
C.װ�âۿ����ڸ��ﰱ��
D.װ�âܿ������ſ������ռ�H2��CO2��Cl2��HCl������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com