
下列有关化学用语正确的是( )
|
| A. | 氮分子的电子式: | B. | 氮原子电子排布式:1s22s22p5 |
|
| C. | 硝基苯的结构简式为 | D. | 表示甲烷分子的比例模型: |
| 电子式、化学式或化学符号及名称的综合. | |
| 专题: | 化学用语专题. |
| 分析: | A.氮气分子中存在氮氮三键,即两个氮原子之间存在3对共用电子对; B.氮原子的核电荷数为7,最外层含有5个电子,2p轨道应为3个电子; C.硝基书写错误,硝基写在苯环左边,应该表示为:O2N﹣; D.甲烷为正四面体结构,分子中存在1个C、4个H原子,且碳原子半径大于氢原子. |
| 解答: | 解:A.氮气中存在3对氮氮共用电子对,氮气分子正确的电子式为: B.氮原子的结构示意图为 C.硝基写在苯环左边,应该表示为:O2N﹣,硝基苯正确的结构简式为: D.甲烷中含有1个C、4个H原子,C原子半径大于氢原子,为正四面体结构,甲烷分子的比例模型为: 故选D. |
| 点评: | 本题考查了常见化学用语的书写判断,题目难度中等,注意掌握原子结构示意图、比例模型、结构简式、电子式等化学用语的概念及表示方法,选项C为易错点,注意硝基正确的书写方法. |


科目:高中化学 来源: 题型:
下列叙述不正确的是
A.光照氯水有气泡逸出,该气体是Cl2
B.工业上可用碳在高温下还原二氧化硅制取硅
C.工业上可用氯气和石灰乳为原料制造漂白粉
D.将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路
查看答案和解析>>
科目:高中化学 来源: 题型:
有一固体粉末可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,可证明滤液中含Na+,不含K+。
由上述现象推断:
(1)该混合物中一定含有 ;一定不含有 ;
(2)可能含有 ,如要检验其是否存在,将如何操作
。
查看答案和解析>>
科目:高中化学 来源: 题型:
某氯化铁样品含有FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
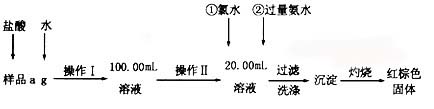
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、
(填仪器名称).
(2)加入过量氨水生成沉淀的离子方程式为 ;
(3)若不用氯水,可用下列试剂中的 代替(填序号)。
A.H2O2 B.碘水 C.NaClO
(4)步骤⑤中检验沉淀是否洗净的方法是 。
(5)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为
(请把结果约到最简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学键的叙述正确的是( )
|
| A. | 非金属元素组成的化合物中只含共价键 |
|
| B. | C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键 |
|
| C. | 不同元素的原子构成的分子只含极性共价键 |
|
| D. | CH4中所有的价电子都参与形成共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
3 SiO2+ 6 C+ 2 N2 1 Si3N4+ 6 CO
1 Si3N4+ 6 CO
(1)配平上述反应的化学方程式(将化学计量数填在方框内)
(2)该反应中的氧化剂是 N2 ,其还原产物是 Si3N4 ;
(3)该反应的平衡常数表达式为K=  ;
;
(4)若知上述反应为放热反应,则其反应热为△H 小于 零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值 减小 (填“增大”、“减小”或“不变”)
(5)若使压强增大,则上述平衡向 逆 反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18mol/(L•min)则N2的消耗速率为v(N2)= 6 mol/(L•min).
查看答案和解析>>
科目:高中化学 来源: 题型:
一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
A.浓硫酸与水 B.生石灰与水 C.熟石灰与水 D.氯化钠与水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.氮族元素的氢化物中,NH3的沸点最低
B.非金属性:Cl > Br > I,所以酸性:HCl > HBr > HI
C.Na和Cs同主族,所以NaCl和CsCl晶胞的结构相同
D.O和S同主族,所以CO2和CS2都是直线型非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com