
【题目】某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
(1)根据下表中数据,在下图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:_________
t/min | X/mol | Y/mol | Z/mol |
0 | 1.00 | 1.00 | 0.00 |
1 | 0.90 | 0.80 | 0.20 |
3 | 0.75 | 0.50 | 0.50 |
5 | 0.65 | 0.30 | 0.70 |
9 | 0.55 | 0.10 | 0.90 |
10 | 0.55 | 0.10 | 0.90 |
14 | 0.55 | 0.10 | 0.90 |

(2)体系中发生反应的化学方程式是___________________________________________;
(3)列式计算该反应在0~3 min时间内产物Z的平均反应速率:_________________________;
(4)该反应达到平衡时反应物X的转化率α等于__________________________________________ ;
(5)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是: 1___________________,2_______________________,3______________________。
1___________________,2_______________________,3______________________。
【答案】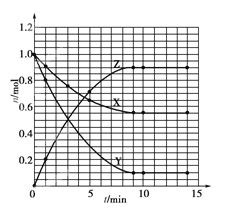
![]()
![]() 45%升高温度加入催化剂增大压强
45%升高温度加入催化剂增大压强
【解析】
(1)依据图表数据画出X、Y、Z的物质的量(n)随时间(t)变化的曲线;(2)分析达到平衡时消耗X、Y和生成Z的物质的量物质的量之比,物质的量的变化与化学计量数呈正比写出化学方程式;(3)依据化学反应速率概念是单位时间内物质浓度变化计算反应速率;(4)X的转化率=![]() ×100%;(5)根据平衡时Z的物质的量的变化,结合正反应为放热反应,且为气体体积增大的反应,分析平衡的移动,进而判断改变的条件;
×100%;(5)根据平衡时Z的物质的量的变化,结合正反应为放热反应,且为气体体积增大的反应,分析平衡的移动,进而判断改变的条件;
(1)依据图表数据,X、Y、Z的物质的量(n)随时间(t)变化的曲线是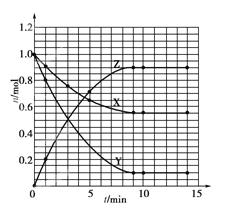 ;(2)由表中数据可知,X、Y为反应物,Z为生成物,9min时△n(X)=1mol-0.55mol=0.45mol,△n(Y)=2mol-1.1mol=0.9mol,△n(Z)=0.9mol,9min后各物质的物质的量不再变化,且反应物不为0,故为可逆反应,物质的量变化量之比等于化学计量数之比,n(X):n(Y):n(Z)=0.45:0.9:0.9=1:2:2,故反应方程式为X+2Y
;(2)由表中数据可知,X、Y为反应物,Z为生成物,9min时△n(X)=1mol-0.55mol=0.45mol,△n(Y)=2mol-1.1mol=0.9mol,△n(Z)=0.9mol,9min后各物质的物质的量不再变化,且反应物不为0,故为可逆反应,物质的量变化量之比等于化学计量数之比,n(X):n(Y):n(Z)=0.45:0.9:0.9=1:2:2,故反应方程式为X+2Y![]() 2Z;(3)0~3 min时间内产物Z的变化量为0.5mol,
2Z;(3)0~3 min时间内产物Z的变化量为0.5mol,![]() 0.083
0.083![]() ; (4)该反应达到平衡时反应物X的转化率α=
; (4)该反应达到平衡时反应物X的转化率α=![]() ;(5)正反应为放热反应,且为气体体积增大的反应。由表中数据可知,平衡时Z的物质的量为0.9mol,由图可知曲线①平衡后,Z的物质的量为0.6,Z的物质的量减小,故平衡向逆反应移动,应是升高温度;曲线②平衡后,Z的物质的量为0.9mol,Z的物质的量未变,应是使用催化剂;曲线③平衡后,Z的物质的量为0.95mol,Z的物质的量增大,平衡正向移动,应是增大压强。
;(5)正反应为放热反应,且为气体体积增大的反应。由表中数据可知,平衡时Z的物质的量为0.9mol,由图可知曲线①平衡后,Z的物质的量为0.6,Z的物质的量减小,故平衡向逆反应移动,应是升高温度;曲线②平衡后,Z的物质的量为0.9mol,Z的物质的量未变,应是使用催化剂;曲线③平衡后,Z的物质的量为0.95mol,Z的物质的量增大,平衡正向移动,应是增大压强。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
【题目】在t ℃时,10 L 0.4 mol·L-1 H2O2溶液发生催化分解:2H2O2===2H2O+O2↑,不同时刻测得生成O2的体积如下表,已知反应至6 min时,H2O2分解了50%(已折算为标准状况)
t/min | 0 | 2 | 4 | 6 |
V(O2)/L | 0.0 | 9.9 | 17.2 | V=? |
下列叙述正确的是(溶液体积变化忽略不计)( )
A. 0~2 min H2O2平均反应速率比4~6 min慢
B. 反应至6 min时,共产生O2 44.8 L
C. 0~6 min的平均反应速率v(H2O2)≈3.3×10-2 mol·L-1·min-1
D. 反应至6 min时,c(H2O2)=0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前钴酸锂(LiCoO2)锂离子电池应用十分广泛,从废旧钴酸锂理离子电池中回收铝、铁、钴、锂等元素成了重要的研究课题,某小组模拟工业流程从废旧电池中对上述元素进行提取。
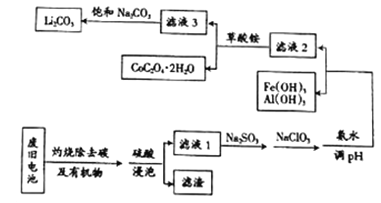
已知:①滤液1中阳离子有H+、CO3+、Fe3+、Al3+、Li+等;
②几种物质不同温度下的溶解度如下表所示:
T/℃ | 20 | 40 | 60 | 80 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)钴酸锂(LiCoO2)中钴元素的化合价是_______________。
(2)上述流程中将CoO2-转化为Co3+的离子方程式为_________________。
(3)滤液1中加入Na2SO3的主要目的是_____________________;加入NaClO3的主要目的是____________。
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mol·L-1时表示已沉淀完全)加入氨水调节pH的最小值是____________(保留一位小数)。{已知:Ksp[Fe(OH)3]=1.0×10-39,Ksp[Al(OH)3]=2.7×10-34,lg3=0.52}
(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是_________。
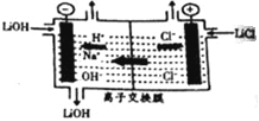
(6)为得到高纯度的Li2CO3,需将粗产品Li2CO3与盐酸反应制得的LiCl进行电解。其原理如图所示:
①电解时阳极的电解反应式为_____________________。
②电解后向产品LiOH溶液中加入过滤NH4HCO3溶液生成Li2CO3,反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的是( )
选项 | 实验目的 | 实验操作 |
A | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
B | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在足量的稀硫酸中 |
D | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、蒸发 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是( )
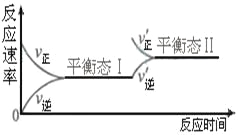
A. 反应达平衡时,正反应速率和逆反应速率相等
B. 该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
C. 该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D. 同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅元素的单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用。试回答下列问题:
(1)硅在自然界中最主要的存在形式是_______和_______。
(2)有下列物体或设备:①水晶镜片 ②计算机芯片 ③玛瑙手镯 ④硅太阳能电池 ⑤石英光导纤维。(用序号填写)用到硅单质的是_________;所用材料主要为SiO2的是_________;
(3)写出工业上制取粗硅的化学反应方程式___________。其中,氧化剂为_____________,还原剂为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某条件下,合成氨反应的数据如下:
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
起始浓度/mol·L-1 1.0 3.0 0.2
2s末浓度/mol·L-1 0.6 1.8 1.0
4s末浓度/mol·L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是 ( )
A. 2s末氨气的反应速率=0.4mol·(L·s)-1
B. 前2s时间内氨气的平均反应速率=0.4mol·(L·s)-1
C. 前4s时间内氨气的平均反应速率=0.3mol·(L·s)-1
D. 2~4s时间内氨气的平均反应速率=0.2mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
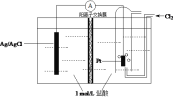
A. 负极反应为Ag-e-+Cl-=AgCl
B. 放电时,交换膜右侧溶液中pH升高
C. 当电路中转移0.1 mol e-,通过交换膜的阳离子为0.2 mol
D. 用KCl溶液代替盐酸,则电池总反应改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com