
| A、加氢氧化钠溶液溶解后分液 |
| B、加盐酸一起蒸馏 |
| C、加水溶解后分液 |
| D、加有机溶剂后分液 |
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
| A、往容积一定的容器中再通入O2,可以加快反应2SO2+O2?2SO3的反应速率 |
| B、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C、对于C(s)+H2O(g)?CO(g)+H2(g)的反应,加入固体炭,反应速率加快 |
| D、100mL 2mol?L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将乙醇蒸汽通过灼热的氧化铜,固体颜色由黑色变为红色 |
| B、苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷 |
| C、一定条件下,将苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D、往溴水中加入四氯化碳溶液,水层褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH3-CH3+Br2
| |||
B、2CH3CHO+O2
| |||
| C、CH3-CH═CH2+Br2→CH3-CHBr-CH2Br | |||
D、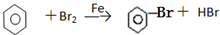 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO32-、OH-、Na+、H+ |
| B、Al3+、Na+、AlO2-、Cl- |
| C、Ba2+、HCO3-、K+、SO42- |
| D、S2-、H+、SO42-、Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
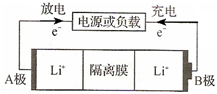 如图为摇摆电池的工作原理图,在充放电过程中Li+在两极间“摇来摇去”,其总反应为:LiCoO2+6C
如图为摇摆电池的工作原理图,在充放电过程中Li+在两极间“摇来摇去”,其总反应为:LiCoO2+6C | 充电 |
| 放电 |
| A、放电时,负极反应为:LiCoO2-═Li(1-x)CoO2+xLi+ |
| B、充电时,B极发生还原反应 |
| C、充电时,Li+穿过隔离膜向B极移动 |
| D、当A极得到x mol电子,电池消耗6 mol C |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | A | B | C | D |
| 目的 | 压强对平衡的影响 | 温度对转化率的影响 | 增加O2浓度对速率的影响 | 浓度对平衡常数的影响 |
图示 |  |  |  |  |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com