
����Ŀ��2019��ŵ������ѧ�������Ϊ﮵�ط�չ����ͻ��������λ��ѧ�ҡ�ij�Ͼ�﮵��������Ҫ��LiFePO4��������̿�ڵ���ɣ�Fe��Li��P���м��ߵĻ��ռ�ֵ�������������£�

��1�����̢�����NaAlO2��Һ�����ӷ���ʽ��__��
��2�����̢���HCl/H2O2��������__��
��3������ҺX����Ҫ�ɷ�Ϊ Li+��Fe3+��H2PO4-�ȡ����̢�����̼������ҺŨ��20%���¶�85 �桢��Ӧʱ��3 h�����£�̽��pH��������������Ӱ�죬��ͼ��ʾ��
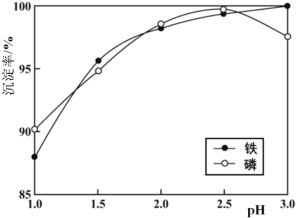
���ۺϿ��������׳����ʣ����pHΪ__��
�ڽ��ƽ���ƶ�ԭ���������̢���pH���������׳����������ԭ��__��
�۵�pH��2.5����pH���ӣ��׳����ʳ����˼�С�����ƣ�������ԭ��__��
��4��LiFePO4����ͨ��(NH4)2Fe(SO4)2��H3PO4��LiOH��Һ������������Ӧ��ȡ����������Ӧ�Ļ�ѧ����ʽΪ__��
���𰸡�2Al��2OH-��2H2O=2AlO2-��3H2�� �ܽ�LiFePO4����Fe2+����ΪFe3+��2Fe2++H2O2+2H+=2Fe3++2H2O�� 2.5 H2PO4-![]() HPO42-+H+��HPO42-
HPO42-+H+��HPO42-![]() PO43-+H+������Na2CO3��CO32-���H+ʹc(H+)��С���ٽ���������ƽ�������ƶ���c(PO43)������Fe3+����γ����������������ߣ�H2PO4-
PO43-+H+������Na2CO3��CO32-���H+ʹc(H+)��С���ٽ���������ƽ�������ƶ���c(PO43)������Fe3+����γ����������������ߣ�H2PO4-![]() HPO42-+H+��HPO42-
HPO42-+H+��HPO42-![]() PO43-+H+����ҺpH����c(H+)��С���ٽ���������ƽ�������ƶ���c(PO43-)������Fe3+����γ����������� pH��2.5ʱ�������е����������в��ֿ�ʼת������Fe(OH)3��ʹ�ò���PO43-�ͷţ������׳������½� (NH4)2Fe(SO4)2+H3PO4+LiOH=2NH4HSO4+LiFePO4��+H2O��(NH4)2Fe(SO4)2+H3PO4+3LiOH=(NH4)2SO4+Li2SO4+LiFePO4��+3H2O
PO43-+H+����ҺpH����c(H+)��С���ٽ���������ƽ�������ƶ���c(PO43-)������Fe3+����γ����������� pH��2.5ʱ�������е����������в��ֿ�ʼת������Fe(OH)3��ʹ�ò���PO43-�ͷţ������׳������½� (NH4)2Fe(SO4)2+H3PO4+LiOH=2NH4HSO4+LiFePO4��+H2O��(NH4)2Fe(SO4)2+H3PO4+3LiOH=(NH4)2SO4+Li2SO4+LiFePO4��+3H2O
��������
��LiFePO4��������̿�ڵķϾ�﮵�أ���NaOH�ܽ����ˣ���ҺΪNaAlO2��Һ������ΪLiFePO4��̿�ڣ����������ữ��H2O2�ܽ����������ˣ��õ���Ҫ�ɷ�Ϊ Li+��Fe3+��H2PO4-�ȵ���ҺX����X�м���Na2CO3��Һ����FePO42H2O���������˵���Һ��Ҫ��LiCl���ټ��뱥��Na2CO3��Һ���ٹ��˼��ɵõ�LiCO3�ֲ�Ʒ���ݴ˷������⡣
(1)���̢�Al����NaOH��Һ����NaAlO2��H2��������Ӧ�����ӷ���ʽ��2Al��2OH-��2H2O=2AlO2-��3H2����
(2)���̢��dz��������м��������ữ��H2O2�����˺�õ���Ҫ�ɷ�Ϊ Li+��Fe3+��H2PO4-�ȵ���ҺX����֪HCl/H2O2���������ܽ�LiFePO4����Fe2+����ΪFe3+��
(3)�ٷ���ͼ�����ݿ�֪����pH=2.5ʱ�ij�������ߣ����ij����ʽϸߣ�����̢�ѡ������pHΪ2.5��
����֪��ҺX�д���H2PO4-�ĵ���ƽ�⣬��H2PO4-![]() HPO42-+H+��HPO42-
HPO42-+H+��HPO42-![]() PO43-+H+�����̢��е�����Na2CO3��CO32-���H+ʹc(H+)��С���ٽ���������ƽ�������ƶ���c(PO43)������Fe3+����γ�����������������������׳����ʣ�
PO43-+H+�����̢��е�����Na2CO3��CO32-���H+ʹc(H+)��С���ٽ���������ƽ�������ƶ���c(PO43)������Fe3+����γ�����������������������׳����ʣ�
����֪FePO4(s)![]() Fe3+(aq)+ PO43-(aq)����pH��2.5����pH���ӣ���Һ��c(OH-)����Fe3+��ʼת������Fe(OH)3���ٽ���ƽ�������ƶ���ʹ�ò���PO43-�ͷţ������׳������½���
Fe3+(aq)+ PO43-(aq)����pH��2.5����pH���ӣ���Һ��c(OH-)����Fe3+��ʼת������Fe(OH)3���ٽ���ƽ�������ƶ���ʹ�ò���PO43-�ͷţ������׳������½���
(4)(NH4)2Fe(SO4)2��H3PO4��LiOH��Һ�������LiFePO4��ͬʱ�õ�(NH4)2SO4��Li2SO4�����ԭ���غ㣬������Ӧ�Ļ�ѧ����ʽΪ (NH4)2Fe(SO4)2+H3PO4+LiOH=2NH4HSO4+LiFePO4��+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A��һ�ֳ��õ��ڷ�ֹʹ����ҩ��1 mol A ˮ��õ�1 mol B ��1 mol ���ᡣA��Һ�������ԣ�����ʹFeCl3��Һ��ɫ��A����Է�������������200��B������̼Ԫ�غ���Ԫ���ܵ���������Ϊ0.652��A��B������̼���⡢������Ԫ����ɵķ����廯����������ƶ��У���ȷ����( )
A. A��B����Է�������֮��Ϊ60B. 1��B������Ӧ����2����ԭ��
C. A�ķ���ʽ��C7H6O3D. B����NaOH��Һ��FeCl3��Һ��Ũ��ˮ�����ʷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. ������������ȼ������Al2O3����˿��������ȼ��Ҳ����Fe2O3
B. ���ܴ�����ͭ��Һ���û���ͭ����Ҳ�ܴ�����ͭ��Һ�п����û���ͭ
C. ��Ƭ�������γ����ܵ�����Ĥ���ƿ����Ҳ���γ����ܵ�����Ĥ
D. ����������ˮ�ȷ�Ӧʱ�ƾ�����ԭ�����������ʲ���������ԭ��Ӧʱ����������ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ�������ƽ�з�Ӧ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�
CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g�� ��H1=-53.7kJ��mol-1 I
CH3OH��g��+H2O��g�� ��H1=-53.7kJ��mol-1 I
CO2��g��+H2��g��![]() CO��g��+H2O��g�� ��H2 II
CO��g��+H2O��g�� ��H2 II
ijʵ���ҿ���CO2��H2��ʼͶ�ϱ�Ϊ1��2.2������ͬѹǿ�£�������ͬ��Ӧʱ��������ʵ�����ݣ�
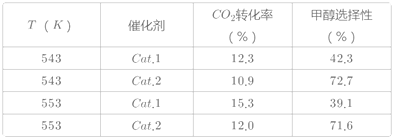
����ע��Cat.1��Cu/ZnO���װ���Cat.2��Cu/ZnO����Ƭ���״�ѡ���ԣ�ת����CO2�����ɼ״��İٷֱ�
��֪����CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJ��mol-1��-285.8kJ��mol-1
��H2O��l��=H2O��g����H3=44.0kJ��mol-1
��ش𣨲������¶ȶ���H��Ӱ�죩��
��1����ӦI��ƽ�ⳣ������ʽK=___��
��2�����������CO2ת��ΪCH3OHƽ��ת���ʵĴ�ʩ��___��
A.ʹ�ô���Cat.1
B.ʹ�ô���Cat.2
C.���ͷ�Ӧ�¶�
D.Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
E.����CO2��H2�ij�ʼͶ�ϱ�
��3������ʵ�����ݱ���������ͬ�¶��²�ͬ�Ĵ�����CO2ת����CH3OH��ѡ������������Ӱ�죬��ԭ����___��
��4����ͼ�зֱ���ӦI����������Cat.1����Cat.2�������������Ӧ���̡�������ʾ��ͼ___��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��298Kʱ����20mLcmol��L��1KOH��Һ�еμ�0.1mol��L��1HCOOH��Һ�������Һ��ˮ���������������Ũ����μӼ���(����)��Һ���(V)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
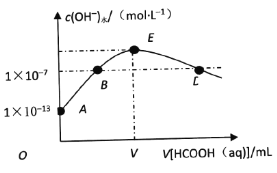
A. ����KOH��Һ��Ũ��c��0.01mol��L��1
B. B���Ӧ����Һ�У�c(K��)��c(HCOO��)
C. E���Ӧ����Һ�У�c(OH��)��c(H��)��c(HCOOH)
D. ��D���Ӧ�ļ�����Һ���ΪV1mL����HCOOH����ƽ�ⳣ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ��֤��SO2��Cl2��Ư���ԣ��������ͼ��ʾ��ʵ��װ�ã�
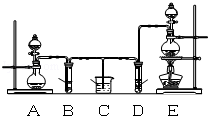
��1�������Ʊ�Cl2���ݵ�ԭ���ǣ�MnO2+4HCl��Ũ����MnCl2+2H2O+Cl2����Ӧѡ��ͼA��Eװ���е� ������ţ���Cl2����Ӧ��Ũ���������ֳ��������� �� ��
��2����Ӧ��ʼ����B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ����B��D�����Թ��е�Һ����ȣ�B�Թ��е������� ��
��3��д������NaOH��Һ��SO2���巴Ӧ�����ӷ���ʽ�� ��
��4����С��ͬѧ�����������Ϻ�ͨ��Ʒ����Һ��һ��ʱ���Ʒ����Һ��������ɫ���������ϵ�֪���������尴�����1��1��ϣ�����ˮ��Ӧ���������ֳ������ᣬ���ʧȥƯ�����ã��÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ɲ��Ƭ�ľۺ��� Y ��һ�־�������ά���ϳ�·����ͼ��
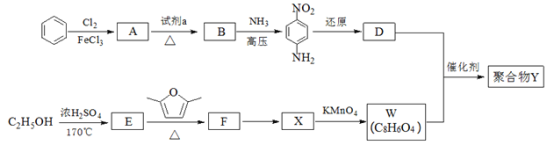
��֪��![]()
(1)���� A �ķ�Ӧ������_____��
(2)�Լ� a ��_____��
(3)B �������Ĺ����ŵ�������_____��
(4)W��D ��Ϊ���㻯��������о�ֻ�����ֲ�ͬ��ѧ��������ԭ�ӡ�
��F �Ľṹ��ʽ��_____��
�����ɾۺ��� Y �Ļ�ѧ����ʽ��_____��
(5)Q �� W ��ͬϵ������Է��������� W �� 14���� Q ��______�֣����к˴Ź���������4 ��壬�ҷ������Ϊ 1��2��2��3 ��Ϊ___________��дһ�ֽṹ��ʽ���ɣ���
(6)��д���� 1��3������ϩ����ȲΪԭ�ϣ����Լ����������ã��ϳ�![]() �ĺϳ�·��__________________�����ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
�ĺϳ�·��__________________�����ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йط�Ӧ14CuSO4��5FeS2��12H2O===7Cu2S��5FeSO4��12H2SO4������˵���д������
A. CuSO4�ڷ�Ӧ�б���ԭ
B. FeS2����������Ҳ�ǻ�ԭ��
C. 14 mol CuSO4������1 mol FeS2
D. ����ԭ��S�ͱ�������S������֮��Ϊ3��7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�������A�����ϣ��������к�̼Ϊ70.59%������Ϊ 5.88%�����ຬ�������������з����ⶨ���л����������Է��������ͷ��ӽṹ��
����һ��������������֪A��������ͼ��
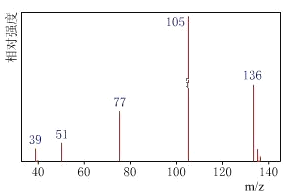
���������˴Ź����Dz��A�ĺ˴Ź���������4���壬�����֮��Ϊ1��2��2��3��
�����������ú�������Dz��A���ӵĺ�����ף���ͼ��
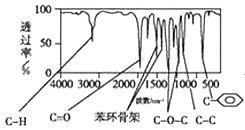
��1�������й���____�ֻ�ѧ������ͬ����ԭ�ӡ�
��2��A�ķ���ʽΪ____��
��3��������������һ���л���____��
��4��A�ķ�����ֻ��һ������������____(�����)��
a A����Է������� b A�ķ���ʽ
c A�ĺ˴Ź�������ͼ d A���ӵĺ������ͼ
��5��A�Ľṹ��ʽΪ________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com