
����Ŀ����Ԫ��������Ŵ����ʺ���Ļ����ɷ�֮һ������Ԫ��(Sn)�γɵ�ijЩ�������ܹ��ٽ�����ĺϳɡ��ش��������⡣
(1)��̬��ԭ�ӵ���ռ�ݵ�����ܲ������____��ռ�ݸ��ܲ�ĵ�����������ߵĵ�����������ڿռ���_____����չ����ԭ�ӹ����_____�Ρ�
(2)��Ԫ�ؿ��γɰ������������������ֵ��ʡ��о���������Ľṹ��õ�������_____��������������ʯ�ṹ��ͬ�����������ȶ�����ԭ����_____��
(3)��̬PCl5�ṹ�д���PCl4+��PCl6-���ֽṹ��Ԫ���侧����ͼ��ʾ��
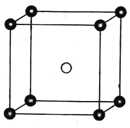
��PCl4+�Ŀռ�ṹΪ________��PCl3�ļ���С��PCl4+���ǵ�ԭ��Ϊ___________��
����֪�����ı߳�Ϊanm,�����ӵ�����ֵ��NA��ʾ����PCl4+��PCl6-֮�����̾���Ϊ_______pm,��̬PCl5���ܶ�Ϊ______g.cm-3��
���𰸡� M 3 ���� X-���������� Sn-Sn���ļ�����������С,�ʻ������ȶ� �������� PCl3��PCl4+����ԭ�ӵ��ӻ���ʽ��Ϊsp3�ӻ�, PCl3��ԭ�Ӽ۲���Ӷ�����һ�Թµ��Ӷ�, PCl4+��ԭ�Ӽ۲���Ӷ����µ��Ӷԣ��µ��ӶԶԳɼ����ӶԵ��ų������ڳɼ����Ӷ�֮����ų��� ![]()
![]()
��������(1)��Ϊ15��Ԫ�أ���̬��ԭ�ӵ���ռ�ݵ�����ܲ������M��ռ�ݸ��ܲ�ĵ�����������ߵĵ���Ϊ3p����������ڿռ���3����չ����ԭ�ӹ���������Σ��ʴ�Ϊ��M��3��������
(2)�о�����Ľṹ��õ�������X-������������������������ʯ�ṹ��ͬ��Sn-Sn���ļ����ϳ������ܽ�С�����»������ȶ����ʴ�Ϊ��X-������������Sn-Sn���ļ�����������С���ʻ������ȶ���
��3����PCl4+������ԭ��P�ļ۲���Ӷ���=4+![]() =4������sp3�ӻ����ռ�ṹΪ����������PCl3��PCl4+����ԭ�ӵ��ӻ���ʽ��Ϊsp3�ӻ�, PCl3��ԭ�Ӽ۲���Ӷ�����һ�Թµ��Ӷ�, PCl4+��ԭ�Ӽ۲���Ӷ����µ��Ӷԣ��µ��ӶԶԳɼ����ӶԵ��ų������ڳɼ����Ӷ�֮����ų�����ʹ��PCl3�ļ���С��PCl4+���ǣ��ʴ�Ϊ������������PCl3��PCl4+����ԭ�ӵ��ӻ���ʽ��Ϊsp3�ӻ�, PCl3��ԭ�Ӽ۲���Ӷ�����һ�Թµ��Ӷ�, PCl4+��ԭ�Ӽ۲���Ӷ����µ��Ӷԣ��µ��ӶԶԳɼ����ӶԵ��ų������ڳɼ����Ӷ�֮����ų�����
=4������sp3�ӻ����ռ�ṹΪ����������PCl3��PCl4+����ԭ�ӵ��ӻ���ʽ��Ϊsp3�ӻ�, PCl3��ԭ�Ӽ۲���Ӷ�����һ�Թµ��Ӷ�, PCl4+��ԭ�Ӽ۲���Ӷ����µ��Ӷԣ��µ��ӶԶԳɼ����ӶԵ��ų������ڳɼ����Ӷ�֮����ų�����ʹ��PCl3�ļ���С��PCl4+���ǣ��ʴ�Ϊ������������PCl3��PCl4+����ԭ�ӵ��ӻ���ʽ��Ϊsp3�ӻ�, PCl3��ԭ�Ӽ۲���Ӷ�����һ�Թµ��Ӷ�, PCl4+��ԭ�Ӽ۲���Ӷ����µ��Ӷԣ��µ��ӶԶԳɼ����ӶԵ��ų������ڳɼ����Ӷ�֮����ų�����
�ڸ��ݾ����ṹ��֪��PCl4+��PCl6-�ĸ�����Ϊ1:1����֪�����ı߳�Ϊanm����PCl4+��PCl6-֮�����̾���Ϊ������Խ��ߵ�һ�룬Ϊ![]() a��103 pm�������к���2��P��10��Clԭ�ӣ���̬PCl5���ܶ�Ϊ
a��103 pm�������к���2��P��10��Clԭ�ӣ���̬PCl5���ܶ�Ϊ g.cm-3=
g.cm-3=![]() g.cm-3���ʴ�Ϊ��
g.cm-3���ʴ�Ϊ�� ![]() a��103��
a��103�� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л������������������ܲ��ɷ֣������е�һЩ���ⳣ�漰��ѧ֪ʶ��
(1)�����м���ʳƷ��

�ٻ����������������������ҪӪ������Ϊ___________(����ࡱ������֬�������ʡ�)��
�ڳԷ�ʱ������һ�����о�����ζ������Ϊ���۷�����_____________(����ĸ)��Ӧ��
A.�ֽ� B.ˮ�� C.�ѽ�
(2)���ճ������У����������������________��
A.��ȼ�շ�����ë֯Ʒ����֯Ʒ
B.�ô���ϴ�ӹ����ϵ�����
C.������ζ�ķ�������ƺ��״�
D.�õ�����Һ����ӵ�ʳ�κͲ������ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������⡿����ȩ������ˮ���������л��ܼ����ܶ�Լ����ˮ���ܶȣ��ڼ��������·����绯��Ӧ�����Ʊ�����ȩ����ˮ���ܽ�Ȳ����������л��ܼ����ܶ�Լ����ˮ���ܶȣ��������ᡣ��Ӧԭ�����£�
2C6H5CHO+NaOH![]() C6H5CH2OH+C6H5COONa
C6H5CH2OH+C6H5COONa
C6H5COONa+HCl![]() C6H5COOH+NaCl
C6H5COOH+NaCl
������������������±���
����ȩ | ���״� | ������ | �� | |
�е�/�� | 178 | 205 | 249 | 80 |
�۵�/�� | 26 | -15 | 122 | 5.5 |
��������ˮ�е��ܽ�� | ||
17�� | 25�� | 100�� |
0.21g | 0.34g | 5.9g |
ʵ���������£�

��1���ڢ�����������1Сʱ����ͼ1�������м��Ȼ�Ϲ̶�װ��Ϊ������
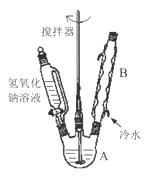
����A������Ϊ_______����������B��Ϊ����C��Ч������B��˵��ԭ��_______��
��2���������йط�Һ©����ʹ�ò���ȷ����_______
A.��Һ©����ʹ��֮ǰ��������Ƿ�©ˮ
B.��Һ©���ڵ�Һ�岻�ܹ��࣬����������
C.�����Һ©����������̨�Ͼ��ã��ֲ���������������з�Һ
D.��Һʱ���²�Һ�����������ر������������ձ��ٴ�����ʹ�ϲ�Һ������
��3�����������÷�ˮԡ���������ٽ��в����ܣ���ͼ2�����ռ�______�����֡�ͼ2����һ�����Դ�����ȷ��Ӧ��Ϊ_____________��
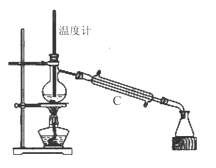
��4������ʱ����ͼ3���ձ��б����ᾧ��ת�벼��©��ʱ�������ϻ�ճ���������壬��_____��ϴ�����ϲ����ľ��塣������ɺ���������ˮ�Ծ������ϴ�ӣ�ϴ��Ӧ____________��
��5���õ�����ƽȷ��ȡ0.2440g����������ƿ�м�100mL����ˮ�ܽ⣨��Ҫʱ���Լ��ȣ�������0.1000mol/L�ı�����������Һ�ζ��������ı�����������Һ19.20mL��������Ĵ���Ϊ_____%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ�����������֮��������ת����ϵ��
��![]() ��
��![]() ��
��![]() ��
��
��1�������Dz�����ˮ�İ�ɫ�������ʣ�������������������������������Һ�������_____��д������![]() ����ת���Ļ�ѧ����ʽ��_______________________________��
����ת���Ļ�ѧ����ʽ��_______________________________��
��2��������Һ�м���KSCN��Һ����Ѫ��ɫ���֣���������ǣ�___________��д������![]() ����ת�������ӷ���ʽ��________________________________��
����ת�������ӷ���ʽ��________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£������ܱ������н��еĿ��淴ӦA(g)��3B(g)![]() 2C(g)������˵���У���˵����һ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬����( )
2C(g)������˵���У���˵����һ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬����( )
A������C��������C�ֽ���������
B��A��B��C��Ũ�����
C����λʱ������n mol A��ͬʱ����3n mol B
D��A��B��C�ķ�����֮��Ϊ1��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��������,��һ�����ܱ�������,�ܱ�ʾ��ӦX(g)+2Y(g)![]() 2Z(g)һ���ﵽ��ѧƽ��״̬���� ( )
2Z(g)һ���ﵽ��ѧƽ��״̬���� ( )
��������������ܶȲ��ٷ����仯
��X��Y��Z��Ũ�Ȳ��ٷ����仯
�������е�ѹǿ���ٷ����仯
�ܵ�λʱ��������nmol Z,ͬʱ����2nmol Y
A.�٢� B.�ڢ� C.�ۢ� D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߽���ѧ�仯�������磬�����ڽ�һ����ʶ��ѧ�仯����ͼ��ij��ѧ�仯����ʾ��ͼ��X��Y��Z�ֱ��ʾ��ͬ����ԭ�ӣ���ͼ�ش����⣺

��Ӧǰ ��Ӧ��
��1���û�ѧ��Ӧ��������ķ��Ӹ�����Ϊ______________��
��2�����۽Ƕȷ�������ѧ��Ӧǰ������ʵ������ܺ���ȵ�ԭ����__________________________________________________________��
��3���û�ѧ��Ӧ�Ļ�������Ϊ_________________________________��
��4����Xԭ�ӹ��ɵ������ڸ÷�Ӧ��____________����ǡ����ǡ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�ӽṹ��������ȷ����
A.���е�ԭ�Ӻ˶��������Ӻ�������ɵ�B.ԭ�ӵ�����������������8��
C.ϡ������ԭ�ӵ�������������Ϊ8D.ԭ�ӵĴ�������������2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ��ѧ��ʵ�����߽����ã�����������������ɫ��ѧ������

��ʵ�����ռ���������ͼ����ʾװ��
��ʵ���������������Ƶķ�Ӧʵ��ʱ����ͼ����ʾװ��
��ʵ�������ò������ֱ�պȡŨ�����Ũ��ˮ����������������ε�ʵ��
��ʵ�����в���ͼ����ʾװ�ý���ͭ��ϡ����ķ�Ӧ
A. �ڢۢ�
B. �٢ڢ�
C. �٢ڢ�
D. �٢ۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com