
��17�֣�H2O2��һ����ɫ������ԭ�Լ����ڻ�ѧ�о���Ӧ�ù㷺��
��1��ijС������ͬŨ��Fe3+�Ĵ��£�̽��H2O2Ũ�ȶ�H2O2�ֽⷴӦ���ʵ�Ӱ�졣��ѡ�Լ���������30% H2O2��0.1mol?L-1Fe2(SO4)3������ˮ����ƿ��˫������ˮ�ۡ����ܡ��������ܡ���Ͳ�����������ˮԡ�ۡ�ע����
��д����ʵ��H2O2�ֽⷴӦ����ʽ����������ת�Ƶķ������Ŀ��____________
�����ʵ�鷽�����ڲ�ͬH2O2Ũ���£��ⶨ ____________________________________��Ҫ������õ�������ֱ�����ַ�Ӧ���ʴ�С����
�����ʵ��װ�ã������ͼ��װ��ʾ��ͼ��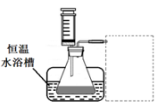
�ܲ����±���ʽ���ⶨʵ�������������ʵ�鷽�����г���ѡ�Լ���������¼�Ĵ��������������ⶨ�����ݣ���������ĸ��ʾ����
��2������ͼ21��a����21��b���е���Ϣ����ͼ21��c��װ�ã����ܵ�A��Bƿ���ѳ���NO2���壩����ʵ�顣�ɹ۲쵽Bƿ��������ɫ��Aƿ�е�_________������dz��������ԭ����______________________________________________________��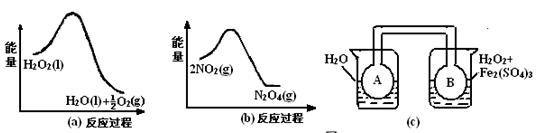
��1����
��������ͬ��������������ʱ��
��
�ܲⶨ��Ӧʱ��
��2�����Ϊ��������ֽ��Ƿ��ȷ�Ӧ��2NO2(g) H2O2�����(mL) 0.1mol?L-1Fe2(SO4)3�������mL�� ��������ˮ�������mL�� ����O2�����(mL) ��Ӧʱ�䣨min�� ʵ��1 b a c d ʵ��2 c a b d  N2O4(g)Ҳ�Ƿ��ȷ�Ӧ������Bƿ�¶ȸ���Aƿ���¶����ߣ�ƽ�������ƶ�����������Ũ��������ɫ���
N2O4(g)Ҳ�Ƿ��ȷ�Ӧ������Bƿ�¶ȸ���Aƿ���¶����ߣ�ƽ�������ƶ�����������Ũ��������ɫ���
���������������1���ٹ��������������������������·ֽ�����ˮ�������������������������������ԭ������ѧ����ʽ������ת�Ʒ������ĿΪ
�ڷ�Ӧ�����ǵ�λʱ��������Ũ�ȵĸı��������Բⶨ��ͬŨ�ȵĹ�������Էֽ����ʵ�Ӱ�죬��ⶨ��ͬʱ���ڣ���������������Ķ��٣���������ͬ�������������ʱ��Ķ��٣�
��������ˮ���������ռ�һ�������O2����Ҫˮ�ۡ���Ͳ�������ܣ���Ͳ��ʢ��ˮ������ˮ���У�װ����ͼ
��
��2����ͼa��֪��������ķֽⷴӦ�Ƿ��ȷ�Ӧ����ͼb��֪��������ת��Ϊ�����������ķ�ӦҲ�Ƿ��ȷ�Ӧ������װ��c�У��Ҳ��ձ�Bƿ�¶ȸ�������ձ�Aƿ�����¶����ߣ�ʹƽ��2NO2(g) H2O2�����(mL) 0.1mol?L-1Fe2(SO4)3�������mL�� ��������ˮ�������mL�� ����O2�����(mL) ��Ӧʱ�䣨min�� ʵ��1 b a c d ʵ��2 c a b d  N2O4(g)������У���������Ũ������Bƿ����ɫ��Aƿ����ɫ�
N2O4(g)������У���������Ũ������Bƿ����ɫ��Aƿ����ɫ�
���㣺�����ʵ��ķ�������ƣ�������ԭ��Ӧ�ķ���������ת�Ƶı�ʾ��ƽ����ƶ����ж�


 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����������NF3����һ�����͵��Ӳ��ϣ����ڳ�ʪ�Ŀ�������ˮ�����ܷ���������ԭ��Ӧ���䷴Ӧ�IJ����У� HF�� NO �� HNO3��������˵��������ǣ�( )
| A����Ӧ�����У��������뱻��ԭ��Ԫ�ص����ʵ���֮��Ϊ1 ��2 |
| B��NF3��һ����ɫ���������壬���NF3�ڿ�����й©ʱ���ױ���� |
| C��һ��NF3й©��������NaOH��Һ���ܵķ������ٿ�����Ⱦ |
| D������Ӧ������1.0mol NO��ת�Ƶĵ�����ĿΪ6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��12 �֣���ԭ������������ĵ���ƽ�ⳣ�������
| ���� | HCOOH | HNO2 | H2S | H2SO3 | H2C2O4 |
| ����ƽ�ⳣ�� ��25�棩 | K=1.8��10��4 | K=5.1��10��4 | K1=9.1��10��8 K2=1.1��10��12 | K1=1.23��10��2 K2=6.6��10��8 | K1=5.4��10��2 K2=5.4��10��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������ϡ�������ܽ⣺ ��Fe(NO3)3��NO����2H2O
��Fe(NO3)3��NO����2H2O
24.����������ʽ�ϱ������ת�Ƶķ������Ŀ��
25.�÷�Ӧ�б���ԭ��Ԫ���� ����ԭ���� ��
26.����0.1 mol���μӷ�Ӧ������ԭ��HNO3Ϊ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣�ij���ÿ���������ұ�������ȼ���״��������һ����ҵ������ͼ��ʾ���������������Դ�����ʣ������˻�����Ⱦ��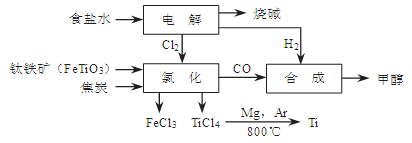
����д���пհף�
��1��д���������Ȼ��õ����Ȼ��ѵĻ�ѧ����ʽ�� ��
��2����CO��H2�ϳɼ״��Ƿ��ȵģ�����ʽ�ǣ�CO(g)��2H2(g)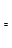 CH3OH(g)��
CH3OH(g)��
����֪�÷�Ӧ��300��ʱ�Ļ�ѧƽ�ⳣ��Ϊ0.27�����¶��½�2 mol CO��3 mol H2��2 mol CH3OH�����ݻ�Ϊ2 L���ܱ������У���ʱ��Ӧ�� ���������Ӧ������С��������淴Ӧ������С�����ƽ��״̬������
����ͼ��ʾ�ϳɼ״���Ӧ�ﵽƽ���ÿ��ֻ�ı��¶ȡ�ѹǿ�������е�ijһ��������Ӧ���ʦ���ʱ��t�Ĺ�ϵ�����б�ʾƽ�������еļ״��ĺ�����ߵ�һ��ʱ���� ��ͼ��t3ʱ�ı������������ ��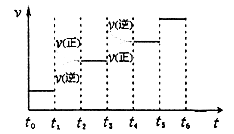
��3��ijͬѧ�����һ���״�ȼ�ϵ�أ����øõ�ص��200mL����Ũ��NaCl��CuSO4�����Һ����װ����ͼ��
��д������ͨ��״���һ���ĵ缫��Ӧʽ ��
������������������������������ʱ��仯�Ĺ�ϵ���ͼ��ʾ����������ѻ���ɱ�״���µ��������д����t1��,ʯī�缫�ϵĵ缫��Ӧʽ ��ԭ�����Һ��NaCl�����ʵ���Ũ��Ϊ mol/L����������Һ������䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ���㷺��������Ȼ����,���������������������Ҫ���塣����Ԫ�صĻ������ڹ�ҵ�������������ж��й㷺��Ӧ�á�
��1����Ԫ��ԭ�Ӻ����� ��δ�ɶԵ��ӣ�������� ��������ͬ�ĵ��ӡ�PH3���ӵĿռ乹��Ϊ ���� ���ӡ�����Ի�Ǽ��ԣ�
��2����������ͬ����Ԫ�أ�������˵�����߷ǽ��������ǿ������ �����ţ�
a��NH3��PH3�ȶ���ǿ
b��������ǿ�����ԣ������ǿ������
c��������������ֱ�ӻ��ϣ�������������ֱ�ӻ���
d���������������壬�����ǹ���
����������ʳƷ���Ӽ��м��Զ��Խ�ǿ������֮һ����ʹ������Ѫ�쵰�ױ������Ѫ�쵰��ʧȥЯ�����Ĺ��ܣ�������֯ȱ����
��3������������Һ�μӵ�K2Cr2O7������Һ�У���Һ�ɳ�ɫ��Ϊ��ɫ����Ӧ���£�����ȱ�����ʲ���ƽ��
Cr2O72��+ NO2��+ �� Cr3+ + NO3��+
��4�����ⷴӦ��ÿ����0.6mol NO2����ת�Ƶ�����Ϊ ��
��5���������NO��NO2����Ⱦ����������Na2CO3��Һ����NO2������CO2��9.2gNO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1 mol����Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ʢ��KI��Һ���Թ��м�������CCl4��μ���ˮ��CCl4������ɫ������������Թ��еμ���ˮ����CCl4�����dz���������ɫ�����������գ�
(1)д������ƽCCl4������ɫ�����ɫ�Ļ�ѧ��Ӧ����ʽ ��
(2)���������еĻ�ԭ���� ��
(3)��KI����KBr����CCl4���Ϊ ɫ�������μ���ˮ��CCl4�����ɫû�б仯��Cl2��HIO3��HBrO3��������ǿ������˳���� ��
(4)�ӵ����к�����Ϊ20��50 mg��kg��1����ȡ�ӵ���(��KIO3��ʳ��)1 000 kg������KI��Cl2��Ӧ��KIO3��������Ҫ����Cl2 L(��״��������2λС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ۻ�(As4S4)�ʹƻ�(As2S3)����ȡ�����Ҫ����ԭ�ϣ���������Ȼ���й����������������������գ�
(1)As2S3��SnCl2�������з�Ӧת��ΪAs4S4��SnCl4���ų�H2S���塣��As2S3��SnCl2������ȫ��Ӧ��As2S3��SnCl2�����ʵ���֮��Ϊ ��
(2)������Ӧ�е��������� ����Ӧ������������� ���ա�
(3)As2S3��HNO3�����·�Ӧ��
As2S3��10H����10NO3��=2H3AsO4��3S��10NO2����2H2O������2 mol H3 AsO4����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ �������÷�Ӧ��Ƴ�һԭ��أ���NO2Ӧ���� (�������������)�����ݳ���
(4)����Ӧ����NO2��11.2 L O2(��״��)��Ϻ���ˮ����ȫ��ת����ŨHNO3��Ȼ���������̼��Ӧ����������CO2���� (ѡ����)��
a����0.5 mol b������0.5 mol
c������0.5 mol d����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ɻ�ͭ��(��Ҫ�ɷ���CuFeS2)���ƾ�ͭ�Ĺ�������ʾ��ͼ���£�
��1���ڷ���¯�У���ͭ����ɰ��ʯӢɰ��ϼ��ȵ�1000�����ң���ͭ���������Ӧ����Cu��Fe�ĵͼ�������ֵͼ�����Ļ�ѧʽ�ֱ�Ϊ________��_______���ڷ�Ӧ�����л���һ����Fe������ת��Ϊ�ͼ�������仯ѧ��Ӧ����ʽΪ____________��
��2����ͭ(Cu2S��FeS�����ۺ϶���)��Cu���ϵ͡�ת¯�У�����ͭ���ۼ�(ʯӢɰ)��1200�����Ҵ���������д�������ͭ�е�Cu2S��������Cu2O����ÿ��1mol�����μӷ�Ӧ������������������ʵ���Ϊ_________�����ɵ�Cu2O��Cu2S��Ӧ�����Ƶú�Cu���ϸߵĴ�ͭ��
��3����ͭ�ĵ�⾫����ͼ��ʾ���ڴ�ͭ�ĵ������У�cΪ��ͭ�壬 ��a��Ӧ���ӵ�Դ��_____��(���������)������ͭ�к���Au��Ag��Fe���ʣ����������c�缫�Ϸ�����Ӧ�ķ���ʽ��__________��
��4������Ӧ�����Ը��������Һ�ζ����ⶨ��Ӧ����Һ����Ԫ�صĺ������ζ�ʱ�����ü�ʽ�ζ���ʢ�����Ը��������Һ��ԭ����____________��������Ӧ�����ӷ���ʽΪ_____________���ζ�ʱ����ƿ�е���Һ��Ӵ������������Ԫ�صĺ�����____(�ƫ�ߡ���ƫ�͡�)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com