
【题目】将等物质的量浓度、等体积的Ba(OH)2溶液与NaHSO4混合后,滴入紫色石蕊试液溶液呈
A. 蓝色 B. 红色 C. 紫色 D. 无色
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】砷(As)广泛分布于自然界,其原子结构示意图是 ![]() .
.
(1)砷位于元素周期表中族,其气态氢化物的稳定性比NH3(填“强”或“弱”).
(2)砷的常见氧化物有As2O3和As2O5 , 其中As2O5热稳定性差.根据图1写出As2O5分解为As2O3的热化学方程式: . 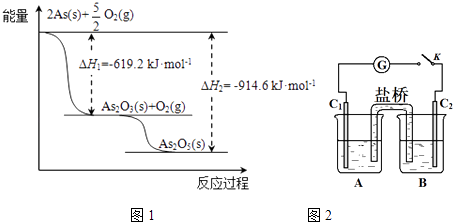
(3)砷酸盐可发生如下反应:AsO43﹣+2I﹣+2HAsO33﹣+I2+H2O.图2装置中,C1、C2是石墨电极
①A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是 .
②一段时间后,当电流计指针回到中间“0”位时,再向B中滴加过量浓NaOH溶液,可观察到电流计指针(填“不动”、“向左偏”或“向右偏”).
(4)利用(3)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样溶于NaOH溶液,得到含AsO43﹣和AsO33﹣的混合溶液.
As2O5与NaOH溶液反应的离子方程式是 .
②上述混合液用0.02500molL﹣1的I2溶液滴定,消耗I2溶液20.00mL.滴定完毕后,使溶液呈酸性,加入过量的KI,析出的I2又用0.1000molL﹣1的Na2S2O3溶液滴定,消耗Na2S2O3溶液30.00mL.(已知2Na2S2O3+I2=Na2S4O6+2NaI)试样中As2O5的质量是 g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,在生产和生活中的应用十分广泛。某化学兴趣小组在实验室中对Cl2与FeCl2和KSCN混合溶液的反应进行了探究。回答下列问题:
(1)Cl2为制备
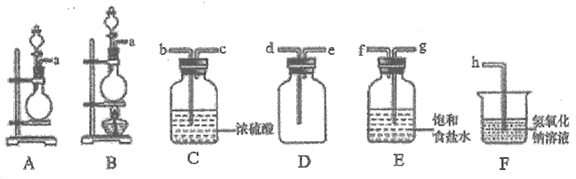
①该小组同学选用KMnO4固体和浓盐酸混合快速制备Cl2,气体发生装置应选择__(填大写字母),该反应的离子方程式为___________。
②欲收集一瓶干燥纯净的氯气,选择上图中的装置,其连接顺序为a→________(按气流方向,用小写字母表示)。
(2)Cl2的性质实验
Cl2与FeCl2和KSCN混合溶液的反应,随着Cl2不断通入,A装置中溶液先变红,后逐渐褪色。
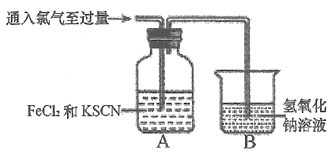
①装置B中发生反应的离子方程式为___________。
②装置A中溶液变红的原因是_________(用离子方程式表示)。
(3)后续实验探究
为了探究上图A装置中溶液红色褪去的原因,该小组取少量A中褪色后的溶液,向其中加入_____(填化学式)后,溶液逐渐恢复为红色,由此得出结论:SCN-被Cl2氧化。
为了探究SCN-被Cl2氧化氧化后的产,该小组又做了如下探究:
①查阅资料,发现SCN-中氮元素为-3价、碳元素为+4价。
②取A中褪色后的溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀。
③通过实验证明了SCN-中氮元素转化为NO3-。
请结合以上实验探究结果写出SCN-与Cl2反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有NaCl、Na2CO3、NaOH的水溶液中,加入过量的稀盐酸,溶液中离子数目不变的是( )
A.Na+B.CO32-C.OH-D.Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化钛是一种重要的工业原料.
(1)实验室可通过以下方法制得:TiCI4 ![]() TiO2xH2O
TiO2xH2O ![]() TiO2TiCl4水解生成TiO2xH2O的化学方程式是;检验TiO2xH2O中Cl﹣是否被除净的方法是 .
TiO2TiCl4水解生成TiO2xH2O的化学方程式是;检验TiO2xH2O中Cl﹣是否被除净的方法是 .
(2)工业上可用含Fe2O3的钛铁矿(主要成分为FeTiO3 , 其中Ti化合价为+4价)制取,其主要流程如下: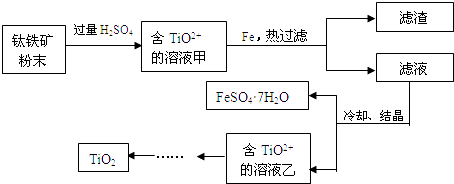
Fe2O3与硫酸反应的离子方程式是;向甲溶液中加入铁的目的是 .
(3)二氧化钛可用于制取金属钛,其步骤如下:TiO2![]() TiCl4
TiCl4![]() Ti反应②的方程式是 , 该反应需要在Ar的气氛中进行,原因是 .
Ti反应②的方程式是 , 该反应需要在Ar的气氛中进行,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两种物质的溶液混合后,能发生离子反应,且溶液的总质量不会发生改变的是( )
A.澄清石灰水和稀盐酸混合
B.小苏打溶液和醋酸混合
C.盐(含有硫酸钠、碳酸氢钠、氯化钠、硫酸钾)溶液与BaCl2溶液混合
D.氯化钠溶液和蔗糖水混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( )
A.盐和盐的反应B.碱性氧化物和水的反应
C.酸与碱的反应D.酸性氧化物和碱的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中有取之不尽的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图:

试回答下列问题:
(1)实验室里将粗盐制成精盐的过程中,过滤的操作需用到玻璃棒,玻璃棒的作用是:____,还需要的玻璃仪器有:____。
(2)粗盐中含有Ca2+、 Mg2+、 SO42-等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中:①加入过量的BaC12溶液,②过量的NaOH溶液,③过量的Na2C03溶液,则添加试剂顺序为____(填写序号),最后在滤液加入盐酸至溶液呈中性。请写出加入盐酸后可能发生反应的离子方程式:____。
(3)海水提取食盐后的母液中有K+、Na+、Mg2+等阳离子。从离子反应的角度考虑,在母液里加入石灰乳发生反应的离子方程式:____。
(4)电解无水氯化镁制取镁的化学方程式为____。将镁蒸气冷却后即为固体镁,镁蒸气需在Ar气氛围中冷却,理由:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半导体工业用石英砂做原料通过三个重要反应生产单质硅:
①SiO2(s)+2C(s)═Si(s)+2CO(g)△H=+682.44kJmol﹣1 ,
(石英砂) (粗硅)
②Si(s)+2Cl2(g)═SiCl4(g)△H=﹣657.01kJmol﹣1
③SiCl4(g)+2Mg(s)═2MgCl2(s)+Si(s)△H=﹣625.63kJmol﹣1
(纯硅)
用石英砂生产1.00kg纯硅的总放热为( )
A.2.43×104 kJ
B.2.35×104 kJ
C.2.23×104 kJ
D.2.14×104 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com