
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是( )
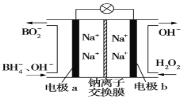
A.电池放电时Na+从b极区移向a极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.每消耗1molH2O2,转移的电子为1mol
D.该电池的正极反应为:BH4-+8OH--8e-=BO2-+6H2O
科目:高中化学 来源: 题型:
【题目】某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)。
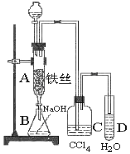
(1)写出A中反应的化学方程式_____。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是____。
(3)C中盛放CCl4的作用是___。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入___,现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:

(1)仪器a的名称为______;仪器b中可选择的试剂为______。
(2)实验室中,利用装置A,还可制取的无色气体是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式______。
(4)E装置中浓硫酸的作用______。
(5)读取气体体积前,应对装置F进行的操作:______。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. NaHS溶液水解的方程式为:HS﹣+H2O![]() S2﹣+H3O+
S2﹣+H3O+
B. 向H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH﹣+18O2↑
C. 在100 mL 2 mol/L FeBr2溶液中通入4.48 L氯气(标况下),充分反应:2Fe2++2Br﹣+2Cl2=2Fe3++Br2+4Cl-
D. 用惰性电极电解饱和氯化钠溶液:2Cl﹣+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )

A.0.1 mol CuOB.0.1 mol CuCO3
C.0.1 mol Cu(OH)2D.0.05 mol Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色固体粉末,由FeCl3、CaCO3、Na2SO4、KCl、Ba(NO3)2中的几种物质组成,取样品进行如下实验(假设下列过程中,能反应的物质之间的反应恰好完全):

(1)步骤①所用分离方法叫做___,要从步骤②所得“无色溶液”中提取溶剂,所用分离方法叫做___。
(2)写出实验过程中发生化学反应的离子方程式①___;②___。
(3)固体粉末中一定不存在的物质是(填化学式,下同)___;不能确定是否存在的物质是___。
(4)将固体粉末可能的组成填入下表(可以不填满,也可以再补充)。___
序号 | 化学式 |
Ⅰ | |
Ⅱ | |
(5)设计一个实验,进一步确定混合物的组成,简述实验操作、现象和结论。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和滴定是高中化学重要的定量实验。请回答下列问题:
(1)用标准盐酸滴定未知浓度的NaOH溶液,下列情况会造成测定结果偏高的是____(填选项字母)。
A.滴定终点读数时,俯视滴定管刻度
B.盛装NaOH溶液的锥形瓶用蒸馏水洗过,未用NaOH溶液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.02mol·L-1的高锰酸钾溶液滴定,发生反应的离子方程式为:____。
(3)一滴定数据如下:
滴定次数 | 待测液体积(mL) | 标准KMnO4溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 3.00 | 23.00 |
第三次 | 25.00 | 4.00 | 24.10 |
①滴定时,该反应速率开始十分缓慢,一段时间后突然加快,这是因为____(填离子)对该反应具有催化作用,KMnO4溶液应装在____(填“酸”或“碱”)式滴定管中;滴定终点的现象是____。
②该草酸溶液的物质的量浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关注饮用水,保证生活质量。请回答下列问题:
(1)饮用水中的![]() 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中![]() 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将![]() 还原为N2,其化学方程式为: 10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
还原为N2,其化学方程式为: 10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
上述反应中,_________元素的化合价升高,则该元素的原子_______(填“得到”或“失去”)电子。当有1mol N2生成时,反应中转移电子的数目为____________。
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳 [Ca(OH)2]制取漂白粉,化学方程式为:__________________。
(3)KA1(SO4)212H2O的俗名为明矾,因其溶于水生成_____________(化学式)可以吸附杂质,从而达到净水作用。向饱和明矾溶液滴加稀氢氧化钠溶液至过量,用离子方程式和必要文字描述过程现象:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
B.含NA个Na+的Na2O溶解于1L水中,所得溶液中Na+的物质的量浓度为1mol·L-1
C.在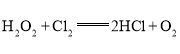 反应中,每生成32g氧气,则转移2NA个电子
反应中,每生成32g氧气,则转移2NA个电子
D.常温下,1L0.50mol·L-1NH4Cl溶液与2L0.25mol·L-1NH4Cl溶液所含![]() 物质的量相同
物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com