
【题目】有一包白色固体粉末,由FeCl3、CaCO3、Na2SO4、KCl、Ba(NO3)2中的几种物质组成,取样品进行如下实验(假设下列过程中,能反应的物质之间的反应恰好完全):

(1)步骤①所用分离方法叫做___,要从步骤②所得“无色溶液”中提取溶剂,所用分离方法叫做___。
(2)写出实验过程中发生化学反应的离子方程式①___;②___。
(3)固体粉末中一定不存在的物质是(填化学式,下同)___;不能确定是否存在的物质是___。
(4)将固体粉末可能的组成填入下表(可以不填满,也可以再补充)。___
序号 | 化学式 |
Ⅰ | |
Ⅱ | |
(5)设计一个实验,进一步确定混合物的组成,简述实验操作、现象和结论。___
【答案】过滤 蒸馏 Ba2++SO42-=BaSO4↓ H++CaCO3=Ca2++CO2↑+H2O CuSO4 KCl
序号 | 化学式 |
I | CaCO3、Na2SO4、Ba(NO3)2 |
II | CaCO3、Na2SO4、Ba(NO3)2、KCl |
用试管取少许步骤①中的“无色溶液”,滴入HNO3酸化,再滴入AgNO3溶液;若有白色沉淀出现,则原白色固体粉末中含有KCl;若无白色沉淀出现,则原白色固体粉末中不含KCl
【解析】
假设这些物质都有,经步骤①得到无色溶液和白色沉淀,说明原粉末中没有FeCl3,在该假设的前提下,白色沉淀是CaCO3、BaSO4,向该沉淀中加入稀硝酸产生无色气体,则说明沉淀中一定有CaCO3,题中告知能反应的物质之间的反应恰好完全,加入稀硝酸之后,沉淀的质量减少,说明还含有BaSO4,则原粉末中有一定有CaCO3、Na2SO4、Ba(NO3)2;KCl不和上述的任何物质反应,也不能通过实验现象去确定其是否存在,故可能有KCl。
(1)经步骤①得到无色溶液和白色沉淀,则该步骤为过滤;要从步骤②所得“无色溶液”中提取溶剂,需要采用蒸馏;
(2)经分析,原粉末中一定有CaCO3、Na2SO4、Ba(NO3)2,则步骤①中的离子方程式为Ba2++SO42-=BaSO4↓;步骤②中,仅CaCO3和HNO3反应,该反应的离子方程式为2H++CaCO3=Ca2++CO2↑+H2O;
(3)经分析,原固体粉末中一定没有CuSO4,不能确定是否存在的是KCl;
(4)由于原固体粉末中一定没有CuSO4,一定有CaCO3、Na2SO4、Ba(NO3)2,可能有KCl,故其组成由两种情况:
序号 | 化学式 |
I | CaCO3、Na2SO4、Ba(NO3)2 |
II | CaCO3、Na2SO4、Ba(NO3)2、KCl |
(5)KCl是唯一可能存在的物质,故只需要鉴定KCl即可,可以用AgNO3溶液检验KCl:用试管取少许步骤①中的“无色溶液”,滴入HNO3酸化,再滴入AgNO3溶液;若有白色沉淀出现,则原白色固体粉末中含有KCl;若无白色沉淀出现,则原白色固体粉末中不含KCl。


科目:高中化学 来源: 题型:
【题目】燃烧8.88g某有机物生成CO2和H2O,将燃烧后的气体通过浓H2SO4,浓H2SO4质量增加10.8g,剩余气体通过NaOH溶液,溶液质量增加21.12g。有机物蒸汽密度为3.3g/L(标准状况)。
(1)通过计算写出有机物的分子式。____
(2)若该物质与金属钠反应能放出H2,写出该有机物可能的结构简式。____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+4B(g)![]() 2C(g)+2D(g),下列数据表示反应进行得最快的是( )
2C(g)+2D(g),下列数据表示反应进行得最快的是( )
A.v(A)=1.4mol/(Ls)B.v(B)=3.6 mol/(Ls)
C.v(C)=2mol/(Ls)D.v(D)=30 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。
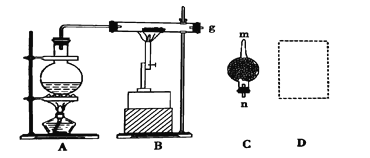
(1)写出铁在高温下与水蒸气反应的化学方程式: _____________________
(2)干燥管C中盛放的药品是________;干燥管的_______(填“m”或“n”)端与g导管相连接。
(3)怎样用简单的方法检验收集到的气体是氢气?简述实验操作步骤和现象:_____
(4)若收集到标准状况下的H2 11.2 L,则参加反应的铁粉的质量为____________g。
(5)当固体质量增加16 g时,生成H2的质量为____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是( )
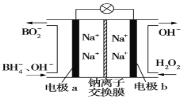
A.电池放电时Na+从b极区移向a极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.每消耗1molH2O2,转移的电子为1mol
D.该电池的正极反应为:BH4-+8OH--8e-=BO2-+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。
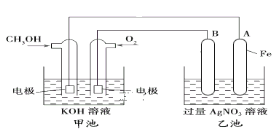
请填空:
(1)充电时,①原电池的负极与电源___极相连。
②阳极的电极反应为____。
(2)放电时:负极的电极反应式为____。
(3)在此过程中若完全反应,乙池中A极的质量增加648 g,则甲池中理论上消耗O2____L(标准状况下)。
(4)若在常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,表示甲醇燃烧热的热化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是无色油状液体沸点为38.4℃,难溶于水,能溶于多种有机溶剂.以NaBr固体、C2H5OH、浓H2SO4、水为原料,对反应后的混合液微热可在烧杯中得到粗产品(溴乙烷),反应装置如图(已略去夹持和加热装置),反应原理:①NaBr+H2SO4(浓)=NaHSO4+HBr;②CH3CH2OH+HBr![]() CH3CH2Br+H2O。下列有关说法正确的是( )
CH3CH2Br+H2O。下列有关说法正确的是( )
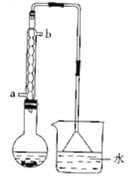
A.烧瓶中试剂加入的先后顺序:浓硫酸、水、溴化钠、乙醇
B.可用 装置代替倒置漏斗装置
装置代替倒置漏斗装置
C.冷凝水从b口进a口出
D.粗产品经水洗涤、蒸发结晶得到纯净的溴乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国稀土资源丰富。下列有关稀土元素![]() 与
与![]() 的说法正确的是( )
的说法正确的是( )
A. ![]() 与
与![]() 的质量数相同
的质量数相同
B. ![]() 与
与![]() 是同一种核素
是同一种核素
C. ![]() 与
与![]() 互为同位素
互为同位素
D. ![]() 与
与![]() 的核外电子数和中子数均为62
的核外电子数和中子数均为62
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是

A. 复分解反应、复分解反应、化合反应、置换反应
B. 中和反应、置换反应、复分解反应、置换反应
C. 复分解反应、复分解反应、置换反应、置换反应
D. 分解反应、复分解反应、置换反应、置换反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com