
【题目】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )

A.0.1 mol CuOB.0.1 mol CuCO3
C.0.1 mol Cu(OH)2D.0.05 mol Cu2(OH)2CO3
【答案】D
【解析】
观察图像中曲线的斜率可知,OP段和PQ段气体的成分不同。由于阳极始终是OH-放电,所以可以推断出,OP段只有阳极产生O2(阴极无气体生成),PQ段阴、阳两极都产生气体。因此,整个过程发生的反应为①2CuSO4+2H2O![]() 2Cu+2H2SO4+O2↑和②2H2O
2Cu+2H2SO4+O2↑和②2H2O![]() H2↑+O2↑。结合图像中转移电子的物质的量,可计算出反应①析出0.1 mol Cu和0.05 mol O2,反应②消耗0.05 mol H2O。根据“出什么加什么,出多少加多少”的原则,欲使溶液恢复到起始状态,应向溶液中加入0.1 mol CuO和0.05 mol H2O。而0.05 mol Cu2(OH)2CO3恰好相当于0.1 mol CuO和0.05 mol H2O(生成0.05 mol CO2无影响),故D正确,故答案为D。
H2↑+O2↑。结合图像中转移电子的物质的量,可计算出反应①析出0.1 mol Cu和0.05 mol O2,反应②消耗0.05 mol H2O。根据“出什么加什么,出多少加多少”的原则,欲使溶液恢复到起始状态,应向溶液中加入0.1 mol CuO和0.05 mol H2O。而0.05 mol Cu2(OH)2CO3恰好相当于0.1 mol CuO和0.05 mol H2O(生成0.05 mol CO2无影响),故D正确,故答案为D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.下表是A、B两种有机物的有关信息:
A | B |
①分子填充模型为: ②能使溴的四氯化碳溶液褪色; ③其产量是衡量石油化工水平的标志。 | ①由C、H、O三种元素组成,是厨房中的常见调味剂; ②水溶液能使紫色石蕊试液变红。 |
根据表中信息回答下列问题:
(1)关于A的下列说法中,不正确的是____(填标号)。
a.分子里含有碳碳双键 b.分子里所有的原子共平面 c.结构简式为CH2CH2
(2)A与氢气发生加成反应后生成物质C,与C在分子组成和结构上相似的有机物有一大类,它们的通式为CnH2n+2。当n=___时,这类有机物开始出现同分异构体。
(3)B与乙醇反应的化学方程式为___,反应类型为____。
Ⅱ.糖类、油脂和蛋白质是人体需要的重要营养素。
(4)下列说法正确的是____(填标号)。
a.糖类、油脂、蛋白质都是仅由C、H、O三种元素组成的
b.糖类、油脂、蛋白质都是高分子化合物
c.油脂有油和脂肪之分,都属于酯
(5)淀粉和纤维素的化学式都是(C6H10O5)n,它们____(填“是”或“不是”)同分异构体,淀粉水解的最终产物是____(写名称)。
(6)重金属盐能使人体中毒,这是由于它使人体内的蛋白质发生了____(填“盐析”或“变性”)作用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.硅酸钠溶液与盐酸反应![]() +2HCl=2Cl-+ H2O+SiO2↓
+2HCl=2Cl-+ H2O+SiO2↓
B.水玻璃中通入过量二氧化碳![]() +CO2+H2O=
+CO2+H2O=![]() +H2SiO3↓
+H2SiO3↓
C.硅酸与氢氧化钠溶液反应H2SiO3+ OH-=![]() + H2O
+ H2O
D.SiO2与氢氧化钠溶液反应SiO2+2OH-=![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的反应式为LixC6+Li1﹣xCoO2![]() 6C+LiCoO2(x<1)其工作原理如图所示。下列说法不正确的是( )
6C+LiCoO2(x<1)其工作原理如图所示。下列说法不正确的是( )

A.放电时A极电极式为:LixC6–xe-=6C+xLi+
B.放电时,若转移0.3mol电子,石墨电极将减重2.1g
C.充电时,A极接外电源的正极
D.该废旧电池进行“放电处理”有利于锂在B极回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置说法正确的是( )
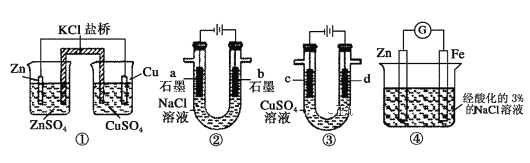
A.装置①中,一段时间后CuSO4浓度增大
B.装置②中滴入酚酞,a极附近变红
C.用装置③精炼铜时,c极为粗铜
D.装置④中发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是( )
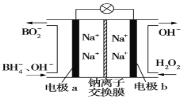
A.电池放电时Na+从b极区移向a极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.每消耗1molH2O2,转移的电子为1mol
D.该电池的正极反应为:BH4-+8OH--8e-=BO2-+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
A.m=2
B.达平衡时,Z的体积分数为10%
C.达平衡后,保持容器体积不变,加热,容器内压强将增大
D.将平衡后的容器体积压缩至1L,X的浓度为0.45mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含(NH4)2SO4和K2SO4的混合溶液100mL,向其中滴加足量的Ba(OH)2溶液,加热,充分反应,生成的气体在标准状况下体积为448 mL,将反应后的溶液过滤得白色沉淀4.66 g。求原混合溶液中K2SO4的物质的量浓度________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
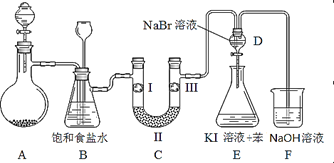
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:_____________。装置B中饱和食盐水的作用是_____________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 _____________________________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入_______。(填字母序号)
a | b | c | d | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为__________色,说明_________________________。
打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是 _______________,写出反应的化学方程式是_________________________。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com