
����Ŀ����ͼ����ѧ��ѧ�г������ʵ�ת����ϵ���������ʺͷ�Ӧ������ȥ��
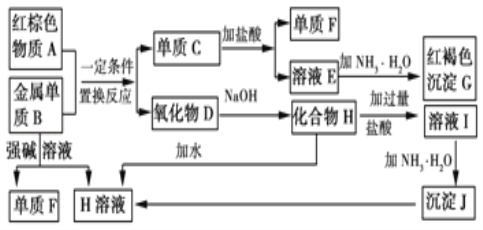
��ش��������⣺
(1)����A�Ļ�ѧʽΪ_____��
(2)д������B��ǿ����Һ��Ӧ�����ӷ���ʽ_____��������D��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ_____��
(3)��ҺE�м��백ˮʱ�������ɰ�ɫ����L��L���ձ�Ϊ���ɫ����G��д��L��ΪG�Ļ�ѧ��Ӧ����ʽ_____��
(4)��ҺE���ڷ������ױ��ʣ�д��������ҺE�Ƿ���ʵ�ʵ�������������_____��Ϊ�˷�ֹ��ҺE�ı��ʣ�������Һ�м���_____�������ӷ���ʽ˵��______________
(5) ��3.06 g����þ�Ļ�����ĩ����100 mL������,ǡ����ȫ��Ӧ,���õ���״����3.36 L H2����úϽ����������ʵ���_____,��Ӧ����Һ��Cl-�����ʵ���Ũ��_____(�ٶ���Ӧ�����Ϊ100 mL)
���𰸡� Fe2O3 2Al+2OH��+2H2O�T2AlO2��+3H2�� Al2O3+2NaOH�T2NaAlO2+H2O 4Fe��OH��2+O2+2H2O�T4Fe��OH��3 ȡ��ҺE�������Թ��У��μӼ���KSCN��Һ������Һ���ɫ��֤����ҺE�Ѿ����� ���� 2Fe3++Fe=3Fe2+ 0.06 mol 3.0 mol��L-1
��������
���ɫ����G����������������ת����ϵ��֪������C��Fe������F����������ҺE���Ȼ������������ɫ����A��Fe2O3������B���������Ʒ�Ӧ�ų���������B��������ҺH��ƫ�����ƣ������������������ȷ�Ӧ����������������D����������ƫ�����������ᷴӦ�����Ȼ�������ҺI���Ȼ���������J������������
�������Ϸ�����(1)����ɫ����A������������ѧʽΪFe2O3��
(2)����B��������ǿ����Һ��Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽ��2Al+2OH��+2H2O�T2AlO2��+3H2����������D������������������NaOH��Һ��Ӧ����ƫ�����ƣ���ѧ����ʽ��Al2O3+2NaOH�T2NaAlO2+H2O��
(3)�������ᷴӦ�����Ȼ���������������ҺE���Ȼ��������Ȼ�������Һ�м��백ˮʱ������������������������������������Ϊ������������Ӧ�Ļ�ѧ��Ӧ����ʽ��4Fe(OH)2+O2+2H2O�T4Fe(OH)3��
(4)�Ȼ��������ڷ������ױ���������Fe3+��Fe3+��KSCN��Һ��ΪѪ��ɫ��������Һ�Ȼ������Ƿ���ʵ�ʵ�������������Ϊ��ȡ��ҺE�������Թ��У��μӼ���KSCN��Һ������Һ���ɫ��֤����ҺE�Ѿ����ʡ��������ܰ�Fe3+��ԭΪFe2+��Ϊ�˷�ֹ��ҺE�ı��ʣ�������Һ�м������ۣ���Ӧ�����ӷ���ʽ��2Fe3++Fe=3Fe2+��
(5) ����þ�ֱ������ᷴӦ�Ļ�ѧ����ʽ��2Al+6HCl==2AlCl3+3H2����Mg+2HCl==MgCl2+H2����
������þ�����ʵ����ֱ���xmol��ymol���� ��
��![]() �����ԸúϽ����������ʵ�����0.06 mol�����ݵ���غ㣬n(Cl-)= 3n(Al 3+)+ 2n(Mg2 +)=3��0.06 mol+2��0.06 mol=0.3mol�����ʵ�����Cl-�����ʵ���Ũ����0.3mol��0.1L=3.0 mol��L-1��
�����ԸúϽ����������ʵ�����0.06 mol�����ݵ���غ㣬n(Cl-)= 3n(Al 3+)+ 2n(Mg2 +)=3��0.06 mol+2��0.06 mol=0.3mol�����ʵ�����Cl-�����ʵ���Ũ����0.3mol��0.1L=3.0 mol��L-1��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д� Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A(s)��3B(g)![]() 2C(g)��D(g)��2 min B��Ũ�ȼ���0.6 mol��L��1�������й�˵����ȷ����
2C(g)��D(g)��2 min B��Ũ�ȼ���0.6 mol��L��1�������й�˵����ȷ����
����A��ʾ�ķ�Ӧ������0.4 mol��L��1��min��1
����2 minĩʱ����Ӧ��B�ķ�Ӧ������0.3 mol��L��1��min��1
������2 min����C��ʾ��ƽ������Ϊ0.2 mol��L��1��min��1
����2 minʱ��B��C��D��Ũ�ȱ�һ��Ϊ3��2��1
����D����ʼŨ��Ϊ0.1 mol��L��1����2 minʱD��Ũ��Ϊ0.3 mol��L��1
A. �٢ڢ�B. �ڢ�C. �ܢ�D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Na2SO4����������480mL0.2mol��L-1��Na2SO4��Һ���ɹ�ѡ���������ͼ��
��1����ͼ��ʾ��������������Һ����Ҫ����__ (��ѡ��)������������Һ�����õ��IJ���������___��__ (����������)��
��2��ʹ������ƿ֮ǰ������еIJ�����___��(��ѡ��)
A.��������� B.����Ƿ�©ˮ C.���
��3�������㣬��Na2SO4������Ϊ___g��
��4����ѡ�õ�����ƿ���Ϊ___mL��
��5��������Һʱ��һ��ɷ�Ϊ���¼������裺
�ٳ��� �ڼ��� ���ܽ� ��ҡ�� ��ת�� ��ϴ�� �߶���
�����˳����__��__��__��__��__��__(�����)��___
��6�������ƹ����У�����������ȷ������ʱ���ӿ̶���ʹ������ҺŨ��__(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ672 mL����ƿ�г���NO��NO2�Ļ�����壬���䵹����ˮ���ȥ������ͨ��280 mL������ǡ����ȫ��Ӧ����Һ�������ƿ(������������ۺ�Ϊ��״���µ����)�������й�������ȷ����(����)
A. �ܷ�ӦΪNO��NO2��O2��H2O===2HNO3
B. �ܷ�ӦΪ4NO��8NO2��5O2��6H2O===12HNO3
C. ������������ʵ���Ũ�Ⱦ�Ϊ0.030 mol��L��1
D. ������������ʵ���Ũ��ԼΪ0.060 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2009��10��1�գ��ҹ��ɹ��ٰ������ʮ���ı���������ı���ʽ��9���綯�����϶�����������Դ���������࣬չʾ���ۺϹ����������Ƽ���չˮƽ��ͬʱҲ˵����Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��Ӧ�� CO(g) �� 2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��Ӧ�� CO2(g) �� 3H2(g)![]() CH3OH(g) + H2O(g) ��H2
CH3OH(g) + H2O(g) ��H2
��������Ӧ������ԭ�Ӿ�����ԭ����� _____����������������������
���±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶� | 250�� | 300�� | 350�� |
K | 2.041 | 0.270 | 0.012 |
�ɱ��������ж���H1 0 ������������������������������
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c(CO)�� 0.2 mol/L����CO��ת����Ϊ ����ʱ���¶�Ϊ �����ϱ���ѡ��
��2����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H1����1275.6 kJ/mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H2����566.0 kJ/mol
�� H2O(g) �� H2O(l) ��H3����44.0 kJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ����
�������ͼ��ʾ�ĵ��װ�á��õ�������ĵ缫��ӦΪ ��

�ڹ���һ��ʱ������Һ��pH��С���õ���ܷ�Ӧ�Ļ�ѧ����ʽΪ
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ƴ���Ư����ɱ���������������������Ʊ��治���������տ�����CO2�����ʡ�
(1)ij����С����̽��ij����������Ʒ�Ƿ��Ѿ����ʣ�ȡ������Ʒ���ܽ⣬����_______________��Һ��������а�ɫ������֤��Na2O2�Ѿ����ʡ�
(2)�ÿ���С��Ϊ�˴��Բⶨ�������ƵĴ��ȣ����dz�ȡag��Ʒ�����������ͼװ�� ���ⶨ�������Ƶ�����������

��A�з�����Ӧ���ӷ���ʽΪ___________________
�ڽ��������Ӻ��Ժ�����еĵ�һ��������__________
��д��װ��C�з��������з�Ӧ�Ļ�ѧ����ʽ______________________________��_______________________________________________________
��D��NaOH��Һ������__________________________
�ݶ�����Ͳ��ˮ�����������ɱ�״�������������ΪVmL������Ʒ�й������Ƶ������� ��Ϊ__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ƣ�Na2S2O4���׳Ʊ��շۣ��ױ�����������������ͼװ�ã�����ƿ�м���HCOONa��NaOH��CH3OH��ˮ�γɵĻ��Һ��ͨ��SO2ʱ������Ӧ���ɱ��շۺ�һ�ֳ������壬����˵���������
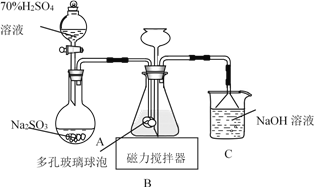
A. �Ʊ����շ۵����ӷ���ʽΪHCOO����OH����2SO2===S2O42����CO2����H2O
B. NaOH��Һ����Ҫ�����������ݳ���CO2
C. ��ײ������ݵ�������������������Һ�ĽӴ������ʹSO2�ܱ��������
D. Ϊ���������Na2S2O4��O2������ʹ���������������ȷ�Ӧ��������SO2�ų�װ���в�����O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̫��ˮ�����װ����ͼ��ʾ���õ���������缫��ɣ�����aΪTiO2�缫��bΪPt�缫��cΪWO3�缫���������ҺΪpH=3��Li2SO4-H2SO4��Һ������ӽ���Ĥ����ط�ΪA��B��������A����� ����ͨ��B��Ϊ�����ϵ����N2���������й��ڸõ�ص�˵��������ǣ� ��
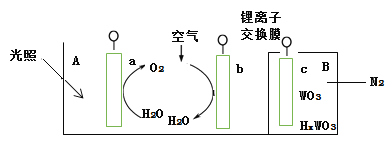
A.���õ�������a��c,��aΪ�������õ缫����pH��С
B.���õ�������a��c,��c�缫�ĵ缫��ӦʽΪHxWO3 - xe- =WO3 + xH+
C.���õ���������a��c,������b��c,��ʵ��̫���������ת��
D.���õ�������b��c, b�缫�ĵ缫��ӦʽΪO2+4H++4e-=2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X����Һ�У�����Y�Լ��������ij��������������ͼ��ʾ�����������������������

A. ��HCl��AlCl3�Ļ��Һ�еμ�NaOH��Һ
B. ��NaOH��Ca(OH)2�Ļ��Һ��ͨ��CO2
C. ��NH4Al(SO4)2��Һ�еμ�NaOH��Һ
D. ��NaOH��Na2CO3�Ļ��Һ�еμ�ϡ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com