
【题目】某同学在画某种元素的一种单核微粒的结构的示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
![]()
(1)该微粒是中性微粒,这种微粒的符号是
(2)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,该单质与水反应的化学方程式:
(3)该微粒的还原性很弱,失去2个电子后变成原子,该元素在周期表中的位置为
(4))该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,该单质与水反应的化学方程式 .
(5)该微粒的符号为X3﹣,则这种微粒的单质的电子式为 .
【答案】(1)Ne;
(2)2F2+2H2O═4HF+O2;
(3)第二周期第VIA族;
(4)2Na+2H2O═2Na++2OH﹣+H2↑;
(5)![]() .
.
【解析】试题分析:(1)该微粒是中性微粒,质子数10,为Ne原子;
(2)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,则原子质子数为2+8﹣1=9,为F﹣离子,其单质氟气与水反应生成HF与氧气;
(3)该微粒的还原性很弱,失去2个电子后变成原子,据此可知该原子的核外有8个电子;
(4)该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,则原子质子数为2+8+1=11,为Na+离子,其单质Na与水反应生成氢氧化钠与氢气;
(5)该微粒的符号为X3﹣,则该微粒所对应的原子的核外有7个电子,即氮原子,则对应的单质为氮气,分析其电子式.
解:(1)该微粒是中性微粒,则为Ne原子,故答案为:Ne;
(2)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,则原子质子数为2+8﹣1=9,为F﹣离子,其单质氟气与水反应生成HF与氧气,反应方程式为:2F2+2H2O=4HF+O2,故答案为:2F2+2H2O═4HF+O2;
(3)该微粒的还原性很弱,失去2个电子后变成原子,据此可知该原子的核外有8个电子,即为氧原子,则在周期表中的位置为第二周期第VIA族,故答案为:第二周期第VIA族;
(4)该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,则原子质子数为2+8+1=11,为Na+离子,其单质Na与水反应生成氢氧化钠与氢气,反应方程式为:2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O═2Na++2OH﹣+H2↑;
(5)该微粒的符号为X3﹣,则该微粒所对应的原子的核外有7个电子,即氮原子,则对应的单质为氮气,氮气的电子式为![]() ,故答案为:
,故答案为:![]() .
.


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:制备溴乙烷的的一种方法是乙醇与氢溴酸反应,该反应的化学方程式为:CH3CH2OH+HBr![]() CH3CH2Br+H2O。
CH3CH2Br+H2O。
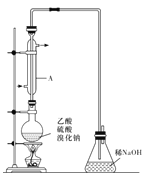
I.实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写正确选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
II.溴乙烷的性质实验
(4)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是 。通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液
(5)溴乙烷与NaOH乙醇溶液共热可产生乙烯气体。在进行该实验时,把生成的气体通过右图所示的装置。用该装置进行实验的目的是检验乙烯的生成,该图中右侧试管中的现象是______________;左侧试管中水的作用是___________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他产物已略去):
![]()
(1)若A、D的水溶液均呈酸性,且D为强酸.
①A、D分别为A: ,D: .(填写化学式,下同)
②写出B→C转化的化学方程式: .
③简述检验B物质的方法 .
④写出D的浓溶液和Cu在加热条件的化学方程式 .21*cnjy*com
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.
①工业上合成A的化学方程式: .在实验室中则用加热固体混合物的方法制取气体A,其化学方程式为 .
②写出C→D的化学方程式,并用双线桥标出电子转移的方向和数目.
③写出A→B的化学方程式
④1.92g铜投入一定的D浓溶液中,铜完全溶解,共收集到672mL气体(标准状况).将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为 mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的描述和相关知识均正确的是
物质及变化 | 描述 | 相关知识 | |
A | 碘化钾溶液滴到土豆片上 | 变蓝色 | 土豆片含淀粉 |
B | 煤的气化 | 化学变化 | 主要反应是碳与水生成水煤气等 |
C | 乙烯和苯 | 都能使溴水褪色 | 分子中含有相同的碳碳双键 |
D | 蔗糖和麦芽糖 | 多糖 | 二者互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯酚的化学式是C6H6O,是一种有毒的物质,对皮肤、黏膜有强烈的腐蚀作用.2014年6月,一辆载有近30吨苯酚的槽罐车侧翻,约有10吨的苯酚泄漏,造成很大程度的污染.
(1)你认为下列对事故的处理方法合理的是 .
A、用碱性溶液冲洗可以减少苯酚的挥发
B、挖隔离沟、铺膜防止扩散并回收泄漏的苯酚
C、随时监测附近水源、土壤中的苯酚的含量
D、用水溶解后回收
(2)用木屑吸附残余的苯酚,然后点火燃烧除去.写出苯酚在空气中完全燃烧的化学方程式: .
(3)如图是从苯酚的乙醇溶液中分离回收苯酚的操作流程图:

根据图示完成下列问题:
①试剂A的化学式为 .
②步骤③的操作名称为 .
③写出C+D﹣→E+C6H5OH的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中各化学键如图所示对乙醇在各种反应中应断裂的键说明不正确的是( )
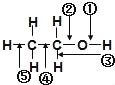
A.和金属钠作用时,键②断裂
B.和浓硫酸共热至170℃时,键②和⑤断裂
C.和HBr共热时,键④断裂
D.在铜催化下和氧气反应时,键①和③断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空:
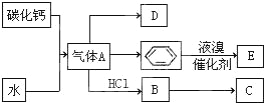
(1)写出A的电子式 ;D的最简式为 .
(2)写出碳化钙与水反应制取A的化学方程式 .
(3)苯和液溴反应生成E的化学方程式 ,其反应类型为 .
(4)D还可以用石蜡油制取,工业上由石油获得汽油、煤油、石蜡油等成份的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.离子化合物的熔点一定比共价化合物熔点高
B.甲烷的标准燃烧热为890.3KJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
C.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g) ![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的△H相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤干馏的产品经加工可得到下列有机物:①甲烷、②乙烯、③苯.其中,可作清洁燃料的是 (填序号,下同),可作植物生长调节剂的是 ,可作有机溶剂的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com