
【题目】某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)配制待测液,用5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液。除烧杯、量筒和胶头滴管外,还需要的玻璃仪器有__________、__________。
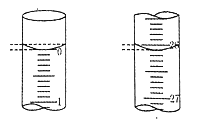
(2)滴定:用标准的盐酸溶液滴定待测的氢氧化钠溶液时,达到滴定终点的判断依据是:__________,若滴定开始和结束时,酸式滴定管中的液面如图所示,则终点读数_________mL。
(3)数据处理,某学生根据三次实验分别记录有关数据如下:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.31 |
则该氢氧化钠溶液的物质的量浓度c(NaOH)=___________。(保留三位有效数字)
(4)若改用含Na2O杂质的NaOH配制成标准溶液来滴定盐酸,测得的盐酸浓度将________。(选填“偏高”、“偏低”或“无影响”)
【答案】1000mL容量瓶 玻璃棒 滴入最后一滴盐酸时,溶液由红色变为无色,并且半分钟之内不恢复红色,说明达到滴定终点 26.10 0.104molL-1 偏低
【解析】
(1)配制1000mL溶液,需要1000mL的容量瓶,引流时还需要用到玻璃棒,所以配制溶液时,除烧杯、量筒和胶头滴管外,还需要的玻璃仪器有1000mL容量瓶和玻璃棒。
(2)该中和滴定用酚酞做指示剂,所以当滴入最后一滴盐酸时,溶液由红色变为无色,并且半分钟之内不恢复红色,说明达到滴定终点;读数时,视线与滴定管内凹液面最低点相平,读到0.01mL,起始读数为0.00mL,终点读数为26.10mL,所以终点读数为26.10 mL。
(3)三次消耗的盐酸的体积分别为 26.11mL,28.74mL,26.09mL,第二次数据误差过大,舍去;另外两次的平均值为(26.11+26.09)mL÷2=26.10mL,c(NaOH)=(0.1000mol/L×0.0261L)÷0.025L=0.104(mol/L)。
(4)若含Na2O杂质,根据反应Na2O+2HCl=2NaCl+H2O,该反应31g消耗1mol盐酸,而NaOH+HCl=NaCl+H2O,该反应40g消耗1mol杂质,导致消耗的标准液体积减小,测定结果偏低。


科目:高中化学 来源: 题型:
【题目】印刷电路板(PCB)是用腐蚀液(FeCl3溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB并将腐蚀后废液(其中金属阳离子主要含Fe3+、Cu2+、Fe2+)回收再生的流程如图。
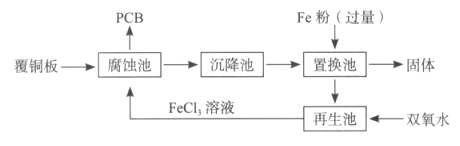
请回答:
(1)腐蚀池中发生反应的化学方程式是__。
(2)上述各池中,没有发生化学变化的是__池。
(3)由置换池中得到固体的操作名称是__。
(4)置换池中发生反应的离子方程式有__。
(5)请提出利用酸从固体中回收Cu并将滤液回收利用的合理方案:__。
(6)向再生池中通入Cl2也可以使废液再生,相比Cl2,用双氧水的优点是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液电导率越大导电能力越强。常温下用0.100 mol·L-1盐酸分别滴定10.00 mL浓度均为0.100 mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温Kb[(CH3)2NH·H2O]=1.6×10-4]。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是( )
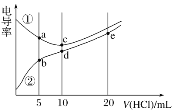
A.曲线②代表滴定二甲胺溶液的曲线
B.b点溶液中:pH<7
C.d点溶液中:c(H+)=c(OH-)+c[(CH3)2NH·H2O]
D.c、d、e三点的溶液中,水的电离程度最大的是d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示的分子,下列叙述正确的是( )

A.除苯环外的其余碳原子有可能在一条直线上
B.1mol该物质与足量溴水反应,最多消耗5molBr2
C.1mol该物质完全燃烧消耗16molO2
D.该分子最多有22个原子在同一平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用活性炭还原法可以处理氮氧化物。如反应:![]()
![]() 。在
。在![]() 时,反应进行到不同时间测得各物质的浓度如下:
时,反应进行到不同时间测得各物质的浓度如下:
0 | 10 | 20 | 30 | 40 | 50 | |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
(1)T1℃时,该反应的平衡常数![]() ______
______
(2)30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 ______ ![]() 答一种即可
答一种即可![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不当的是
A.实验室制取少量蒸馏水时,不需要使用温度计
B.实验室制取少量的![]() 时,为防止其被氧化,应将吸NaOH溶液的胶头滴管插入
时,为防止其被氧化,应将吸NaOH溶液的胶头滴管插入![]() 溶液中
溶液中
C.防止浓![]() 在光照条件下变色,应将浓
在光照条件下变色,应将浓![]() 保存在棕色试剂瓶中
保存在棕色试剂瓶中
D.通常酒精灯中加入酒精的体积不超过酒精灯容积的三分之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项有机物同分异构体的数目,与分子式为C4H8O2的酯的有机物数目相同的是( )
A.分子式为C4H8的烯烃(包括顺反异构体)
B.分子式为C8H8O遇FeCl3溶液显紫色
C.分子式为ClC4H7O2,且能与碳酸氢钠反应生成气体
D.立方烷(![]() )的二氯代物
)的二氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
A.已知2C(s)+2O2(g)=2CO2(g) ΔH=a kJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=b kJ·mol-1,则a>b
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH= -57.3 kJ·mol-1,则含1mol NaOH的稀溶液与足量稀醋酸完全中和,放出的热量等于57.3kJ
C.已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定
D.已知H2(g)+I2(g)![]() 2HI(g) ΔH= -a kJ·mol-1向密闭容器中加入2mol H2和2mol I2(g),充分反应后放出的热量小于2a kJ
2HI(g) ΔH= -a kJ·mol-1向密闭容器中加入2mol H2和2mol I2(g),充分反应后放出的热量小于2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.金属铁原子核外电子运动状态有26种
B.金刚石晶胞中原子的体积占晶胞体积的百分率表达式为![]() π×100%
π×100%
C.从原子轨道重叠方式考虑,氮气分子中的共价键类型有σ键和π键
D.HCN分子的空间构型为直线形
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com