
将质量为2.3g钠用刺了孔的铝箔包裹后放入水中,共收集到2.464L(标准状况)气体.请回答下列问题:
(1)2.3g钠与水反应,理论上生成气体的体积(标准状况)为多少.
(2)反应后溶液的体积为100mL,则混合溶液中NaOH的物质的量浓度为多少?
| 钠的化学性质;化学方程式的有关计算;铝的化学性质.. | |
| 专题: | 几种重要的金属及其化合物. |
| 分析: | (1)根据钠与水的关系式计算; (2)氢气的总体积减去钠与水反应生成氢气的体积就是铝与氢氧化钠反应生成的氢气体积,根据铝与氢氧化钠反应生成的氢气体积计算消耗的氢氧化钠的物质的量,钠与水反应计算生成的氢氧化钠的物质的量减去铝与氢氧化钠反应的物质的量就是剩余的氢氧化钠的物质的量,根据浓度公式计算其浓度. |
| 解答: | 解:(1)设生成氢气的体积为xL, 2Na+2H2O=2NaOH+H2↑ 46g 22.4L 2.3g xL x=1.12 答:理论上生成气体的体积为1.12L; (2)2Na+2H2O=2NaOH+H2↑ 46 2mol 2.3g 0.1mol 钠与水反应生成的氢氧化钠的物质的量为0.1mol,生成氢气1.12L.所以铝与氢氧化钠反应生成的氢气体积为2.464L﹣1.12L=1.344L 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 2mol 2mol (3×22.4 )L 0.04mol 0.04mol 1.344L 与铝反应的氢氧化钠的物质的量为0.04mol,所以剩余氢氧化钠0.1mol﹣0.04mo=0.06mol,故氢氧化钠的物质的量浓度= 答:混合溶液中NaOH的物质的量浓度为0.6mol/L. |
| 点评: | 本题以钠、铝的化学反应为载体考查了化学计算,计算时要注意氢气的来源,不仅包括钠与水反应生成的氢气,还包括铝和氢氧化钠反应生成的氢气. |


科目:高中化学 来源: 题型:
在2A+B 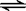 3C+4D中,表示该反应速率最快的是( )
3C+4D中,表示该反应速率最快的是( )
A.υ(A) = 0.5mol·L-1·S-1 B.υ(B) = 0.3 mol·L-1·S-1
C.υ(C) = 0.8mol·L-1·S-1 D.υ(D)= 1 mol·L-1·S-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | FeCl3 溶液与铁反应:Fe+Fe3+═2Fe2+ |
|
| B. | 向Ca(HCO3)2溶液中加入足量NaOH溶液:Ca2++HCO3﹣+OH﹣=CaCO3↓+H2O |
|
| C. | 铝粉溶于NaOH溶液中:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑ |
|
| D. | 金属钠跟水反应Na+2H2O═Na++OH﹣+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
向硫酸铜溶液中加入一小块金属钠后,观察到的现象有( )
①钠浮于液面上
②熔化成小球
③发出嘶嘶的响声,放出气体
④钠周围蓝色沉淀部分变黑
⑤有蓝色沉淀产生
⑥析出大量红色的铜
⑦小球在溶液中沉浮
⑧小球在液面上游动、逐渐变小,直至消失.
|
| A. | ①②③④⑤⑥ | B. | ①②③④⑤⑧ | C. | ①②③⑥⑧ | D. | ②⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一次化学研究性学习实验中,某研究小组学生,研究分析某两瓶无标签的试剂,只知道一瓶是固体,另一瓶是液体,取少量两种试剂在试管中混合,立即产生一种无色无味的气体.现请你对此气体开展一系列探究,并完成下列实验报告.
(1)①此气体是什么物质(只写出其中可能的一种)?验证它的实验方案如下:
| 猜想 | 实验步骤 | 现象及结论 |
| 此气体可能是 氧气 | 将带火星的木条伸入集气瓶中 | __ 木条复燃,则证明是氧气 |
产生此气体的化学方程式可能是 2H2O2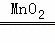 2H2O+O2↑
2H2O+O2↑
②想制取该气体(用本题中两瓶无标签的试剂),采用的发生装置可选用下图A、B、C中的 B (对应填序号).
收集该气体可选用D中的 b 装置.
③若图E是收集该气体的装置,气体由 a 端(填“a”或“b”)导入.
(2)猜想此无色气体还有无可能是另一种气体,如果有,请写出产生它的化学方程式 CaCO3+2HCl=CaCl2+H2O+CO2↑ (只须写一种).

查看答案和解析>>
科目:高中化学 来源: 题型:
理论上不能用于设计成原电池的反应是
A. 2H2(g)+O2(g)==2H2O(l) △H<0 B. HCl(aq)+NaOH(aq)==NaCl(aq)+H2O(l) △H<0
C. 2Al(s)+3Cl2(g)==2AlCl3(s) △H<0 D. Zn(s)+2HCl(aq)==ZnCl2+H2(g) △H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸盐在能源、环境保护等有着广泛的用途,可以用电解法制高铁酸盐(已知高铁酸盐在酸性条件下不稳定),总反应式为Fe+2H2O+2OH-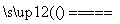 3H2↑+FeO
3H2↑+FeO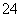 。下列说法正确的是
。下列说法正确的是
A.铁为阳极,H2SO4为电解液 B.铁为阴极,浓NaOH为电解液
C.阳极发生的电极反应为Fe+8OH--6e-===4H2O+FeO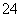
D.铁失去3 mol电子可以在阴极得到33.6 L氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 溴乙烷与氢氧化钠溶液共热后加入硝酸银溶液 | 无浅黄色沉淀出现 | 溴乙烷未水解 |
| B | 向某溶液中先滴加氯水,再滴加少量KSCN溶液。 | 溶液变成血红色 | 溶液中含有Fe2+ |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
| D | 向盛有碘水的试管中加入CCl4后充分振荡静置 | 液体分层,上层基本无色,下层紫红色 | 碘在CCl4中的溶解度较大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
若20 g密度为ρ g·cm-3的硝酸钙溶液里含1 g Ca2+,则NO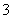 的物质的量浓度是( )
的物质的量浓度是( )
A.ρ/400 mol·L-1 B.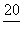 mol·L-1
mol·L-1
C.2.5ρ mol·L-1 D.1.25ρ mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com