
������������Դ���������������Ź㷺����;�������õ�ⷨ�Ƹ�������(��֪�������������������²��ȶ�)���ܷ�ӦʽΪFe��2H2O��2OH��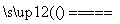 3H2����FeO
3H2����FeO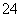 ������˵����ȷ����
������˵����ȷ����
A����Ϊ������H2SO4Ϊ���Һ B����Ϊ������ŨNaOHΪ���Һ
C�����������ĵ缫��ӦΪFe��8OH����6e��===4H2O��FeO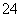
D����ʧȥ3 mol���ӿ����������õ�33.6 L����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£������������ǿ��淴ӦA(g)+3B(g) 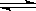 2C(g)�ﵽƽ��ı�־���� �� ��
2C(g)�ﵽƽ��ı�־���� �� ��
��1��C������������C�ķֽ�������ȣ���2����λʱ����amol A���ɣ�ͬʱ����3amol B��
��3��A��B��C��Ũ�Ȳ��ٱ仯����4������������ѹǿ���ٱ仯����5�������������ʵ������ٱ仯����6����λʱ������amol A��ͬʱ����3amol B����7��A ��B��C�ķ�����Ŀ��Ϊ1:3:2��
A.��2����5�� B.��1����3�� C.��2����7�� D.��5����6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ˮ��Һ�еĸ���������Ϊ����������ԭ��Ӧ�����ܴ���������ǣ�������
| �� | A�� | Na+��Ba2+��Cl����SO | B�� | Ca2+��HCO |
| �� | C�� | MnO4����K+��I����H+ | D�� | H+��Cl����Na+��CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Ϊ2.3g���ô��˿��������������ˮ�У����ռ���2.464L����״�������壮��ش��������⣺
��1��2.3g����ˮ��Ӧ������������������������״����Ϊ���٣�
��2����Ӧ����Һ�����Ϊ100mL��������Һ��NaOH�����ʵ���Ũ��Ϊ���٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ò��缫���ij��Һһ��ʱ�䣬����ҺŨ�������pH��С������Һ��
�� A NaOH���� B CuCl2������ C CuSO4������ D H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݵ���������Ӧ���Ȼ�ѧ����ʽ (i) I2 (g)+ H2(g)  2HI(g) ��H=-9.48 kJ/mol
2HI(g) ��H=-9.48 kJ/mol
(ii) I2(S)+ H2(g) 2HI(g) ��H=+26.48 kJ/mol. �����ж���ȷ����
2HI(g) ��H=+26.48 kJ/mol. �����ж���ȷ����
A��254g I2(g)��ͨ��2gH2(g)����Ӧ����9.48 kJ
B��1 mol��̬����1 mol��̬���������������17.00 kJ
C����Ӧ(i)�IJ���ȷ�Ӧ(ii)�IJ����ȶ�
D����Ӧ(ii)�ķ�Ӧ���������ȷ�Ӧ(i)�ķ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
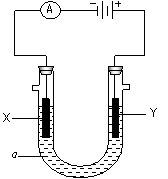 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
��X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
������X���ϵĵ缫��ӦʽΪ
��
��X�������۲쵽�������� ����
��Y�缫�ϵĵ缫��ӦʽΪ ��
����õ缫��Ӧ����ķ����� ��
��2����Ҫ��ij�������ϱ����һ�����ͭ����
��X�缫�IJ����� ���缫��Ӧʽ�� ��
��Y�缫�IJ����� �����Һaѡ�� ��Һ����
����˵�������ʷ����ĵ缫��Ӧ����д����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ж�һЩ��ʵ�����۽�����ȷ����(����)
| ѡ�� | ����ʵ | ���۽��� |
| A | Na����Naԭ���ȶ� | Na��������Ӳ���8�����Ӷ�Naֻ��1�� |
| B | �ۻ�״̬��NaCl�ܵ����NaCl���岻�ܵ��� | �ۻ�״̬�µ�NaCl�д������Ӷ�NaCl������û������ |
| C | ��ԭ�ӱ���ԭ�Ӹ���ʧȥ���� | �صĺ˵�������ƵĶ� |
| D | ������Һ��ʹʪ�����ɫʯ����ֽ����ɫ | �����ܵ����OH����ʹʯ����ֽ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���д�ʩ�����Ͻ��ܼ��ŵ���( )
A��������չ�������磬���������������
B�����ݶ���װ̫������ˮ��Ϊ�����ṩ��������ˮ
C����ʯ�Ҷ�úȼ�պ��γɵ�������������ʯ��
D�����Ӳݡ������������л�������Ͳ�������������ͥȼ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com