
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 溴乙烷与氢氧化钠溶液共热后加入硝酸银溶液 | 无浅黄色沉淀出现 | 溴乙烷未水解 |
| B | 向某溶液中先滴加氯水,再滴加少量KSCN溶液。 | 溶液变成血红色 | 溶液中含有Fe2+ |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
| D | 向盛有碘水的试管中加入CCl4后充分振荡静置 | 液体分层,上层基本无色,下层紫红色 | 碘在CCl4中的溶解度较大 |
【知识点】化学实验方案的评价与判断
【答案解析】D 解析:A、溴乙烷与氢氧化钠溶液共热后加入硝酸银溶液,此时溶液呈碱性,所以,无黄色沉淀出现,不能说明溴乙烷未水解,故A错误;B、向某溶液中先滴加氯水,再滴加少量KSCN溶液,溶液变成血红色,只能说明溶液中此时含有Fe3+,不能说明原来是否含有Fe2+,故B错误;C、常温下,向浓硫酸中投入铁片,使其钝化,是氧化成致密的氧化膜阻止了反应的进一步进行,故C错误;D、向盛有碘水的试管中加入CCl4后充分振荡静置,碘更易溶于CCl4,密度比水大,所以,下层紫红色,故D正确。
故答案选D
【思路点拨】本题考查物质的检验和鉴别,侧重于学生的分析和实验能力的考查,为高考高频考点,注意把握物质的性质以及检验方法,难度不大。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图中阴影部分关系的是( )
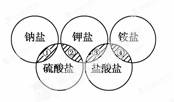
① | ② | ③ | ④ | |
| A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
| B | Na2SO4 | K2SO4 | KCl | NH4Cl |
| C | NaCl | K2SO4 | KCl | NH4Cl |
| D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将质量为2.3g钠用刺了孔的铝箔包裹后放入水中,共收集到2.464L(标准状况)气体.请回答下列问题:
(1)2.3g钠与水反应,理论上生成气体的体积(标准状况)为多少.
(2)反应后溶液的体积为100mL,则混合溶液中NaOH的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式 (i) I2 (g)+ H2(g)  2HI(g) ΔH=-9.48 kJ/mol
2HI(g) ΔH=-9.48 kJ/mol
(ii) I2(S)+ H2(g) 2HI(g) ΔH=+26.48 kJ/mol. 下列判断正确的是
2HI(g) ΔH=+26.48 kJ/mol. 下列判断正确的是
A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
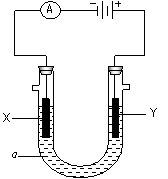 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
电解池中X极上的电极反应式为
。
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,
检验该电极反应产物的方法是 。
(2)如要在某导电塑料表面镀一层金属铜,则
①X电极的材料是 ,电极反应式是 。
②Y电极的材料是 ,电解液a选用 溶液,。
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
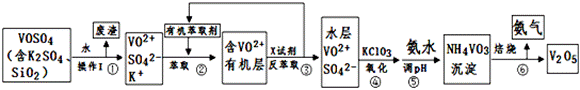 请回答下列问题:
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式)
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+2nHA(有机层) 2RAn(有机层)+nH2SO4 (水层)
2RAn(有机层)+nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)④的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 。
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
该工艺流程中,可以循环利用的物质有 和 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对一些事实的理论解释正确的是( )
| 选项 | 客观事实 | 理论解释 |
| A | Na+比Na原子稳定 | Na+最外电子层有8个电子而Na只有1个 |
| B | 熔化状态下NaCl能导电而NaCl晶体不能导电 | 熔化状态下的NaCl中存在离子而NaCl晶体中没有离子 |
| C | 钾原子比钠原子更易失去电子 | 钾的核电荷数比钠的多 |
| D | 纯碱溶液能使湿润的紫色石蕊试纸变蓝色 | 纯碱能电离出OH-而使石蕊试纸变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧化铁胶体和氯化铁溶液共同具备的性质是
A.都是较稳定的红褐色液体 B. 加入盐酸后,先产生沉淀,随后沉淀溶解
C. 都有丁达尔现象 D.分散质微粒都可通过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,不能用平衡移动原理解释的是( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.黄绿色的氯水光照后颜色变浅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com