
【题目】利用氧化还原反应原理配平
(1)__NH3+___O2![]() ____NO +____H2O
____NO +____H2O
(2)____FeSO4+____KNO3+____H2SO4=____K2SO4+____Fe2(SO4)3+____NO↑+____H2O
【答案】4 5 4 6 6 2 4 1 3 2 4
【解析】
(1)反应中N元素化合价由NH3中-3价升高为NO中+2价,共升高5价,O元素由O2中0价降低为-2价,共降低4价,化合价升降最小公倍数为20,故NH3系数为4,故O2系数为5,利用元素守恒配平其他物质的系数;
(2)反应中Fe元素化合价由+2价升高为+3价,2FeSO4变为Fe2(SO4)3,共升高2价;氮元素由+5价降低到+2价,共降低3价;化合价升降最小公倍数为6,故FeSO4系数为6,KNO3系数为2,利用元素守恒配平其他物质的系数。
(1)反应中N元素化合价由NH3中-3价升高为NO中+2价,共升高5价,O元素由O2中0价降低为-2价,共降低4价,化合价升降最小公倍数为20,故NH3系数为4,故O2系数为5,利用元素守恒可知NO系数为4,H2O的系数为6,故配平后方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
综上所述,本题正确答案为:4 5 4 6;
(2)反应中Fe元素化合价由+2价升高为+3价,2FeSO4变为Fe2(SO4)3,共升高2价;氮元素由+5价降低到+2价,共降低3价;化合价升降最小公倍数为6,故FeSO4系数为6,KNO3系数为2,利用元素守恒可知NO的系数为2,Fe2(SO4)3的系数为3,K2SO4的系数为1,H2SO4的系数为4,H2O的系数为4,故配平后方程式为6FeSO4+2KNO3+4H2SO4=K2SO4+3Fe2(SO4)3+2NO↑+4H2O;
综上所述,本题正确答案: 6 2 4 1 3 2 4。


科目:高中化学 来源: 题型:
【题目】分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇脱水是合成环己烯的常用方法,实验室合成环己烯的反应和实验装置如图:
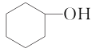
![]()
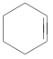 +H2O
+H2O
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
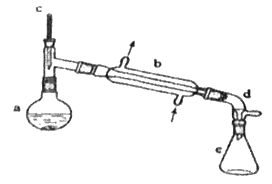
Ⅰ.合成反应:在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
Ⅱ.分离提纯:反应粗产物倒入分液漏斗中分别用少量5 %碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是__。
(2)加入碎瓷片的作用是__;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是__(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并__;在本实验分离过程中,产物应该从分液漏斗的__(填“上口倒出”或“下口倒出”)。
(4)分离提纯过程中加入无水氯化钙的目的是__。
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有__(填正确答案标号)。
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去。)
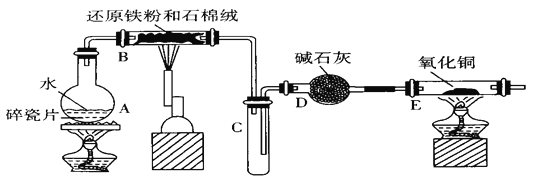
(1)装置B中发生反应的化学方程式是_____________________________________。
(2)装置E中的现象是_____________________________________。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤,简述检验滤液中Fe3+的操作方法:_____________________________________。
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
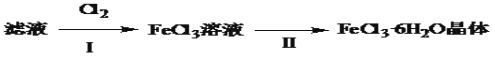
①步骤Ⅰ中通入Cl2发生反应的离子方程式______________________________。
②步骤Ⅱ从FeCl3稀溶液中得到FeCl3·6H2O晶体的主要操作包括:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
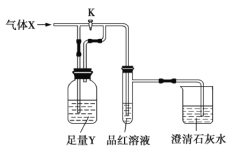
【题目】如图是一套检验气体性质的实验装置。请回答下列问题。
A | B | C | D | |
X | 氯气 | 二氧化硫 | 二氧化碳 | 氯化氢 |
Y | Na2SO3溶液 | 饱和NaHCO3溶液 | Na2SO3溶液 | 饱和NaHSO3溶液 |
(1)向装置中缓缓通入少量气体X,若关闭活塞K,则品红溶液褪色。据此判断气体![]() 和洗气瓶内的溶液Y可能的组合是_________(填表中序号,下同)。
和洗气瓶内的溶液Y可能的组合是_________(填表中序号,下同)。
(2)若打开活塞K,品红溶液褪色,同时澄清石灰水变浑浊,则气体X和洗气瓶内液体Y可能的组合是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CH4可消除NO2的污染,反应原理为:CH4(g)+2NO2(g)![]() N2(g) + CO2(g) +2H2O(g),在10L密闭容器中分别加入0.50mol CH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:
N2(g) + CO2(g) +2H2O(g),在10L密闭容器中分别加入0.50mol CH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:

下列说法正确的是
A.组别①中0 ~20 min内,NO2降解速率为0.0125molL-1min-1
B.由实验数据可知温度T1<T2
C.40min时,表格中M对应的数据为0.18
D.该反应只有在高温下才能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 非金属元素形成的离子一定是阴离子
B. 非金属单质在氧化还原反应中一定是氧化剂
C. 某元素从化合态变为游离态时,一定被还原
D. 金属阳离子被还原不一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将盛有25mLNO2和O2混合气体的量筒倒置于水槽中,一段时间后,气体体积减小到5mL且不再变化(同温同压下)。则原混合气体中NO2和O2的体积比可能是( )
A.1:1B.18:7C.16:9D.23:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)若电解食盐水时消耗NaCl的质量为234 g,则在理论上最多可得氯气的体积为________升(标准状况)。
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙________克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com