
����Ŀ��Na2CO3��һ�ֺ���Ҫ�Ļ�ѧ������ijѧ������ʵ�������Ʊ�Na2CO3�������������Ʊ�ʵ����̣�
��50mL NaOH��Һ����CO2���壬�Ʊ�Na2CO3��Һ��Ϊ�˷�ֹͨ���CO2�������������NaHCO3�������������ʵ�鲽�裺(I)��25mL NaOH��Һ���չ�����CO2���壬��CO2���岻���ܽ⣻(II)С�������Һ1��2���ӣ�(III)�ڵõ�����Һ�м�����һ��(25mL)NaOH��Һ��ʹ��Һ��ֻ�ϡ�
(1)(II)�������Һ��Ŀ���� ��
(III)�л����һ��NaOH��Һ�����ķ�Ӧ�� ��(д���ӷ���ʽ)
(2)����ͬѧ����ƣ���(I)��ʵ��װ�����£�
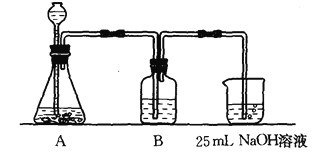
��װ��Aʹ�õ��Լ��� (����)�� ��Һ��
��װ��Bʹ�õ��Լ������ (ѡ��ˮ������NaOH��Һ������Na2CO3��Һ������NaHCO3��Һ)�������� ��д��B�п��ܷ��������ӷ���ʽ ���������Bװ�ã����յõ���Na2CO3��Һ�п��ܴ��ڵ������� ��
��������Ϊʵ�鲽��(II)��(III)��˳��Ե������Ȼ�ϣ�����У�������������Ϊ (���������������)��ԭ��Ϊ ��
���𰸡�(1)��ȥ����������CO2��������ֹ̼�����Ʒֽ⡣
OH-+HCO3-=CO32-+H2O
(2)��ʯ��ʯ ����������̼��������Һ
��ȥCO2�����л��е�HCl���� H++HCO3-=CO2��+H2O
NaCl NaOH
������ �����Ķ�����̼�����������Ʒ�Ӧ����̼������,���²��ﲻ��
��������
���������(1)��(��)�������Һ��Ŀ���Ǹ����ܽ�����Һ�е�CO2���壬��ֹ̼�����Ʒֽ⣬������������Һ���ܽ��CO2���壬����(��)�����NaOH���в�����CO2��Ӧ�����ĵ���ʹNaHCO3������ȫת����Na2CO3����(��)�л����һ��NaOH��Һ�����ķ�Ӧ�����ӷ���ʽ��̼�������ܺ��������Ʒ�Ӧ����̼���ƺ�ˮ����Ӧ���ӷ���ʽΪHCO3-+OH-�TCO32-+H2O��
(2)���Ʊ�������̼������Լ�ѡ��Ӧԭ���ǹ���̼��ƺ����ᷴӦ���ɶ�����̼���壬ѡ�����Ϊ����ʯ��ʯ��ʯ��Һ��Ϊ���
���÷�Ӧ�Ƿ��ȷ�Ӧ�����ŷ�Ӧ�Ľ��У���Һ���¶����ߣ�������лӷ��ԣ��������ɵĶ�����̼�к����Ȼ������壬Ϊ�˳�ȥ������̼�е��Ȼ��������ֲ������µ����ʣ��ñ��͵�̼��������Һ�����Ȼ��⣬��ʱ������Ӧ�����ӷ���ʽΪ H++ HCO3-= CO2��+H2O����ȥ��װ��B���Ȼ���Ͷ�����ֱ̼�ӽ�������������Һ�У��������Ȼ��ƣ�̼���ƣ��ټ�����������������Һ���������ƻ���������Ժ��е�������ҪΪNaCl��NaOH��
�����ʵ�鲽��(II)��(III)��˳��Ե�����Һ���ܽ��˲��ֶ�����̼��������̼���������Ʒ�Ӧ��ʹ�������Ƶ������٣����Һ��̼�����ƺ��������Ƶ����ʵ�������ȣ����Բ���ǡ����ȫ��Ӧ����̼���ƣ������̼�����ƣ����Բ�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڵ���ʲ��ܵ����������
A�����ڵ�NaCl B��KNO3��Һ C������ͭ D���ƾ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.Ϊ�˽�ԼӦ��ʵ�������ȡ�õ�ʣ��ҩƷ�Ż�ԭ�Լ�ƿ
B.��������������Σ�ջ�ѧƷ��־�����ǣ���ʪ��ȼ��Ʒ
C.�ƾ��Ż�Ѹ����ʪĨ����ɳ�Ӹ���
D.����������Һ�������У�Ӧ�����ô���ˮ��ϴ������ϡ�����ϴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��E��F��G��H��I��J��K������ͼת����ϵ�������в���������δ�ڿ��ͼ���г�������A��D��HΪ�������ʣ���ҺC�ڽ�����ɫ��Ӧʱ���۹۲쵽��ɫ���棬�Իش�
��1��д���������ʵĻ�ѧʽ��B�� ��D�� ��K�� ��
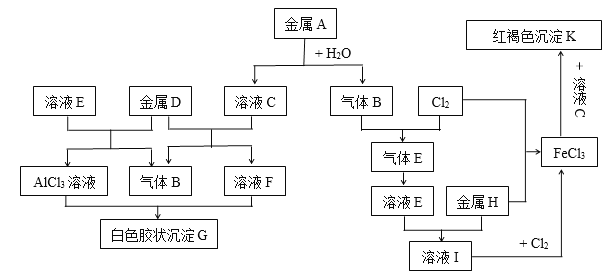
��2����������A��D��H���ܽ���ȼ��ʵ�飺����A��O2�ڼ��ȵ���������� ����ɫ�����壬��Ҫ��;�� ������H��O2��ȼ�յķ�Ӧ�����ǻ������䣬���ɺ�ɫ���� ����д��������������D��ȼ����Ҫ������ȵ�2500������Ҫ��ԭ���� ��
��3��д��C��D��Ӧ�Ļ�ѧ����ʽ�� ���÷�Ӧ�е��������� ��
��4��ʵ������AlCl3��Һ��ȡG�����ӷ���ʽ�ǣ� ��
��5��д��I��C��Ӧ��ʵ������ ��Ϊ����˷�Ӧ����Kһ�����ܱջ�����ʵ�飬ͬʱ�ڷ�Ӧ�Լ��м������� ��ѡ����ۡ��������ᡱ��KSCN��Һ������
��6������A��D��H������ˮ��һ�������·�Ӧ��������A��D��H��������H2O��ַ�Ӧ��õ���ͬ�������壬�����ʵ���֮���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�ӽṹ�������У�
������ԭ�Ӻ˾������Ӻ����ӹ��ɣ�
��ԭ�Ӵ��ڻ�̬ʱ���������Ӳ�һ����8����
��ϡ������Ԫ�أ����̬ԭ������㶼��8�����ӣ�
������������Ϊ2��ԭ��һ���ǽ���ԭ�ӡ�
������ȷ����
A���٢� B���ڢ� C��ֻ�Т� D��ֻ�Т�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڵ�������ܵ������(����)
A. ͭ B. ���ڵ������
C. ����������Һ D. �Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ɫ��Һ�п����ܴ���������������ǣ� ��
A.Na+��NO3����Cl��
B.Cu2+��K+��NO3��
C.H+��HCO3����NO3��
D.Na+��Ba2+��SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����᳧��������Ҫ�ɷ���Fe2O3����κ�������SiO2��FeS����ҵ���������᳧���������մ����Ƶ��̷�(FeSO4��7H2O)��һ�־�������[Fe(OH)SO4]n���̷�������ȱ����ƶѪҩƷ����Ҫ�ɷ�����������������Ҫ��ˮ���������������������������£�

��ͨ�������ش�����������⣺
��1�����ղ�����β���Դ�������Ⱦ����˹�ҵ�����б�����л��մ��������з������е���_______________��
A���ð�ˮ���� B. ֱ����ˮ����
C. ��Ũ�������� D. ����������ʯ��ʯ��ĩ����Һ����
��2����������_____________��_______________�����ˡ�ϴ�ӡ����ﱣ��ȣ�
��3��������ҺX�ƾ������������������pH���������¶�Ŀ����___________________��
��4���ڷ�Ӧ����FeS��O2��ϡH2SO4��Ӧ�����������ʣ���Ӧ�����ӷ���ʽΪ___________________________��
��5��ij�о���С��Ϊ̽���̷�(��Է���������278)�ڸ������������¼��ȷֽⷴӦ�IJ���(��֪�ֽ����ȫΪ������)����������ͼ��ʾ��ʵ�飺

�� ʵ�鿪ʼʱ���ڵ�ȼC���ƾ����֮ǰӦ�ȴ���ͨCO2����Ŀ����_____________�� װ��D��������______________________��
������ͬѧ��Ƶ�װ�ô�����һ�����Ե�ȱ����____________________________��
������ͬѧ��ȡ55.6 g�̷�����ͼװ�ý���ʵ�顣���̷��ֽ���ȫ����Eƿ�в�����23.3 g��ɫ��������C�й������Ͷ������ϡ��������ȫ�ܽ�õ���Һ��ȡ��������Һ����KSCN��Һ�ʺ�ɫ����ȡ��������Һ��������KMnO4��Һ��KMnO4��Һ����ɫ����д���̷��ֽ�Ļ�ѧ����ʽΪ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������m gij���壬����˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM g��mol��1���������ӵ�������NA��ʾ����
��1������������ʵ���Ϊ________mol��
��2������������ԭ������Ϊ________����
��3���������ڱ�״���µ����Ϊ____________L��
��4������������ˮ���γ�VL��Һ������Һ�����ʵ���Ũ��Ϊ____________ mol/L��
��5������������1 Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ_______________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com