
����Ŀ���йص绯ѧ֪ʶ��������ȷ����
A. Cu+H2SO4=CuSO4+H2�������Ӧ����Ƴ�ԭ���
B. ����Cu+2FeCl3=CuCl2+2FeCl2���������ͼ��ʾԭ���װ�ã�������K+��FeCl3��Һ�ƶ�

C. ��Ϊ���Ļ�����ǿ��ͭ�����Խ�����ͭ�õ������Ӻ����Ũ���������ԭ��أ�����������ͭ���������为����ӦʽΪFe-2e-=Fe2+
D. ��Al��Mg������������Һ��ɵ�ԭ��أ��为����ӦʽΪMg-2e-+2OH-=Mg(OH)2
���𰸡�B
��������
A.���ڻ��H>Cu������Cu������ܷ�����Ӧ�����Ը÷�Ӧ�����Է���������ԭ��Ӧ��������Ƴ�ԭ��أ�A����
B.���ݵ���ܷ�ӦʽCu+2FeCl3=CuCl2+2FeCl2����֪Cuʧ���ӣ���ԭ��صĸ�����������Fe3+�õ�������Fe2+�������������ԭ��أ���������FeCl3�ͻ�ԭ��Cu�ֿ���ԭ��ع���ʱ�������е��������������ƶ�����������K+��FeCl3��Һ�ƶ���B��ȷ��
C.����ͭ�õ������Ӻ����Ũ���������ԭ��أ�������������������Ũ�����ۻ������Խ���ͭ��������ʧȥ���ӣ�����������Ӧ���缫��ӦʽΪCu-2e-�TCu2+��C����
D.��Al��Mg��NaOH��Һ��ɵ�ԭ��أ�Mg��NaOH���ܷ�����Ӧ����Al��NaOH��Һ��Ӧ�����Ը�ԭ�����Al��������Alʧ���ӣ�����������Ӧ�� D����
�ʺ���ѡ����B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ʱ��
ʱ��![]() �������ε���Һ�У�H2SO3��HSO3-��SO32-�����ʵ�������(��)����ҺpH�仯��ϵ��ͼ��ʾ�����������������( )
�������ε���Һ�У�H2SO3��HSO3-��SO32-�����ʵ�������(��)����ҺpH�仯��ϵ��ͼ��ʾ�����������������( )

A. ��Һ��pH=5ʱ����Ԫ�ص���Ҫ������ʽΪ![]()
B. ����Һǡ�ó�����ʱ: c(Na+)>c(HSO3-)+c(SO32-)
C. ��pH=8��������Һ�еμ���������ʯ��ˮ�� ��ֵ����
��ֵ����
D. ��pH=3��������Һ�еμ�����ϡ���ᣬ![]() ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鲻�ܴﵽԤ��ʵ��Ŀ���ǣ���
��� | ʵ������ | ʵ��Ŀ�� |
A | �����£���pH��ֽ�ⶨŨ��Ϊ0.1mol��L-1NaClO��Һ��0.1mol��L-1CH3COONa��Һ��pH | �Ƚ�HClO��CH3COOH������ǿ�� |
B | ��ʢ��1mL��������Һ���Թ��еμ�NaCl��Һ���������г������ɣ��������еμ�Na2S��Һ | ˵��һ�ֳ�����ת��Ϊ��һ���ܽ�ȸ�С�ij��� |
C | ��������FeCl3��MgCl2��Һ�м�������Mg(OH)2��ĩ������һ����� | ��ȥMgCl2������FeCl3 |
D | �����£��ֱ���2֧�Թ��м�����ͬ�������ͬŨ�ȵ�Na2S2O3��Һ���ٷֱ������ͬ�����ͬŨ�ȵ�ϡ���� | �о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С������ͼװ�ý���ʵ�飬�Իش��������⣺

(1)����ʼʱ����K��a���ӣ���A���ĵ缫��ӦʽΪ____________________B����Fe����__________ ��ʴ(��������������������)
(2)����ʼʱ����K��b���ӣ�����˵����ȷ����________(�����)
����Һ��Na����A���ƶ���
�ڴ�A�����ݳ���������ʹʪ���KI������ֽ������
�۷�Ӧһ��ʱ������������ɻָ������ǰ����ʵ�Ũ�ȡ�
������״����B������2.24 L���壬����Һ��ת��0.2 mol����
�Ҵ�ʱװ�����ܷ�Ӧ�����ӷ���ʽΪ_____________________________________________________
(3)��С��ͬѧ��Ϊ�����ģ�ҵ�����ӽ���Ĥ�����ռ�ķ�������ô������������ͼװ�õ���������Һ����ȡ������������������������ء�

�ٸõ��۵�������ӦʽΪ_________________________________________����ʱͨ�������ӽ���Ĥ��������________(������������С��������������)ͨ�������ӽ���Ĥ����������
���Ƶõ�����������Һ�ӳ���________(����A����B����C������D��)������
�ö��Ե缫������Ϊ1L��CuSO4��Һ����������������3.36L(���)����ʱ����������ͭ��Ũ��Ϊ______����Ҫ����Һ�ָ���ԭ״̬��Ҫ����________(��ѡ��)
A.CuSO4 B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ģ�����ͼΪN2(g)��O2(g)��Ӧ����NO(g)�����е������仯��������˵����ȷ����

A. ͨ������£�NO��N2�ȶ�
B. ͨ������£�N2(g)��O2(g)�����ֱ������NO
C. 1molN2(g)��1molO2(g)�����������2mol NO(g)���������
D. 1molN2(g)��1molO2(g)��Ӧ�ų�������Ϊ180kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء�����˵���������
A. PM2.5��ָ����������2.5��m�Ŀ���������������
B. ��ɫ��ѧҪ���Դͷ�����������������Ի�������Ⱦ
C. ȼú�м���CaO���Լ���������γɼ�����������ŷ�
D. ��Ȼ����Һ��ʯ�������ҹ�Ŀǰ�ƹ�ʹ�õ����ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����2L���ܱ������У�X��Y��Z(��Ϊ����)�������ʵ�����ʱ��ı仯������ͼ��ʾ��

(1)��ͼ���������ݽ��з������÷�Ӧ�Ļ�ѧ����ʽΪ__________��
(2)��������Ӧ��X��Y��Z�ֱ�ΪH2��N2��NH3��ij�¶��£����ݻ��㶨Ϊ2.0L���ܱ������г���2.0mol N2��2.0mol H2��һ��ʱ���Ӧ��ƽ��״̬��ʵ�����������ʾ��
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
0~50s�ڵ�ƽ����Ӧ����v(N2)=_________��
(3)��֪������ָ�ڱ�״���£���1mol��̬����AB(g)����Ϊ��̬ԭ��A(g)��B(g)������������÷���E��ʾ����λΪkJ/mol��![]() �ļ���Ϊ946kJ/mol��H-H�ļ���Ϊ436kJ/mol��N-H�ļ���Ϊ391kJ/mol��������1mol NH3������___(���������������ų���)������Ϊ____����Ӧ�ﵽ(2)�е�ƽ��״̬ʱ����Ӧ�������仯����ֵΪ____kJ��
�ļ���Ϊ946kJ/mol��H-H�ļ���Ϊ436kJ/mol��N-H�ļ���Ϊ391kJ/mol��������1mol NH3������___(���������������ų���)������Ϊ____����Ӧ�ﵽ(2)�е�ƽ��״̬ʱ����Ӧ�������仯����ֵΪ____kJ��
(4)Ϊ�ӿ췴Ӧ���ʣ����Բ�ȡ�Ĵ�ʩ��_______
a.�����¶�
b.����ѹǿ
c.����ʱ����He��
d.��ѹʱ����He��
e.��ʱ����NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��
3Zn��2K2FeO4��8H2O![]() 3Zn��OH��2��2Fe��OH��3��4KOH
3Zn��OH��2��2Fe��OH��3��4KOH
������������ȷ���ǣ� ��
A. �ŵ�ʱ������ӦΪ��Zn��2e����2OH��=Zn��OH��2
B. �ŵ�ʱ������ӦΪ��FeO42-��4H2O��3e��=Fe��OH��3��5OH��
C. �ŵ�ʱÿת��3 mol���ӣ�������1 mol K2FeO4������
D. �ŵ�ʱ����������Һ�ļ�����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������100mL 0��2mol��L-1�İ�ˮ����μ���0��2mol��L-1�����ᣬ������Һ��pH����Һ��NH4+��NH3��H2O�����ʵ�������![]() �������������V�Ĺ�ϵ��ͼ��ʾ������˵���������
�������������V�Ĺ�ϵ��ͼ��ʾ������˵���������
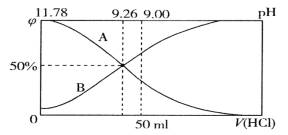
A. ��ʾNH3��H2O���ʵ��������仯��������A
B. NH3��H2O�ĵ��볣��Ϊ1.8��10-5mol��L-1(��֪lg1.8=0.26)
C. �������������Ϊ50mLʱ����Һ��c(NH4+)��c(NH3��H2O)=2��(10-5��10-9)mol��L-1
D. pH=9.26ʱ����Һ�У�NH4+��ˮ��̶ȵ���NH3��H2O�ĵ���̶�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com