
【题目】25°C时,如图烧杯中各盛有50mL的溶液. 
(1)甲溶液PH=;
(2)若将甲溶液全部倒入乙中,所得的混合溶液的PH丙溶液的PH(填“>”、“<”或“=”).
(3)若将乙溶液全部倒入丙中,所得的混合溶液PH>7,所得溶液中离子浓度大小顺序是 .
【答案】
(1)2
(2)>
(3)c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
【解析】解:(1)氯化氢是强电解质,在水中完全电离,所以c(H+)=c(HCl)=0.01mol/L,所以pH=﹣lgc(H+)=﹣lg0.01=2,
所以答案是:2;(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,溶液混合时体积增大一倍,浓度是丙中的一半,氯化铵的浓度越小,其酸性越弱,所以混合溶液的pH大于丙,
所以答案是:>;(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,所以得c(OH﹣)>c(H+),根据电荷守恒c(NH4+)+c(H+)=c(Cl﹣)+c(OH﹣)可知:c(NH4+)>c(Cl﹣),则溶液中离子浓度大小顺序是:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+),
所以答案是:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+).


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是短周期的五种主族元素.A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构.根据上述信息回答下列问题:
(1)B元素的原子结构示意图是;C元素原子的轨道表示式是;D元素原子的价电子排布式是;
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示);
(3)由B,D,E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式;用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
方案Ⅰ:有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸或稀盐酸中,观察产生气泡的快慢,据此确定它们的活动性.该原理的离子方程式为 .
方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性.试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,
并写出电极反应式.正极反应式:;负极反应式:;
方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案与方案Ⅰ、Ⅱ不能雷同: , 用离子方程式表示其反应原理: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镁还原热解制备高纯氧化镁是一种新的探索,以解决氧化镁在医药、建筑等行业的应用广泛。现以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:

(1)酸溶所涉及反应的离子方程式为_________________________________________、_________________________________________________________。
(2)加入H2O2氧化的作用是_________________,滤渣2的成分是___________(填化学式)。
(3)煅烧过程存在以下反应:
2MgSO4+C![]() 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C![]() MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C![]() MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。

①B中盛放的溶液可以是______(填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c. KMnO4溶液 d. 稀硝酸
②C装置的作用是______________________,D中收集的气体可以是 _______(填化学式)。
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时,水溶液中c(H+)与c(OH﹣)的变化关系如图中曲线 ac所示,下列判断错误的是( ) 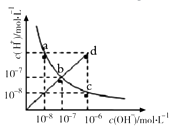
A.ac曲线上的任意一点都有c(H+)×c(OH﹣)=10﹣14
B.CH3COONa溶液不可能位于c点
C.d点对应溶液的温度高于25°C,PH<7
D.bd线段上任意一点对应的溶液都呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的区分方法不正确的是
A.用碘酒区分淀粉溶液与蛋白质溶液
B.用AgNO3溶液区分NaCl与KCl溶液
C.用澄清石灰水区分CO与CO2气体
D.用石蕊试液区分稀H2SO4与NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用合成气(主要成分为CO2、H2、CO)在催化剂作用下合成甲醇,并可用甲醇合成甲醚。
(1)CO2的电子式是________。
(2)已知:CO(g)+2H2(g)![]() CH3OH(g) △H1 = -90.77 kJ/mol
CH3OH(g) △H1 = -90.77 kJ/mol
CO2 (g)+H2 (g)![]() CO(g)+H2O(g) △H2 = +41.19 kJ/mol
CO(g)+H2O(g) △H2 = +41.19 kJ/mol
则CO2与H2反应制备CH3OH(g)的热化学方程式是________。
(3)向三个体积均为1L的恒容密闭容器中分别充入1mol CO2和3mol H2,在不同催化剂作用下同时反应制备CH3OH(g)。测得H2转化率随温度变化的数据如下表所示。

(注:T5时,H2转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是________(填“I”“II”或“III”)。
②T3时,反应I的v(正)________v(逆)(填“>”“<”或“=”)。
③温度为T5时,该反应的平衡常数K=________。
(4)甲醇合成甲醚的反应为2CH3OH(g)![]() CH3OCH3(g)+H2O(g),反应过程中存在副反应2CH3OH(g)
CH3OCH3(g)+H2O(g),反应过程中存在副反应2CH3OH(g)![]() C2H4(g)+2H2O(g)。反应过程中的能量变化如图所示:
C2H4(g)+2H2O(g)。反应过程中的能量变化如图所示:

①反应速率较快的是________(填“Ⅰ”或“Ⅱ”),原因是________。
②根据反应原理,分析增大压强对合成甲醚的影响________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象和结论都正确,且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 常温下,质量和形状相同的Al片分别和等体积稀HNO3和浓HNO3反应 | 前者产生无色气体,后者产生红棕色气体,且后者反应更加剧烈 | 其他条件相同时,反应物浓度越大,反应速率越快 |
B | 某食盐溶液中加入淀粉溶液 | 溶液不变蓝 | 该食盐样品中一定不含KIO3 |
C | SO2通入BaCl2 溶液,然后滴入稀硝酸 | 有白色沉淀产生,加入稀硝酸后沉淀不溶解 | 所得沉淀为BaSO3,后转化为BaSO4 |
D | 将少量大理石粉未加入1.0mol/L的NH4Cl 溶液中 | 产生气体,粉末溶解 | NH4Cl水解使溶液呈酸性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是 ( )
①可能有C2H2
②一定有CH4
③一定有C3H8
④一定没有C4H6
⑤可能有C2H6 . 
A.②⑤
B.②④
C.③④
D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com