
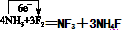 ,故答案为:
,故答案为: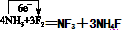 ;
;

科目:高中化学 来源: 题型:
| A、①中水的电离程度最小,③中水的电离程度最大 |
| B、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:①最大 |
| C、将四份溶液稀释相同倍数后,溶液的pH:③>④,②>① |
| D、将②、③混合,若pH=7,则消耗溶液的体积:②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 M是一种治疗艾滋病的新药(结构简式如图所示),已知M分子中-NH-COO-基团(除H外)与苯环在同一平面内,关于M的以下说法正确的是( )
M是一种治疗艾滋病的新药(结构简式如图所示),已知M分子中-NH-COO-基团(除H外)与苯环在同一平面内,关于M的以下说法正确的是( )| A、该物质易溶于水 |
| B、M能发生加聚反应 |
| C、M的分子式为C13H12O2NF4 |
| D、M分子内有15个原子在同一个平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4 | B、5 | C、6 | D、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com