
【题目】某温度下的固定容器中发生反应2SO2(g)+O2(g)![]() 2SO3(g),其浓度与时间的关系如下表。下列说法错误的是( )
2SO3(g),其浓度与时间的关系如下表。下列说法错误的是( )

A. 0 min时正反应速率最大,逆反应速率为零
B. 0~40 min内,正反应速率大于逆反应速率
C. 50 min时达到了化学平衡,此时正反应速率等于逆反应速率
D. 50 min及以后的时间内,都处于平衡状态,反应物和生成物的浓度不再发生变化,反应停止了
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】有机物环丙叉环丙烷,由于其特殊的电导结构一直受到理论化学家的注意,其结构如图所示。有关它的说法中错误的是( )
![]()
A. 其二氯代物有4种 B. 它所有的原子均在同一平面上
C. 其分子式为C6H8 D. 它不可能是环丙烷的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验是科学探究过程中的一种重要方法,掌握化学实验的基本操作和物质的制备、转化及性质的探究尤为重要,请结合所学化学实验知识回答以下问题。
I.实验室配制220mL 1 mol·L-1的稀H2SO4溶液:
(1)用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为________mL。
(2)配制该溶液时需用的主要仪器有量筒、烧杯、玻璃棒、________、________等。
(3)误差下列情况使配制结果偏大的是________。
①溶解后未冷却即转移、定容
②定容时仰视容量瓶刻度线
③用量筒量取一定体积的浓硫酸时俯视
④将量筒、烧杯、玻璃棒洗涤2~3次,转移至容量瓶
II.如图A、B、C是实验室常见的几种气体发生装置:
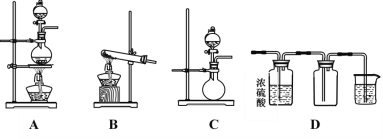
(1)实验室如果用B装置制备氨气,其化学方程式是___________________________。
(2)若想制得干燥的氨气,应选用的干燥剂是_______(填序号,下同)。
①无水CaCl2 ②碱石灰 ③浓硫酸 ④无水CuSO4
(3)若用A装置与D装置相连制备并收集X气体,则X可以是下列气体中的_______。
①CO2 ②NO ③Cl2 ④H2
其中在D装置中连接小烧杯的目的是________________________________。
III.某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
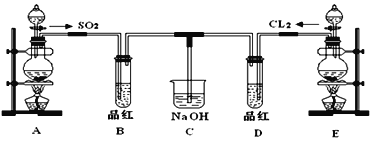
(1)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:_____________________________,D:________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:_____________________________,D:________________________。
(2)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_________。
(3)若E装置中开始加入200mL 11.8 mol·L-1的浓盐酸和足量的MnO2固体,反应后的混合物经过滤所得溶液,加入足量的AgNO3溶液,所得沉淀的物质的量的范围为_____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔质量为Mg·mol-1的气态化合物VL (已换算成标准状况) 溶于mg 水中,得到溶液的溶质质量分数为ω%,物质的量浓度为cmol·L-1,密度为ρg·cm-3,则下列说法正确的是( )
A. M 可表示为![]() B. c 可表示为
B. c 可表示为![]()
C. ω%可表示为![]() D. ρ可表示为
D. ρ可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图装置进行实验:加热钠至熔化后,停止加热并通入氯气,钠剧烈燃烧并生成大量白烟。以下叙述错误的是
![]()
A. 钠着火燃烧产生苍白色火焰
B. 反应生成的大量白烟是氯化钠固体小颗粒
C. 棉球处发生的化学反应是: Cl2+2NaOH=NaCl+NaClO+H2O
D. 可在棉球右侧用湿润的淀粉碘化钾试纸判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是()
A. 铁在潮湿空气中生锈是自发过程
B. 电解池的反应是属于自发反应
C. NH4NO3溶于水吸热,说明其溶于水不是自发过程
D. 非自发反应在任何条件下一定都不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、![]() 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
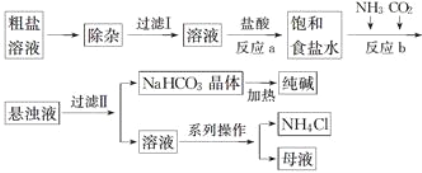
A. 在“侯氏制碱法”中涉及到了氧化还原反应
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 工艺中只有碳酸氢钠加热分解产生的CO2可回收循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C均为中学化学常见的单质, 其中一种是常见金属,通常状况下,A为固体,B为深红棕色液体,C为气体,其余均为化合物,X是一种具有挥发性的无氧强酸,E为黑色晶体,H为无色液体,它们之间的转化关系如图(其中某些反应条件和产物已略去)。

(1)在反应①~⑦中,不属于氧化还原反应的是______ (填序号)。
(2)G溶液与氯气按物质的量1∶1反应的离子方程式:________ 。
(3)反应⑦的化学方程式为 _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,现向50 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.05 mol·L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生)。下列说法正确的是

A.b点溶液中离子浓度由大到小的顺序为:c(Na+)>c(SO![]() )>c(NH
)>c(NH![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.图中b、c、d三点溶液中水的电离程度最大的是c点
C.b点后滴加NaOH溶液过程中,NH3·H2O的电离程度逐渐减小
D.pH=7时,溶液中c(H+)+c(Na+)+c(NH![]() )=c(SO
)=c(SO![]() )+c(OH-)
)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com