
【题目】分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“CH3COOK”的分类不正确的是
A.化合物B.氧化物C.有机物D.钾盐
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】在化学课上老师向NaOH溶液通入CO2后无明显现象。
(提出问题)如何通过实验证明CO2与NaOH发生了反应?
(查阅资料)①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(Na2CO3+HCl=NaHCO3+NaCl)。
②碳酸钠在二氧化碳过量的条件下继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)(1)从反应物之一CO2消失的角度,某同学设计了如图所示的实验,打开活塞。向充满CO2的瓶中滴入NaOH溶液,一会儿后观察到的现象是_________,据此判断NaOH与CO2发生了化学反应。但上述实验还不足证明反应,其理由是_______,完善的方案是_______________________________。

(2)从生成物Na2CO3角度,经过讨论,分别设计了以下两个实验方案:
实验操作 | 实验现象 | 结论 |
方案一:向(1)所得的溶液中加入_______溶液 | 有白色沉淀产生 | 有新物质Na2CO3生成,发生反应。 |
方案二:向(1)所得的溶液中滴加过量稀盐酸 | ___________; |
(反思评价)方案二滴加过量稀盐酸的原因是_________。
(实验拓展)该小组同学将过量的干冰放入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,如图所示,请用化学方程式回答下列问题:

(1)BC段变化原因可能是__________________________;
(2)CD段变化原因可能是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应可用离子方程式“H++OH-=H2O”表示的是( )
A.NaHSO4溶液与Ba(OH)2溶液混合
B.NH4Cl溶液与Ca(OH)2溶液混合
C.HNO3溶液与KOH溶液混合
D.CH3COOH溶液与NaOH溶液混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,pH 均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH 随溶液体积的变化曲线如图所示。下列说法正确的是

A. HA的酸性比HB的酸性弱
B. a点溶液的导电性比c点溶液的导电性弱
C. 若两溶液加水稀释,则所有离子的浓度都减小
D. 对a、b两点溶液同时升高温度,则c(A-)/c(B-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式,书写正确的是( )
A.盐酸与石灰石反应:CO32-+H+=CO2↑+H2O
B.硫酸铜溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4↓
C.氢氧化镁和盐酸反应:H++OH-=H2O
D.氯化铝溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有①甲烷、②乙烯、③苯、④乙酸、⑤甘氨酸(氨基乙酸)5种有机物,请用序号或按题中要求作答:
(1)分子中所有原子都共平面的是__________________。
(2)含氢量最高的是_______,含碳量最高的是________。
(3)完全燃烧后生成的CO2和水的物质的量之比为1∶1的是__________。
(4)其中含有两种不同官能团的有机物是_____,其结构简式为________________,官能团的名称分别为__________和__________。
Ⅱ.下图表示4个碳原子相互结合的几种方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。
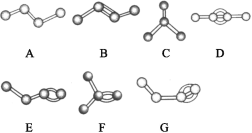
(5)图中属于烷烃的是______(填字母)。
(6)上图中A与________、B与________、D与_____互为同分异构体(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气既是高效洁净的能源,也是重要的化工原料。
(1)甲烷分子的结构式为_________,空间构型为_______________形。
(2)已知25℃、101kPa 时,1 g甲烷完全燃烧生成液态水放出55.64 kJ热量,则该条件下反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=____________kJ·mol-1。
(3)甲烷高温分解生成氢气和炭黑。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是__________________________________________。
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的能量直接转化为电能。用甲烷-空气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。已知甲烷空气碱性燃料电池的总反应为:CH4+2O2+2KOH=K2CO3+3H2O,装置如下图所示:

①a电极名称为____________。
②c电极的电极反应式为_________________________________。
③假设CuCl2溶液足量,当某电极上析出3.2 g 金属Cu时,理论上燃料电池消耗的甲烷在标准状况下的体积是__________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验仪器特点的描述正确的或实验能达到预期目的的是( )
A.托盘天平标尺的“0”刻度在中间
B.量筒的“0”刻度在下面
C.用10 mL量筒去量取7.50 mL稀盐酸
D.用托盘天平称量25.2 g NaCl晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池具有比能量高、无污染的特点,用下图模拟其工作原理(放电时两电极均有稳定的金属氢氧化物生成),下列有关说法中正确的是( )

A. 放电时,电子由正极通过外电路流向负极
B. 放电时,负极上的电极反应式为:Zn-2e ─+2H2O = Zn(OH)2+2H+
C. 充电时,阴极区溶液的pH减小
D. 充电时,阳极上的电极反应式为:Fe(OH)3-3e ─+5OH ─ = FeO42 ─+4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com