
【题目】室温下,0.1mol/L NaOH溶液分别滴定100mL 0.1mol/L HA、HB两种酸溶液。pH随NaOH 溶液体积如下图所示,下列判断错误的是
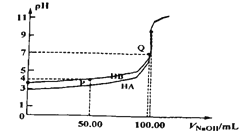
A. 电离常数: Ka(HA)> Kb(HB)
B. 由P点计算Ka(HB) ≈10-4
C. pH=7 时,c(A-)=c(B-)
D. 中和分数达100%时,HA溶液中存在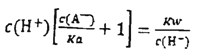
【答案】C
【解析】A、相同物质的量浓度的一元酸,酸的pH越小,氢离子浓度越大,说明酸的电离程度越大,则该酸的酸性越强,其电离平衡常数越大,根据图知,未加NaOH溶液时,pH:HA<HB,说明酸的电离程度HA>HB,则KHA>KHB,故A正确;B、100mL 0.1mol/L HB溶液加入50mL0.1mol/L NaOH溶液后,C(HB) ≈( 0.1mol·L-1 ×100mL -0.1mol·L-1 ×50mL)/(100mL+50mL)=0.1/3mol·L-1,C(B-) ≈(0.1mol·L-1 ×50mL)/(100mL+50mL)=0.1/3mol·L-1,Ka(HB) =C(H+)C(B-)/C(HB) ≈C(H+)=10-4,故B正确;C、pH=7时,溶液中c(H+)=c(OH-),根据电荷守恒,对于HA溶液,c(Na+)=c(A-),对于HB溶液,c(Na+)=c(B-),由于HA,HB的酸性并不一致,则使溶液呈中性时,二种溶液中c(Na+)并不相等,则c(A-),c(B-)并不相等,故C错误;D、中和分数达100%时,HA溶液中实际上是Na A溶液,根据质子守恒得c(HA)+c(H+)=c(OH-),ka=c(H+)c(A-)/c(HA),kw=c(H+)c(OH-)代入质子守恒的等式,得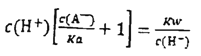 ,故D正确。故选C。
,故D正确。故选C。


科目:高中化学 来源: 题型:
【题目】用锌粒与稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是( )
A. 升高反应体系的温度 B. 增加锌粒的用量
C. 不用锌粒,改用锌粉 D. 滴入少量硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.25℃ 101kPa时,CH4(g)+2O2(g)=CO2(g) +2H2O(g) △H=-Q kJ/mol,则甲烷的燃烧热为Q kJ/mol
B.CaCO3(s)=CaO(s)+CO2(g) 室温下不能自发进行,说明该反应的 ΔH<0
C.反应N2(g)+3H2(g)![]() 2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大
2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大
D.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2的值均大于零):H2(g) +Cl2(g)=2HCl(g),△H1=—Q1 kJ/mol,H2(g) +Br2(g)=2HBr(g),△H2=—Q2 kJ/mol,则△H1<△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度(t℃)时,水的离子积为KW=1.0×10﹣13mol2L﹣2,则该温度(填“大于”、“小于”或“等于”)_____25℃,其理由是________________________________。
(2)若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计). 若所得混合液为中性,则a:b=_____;此溶液中各种离子的浓度由大到小排列顺序是_________________。
(3)FeCl3的水溶液呈酸性的原因是(用离子方程式表示):______________。
(4)实验室在配制FeCl3的溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以__ (填“促进”、“抑制”)其水解。
(5)把氯化铝溶液蒸干并灼烧固体产物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水体中重金属铅的污染问题备受关注。查资料知Pb4+具有很强的氧化性,水中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2( 在水中溶解度小)、Pb(OH)3-、Pb(OH)42-,各形态的物质的量分数a随溶液pH变化的关系如下图所示:
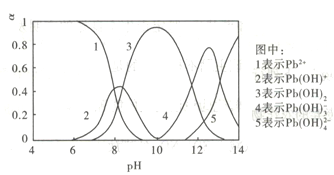
下列有关说法正确的是
A. Pb(NO3)2溶液中,c(Pb2+)/c(NO3-)=1/2
B. 向Pb(NO3)2波中滴加氯化铵溶液,溶液中c(Pb2+)/c(NO3-)变小,可能是Cl-与Pb2+发生反应
C. 向Pb(NO3)2溶液中滴加NaOH溶液,pH 越大,生成沉淀越多
D. pH=12时,混合体系中发生的主要反应的离子方程式为Pb(OH)3-+OH-=Pb(OH)42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学式为C3H4O2的液态有机物X(不含环状结构)不能与碳酸氢钠发生反应,推测X不可能发生的反应是
A.消去反应B.酯化反应C.加聚反应D.银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于A2+3B2═2C+D(均为气态物质)的反应来说,以下化学反应速的表示中,反应速率最快的是( )
A.v(A2)=0.4 molL﹣1s﹣1
B.v(D)=6 molL﹣1min﹣1
C.v(C)=0.6 molL﹣1s﹣1
D.v(B2)=0.8 molL﹣1s﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com