
����Ŀ����A��B��C��D��E���ֶ�����Ԫ�أ����ǵĺ˵������C��A��B��D��E��˳������C��D���ֱܷ���A��ԭ�Ӹ�����Ϊ1:1��2:1�γɻ����CB����EA2��Ӧ����C2A����̬����EB4��E��M���������K���������2����
��1��д������Ԫ�ص����ƣ�B_________��E_____________��
��2��д������ʽ��EB4__________��
��3��D2A2�к��еĻ�ѧ��Ϊ___________________________��
��4����A��C��D����Ԫ����ɵĻ�����M����____������ӡ����ۡ��������M����ˮ��______����ǡ���������ѧ�仯��ԭ����______________________���ӻ�ѧ���Ƕȷ�����
���𰸡� �� �� 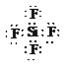 ���Ӽ����ۼ� ���� �� ֻ�оɼ��Ķ��Ѷ����¼����γ�
���Ӽ����ۼ� ���� �� ֻ�оɼ��Ķ��Ѷ����¼����γ�
�����������������������Ҫ�����Ƶ�Ԫ�ص����ʡ�
E��M���������K���������2����E�ǹ���CB����EA2��Ӧ����C2A����̬����EB4��������Ӧ��SiO2+4HF![]() SiF4��+2H2O������C��A��B�ֱ����⡢��������C��D���ֱܷ���A��ԭ�Ӹ�����Ϊ1:1��2:1�γɻ�������D���ơ�
SiF4��+2H2O������C��A��B�ֱ����⡢��������C��D���ֱܷ���A��ԭ�Ӹ�����Ϊ1:1��2:1�γɻ�������D���ơ�
��1������Ԫ�ص����ƣ�B����E����
��2������ʽ��EB4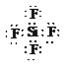 ��
��
��3��D2A2�ǹ������ƣ����еĻ�ѧ��Ϊ���Ӽ����ۼ���
��4����A��C��D����Ԫ����ɵĻ�����M���������ƣ����������������ӻ����M����ˮ������ѧ�仯��ԭ����ֻ�оɼ��Ķ��Ѷ����¼����γ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����8����ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
��1���±��Ǹ�С���о�Ӱ��������⣨H2O2���ֽ����ʵ�����ʱ�ɼ���һ�����ݣ�
��10mL H2O2��ȡ150mLO2�����ʱ�䣨����

�ٸ�С������Ʒ���ʱ��������Ũ�ȡ�a: ��b: �����ضԹ�������ֽ����ʵ�Ӱ�졣
�ڴ�����Ӱ��H2O2�ֽ����ʵ�����a��b����ѡһ����˵�������ضԸ÷�Ӧ���ʵ�Ӱ�죺 ��
��2����������ͬ���ۼ�״̬��ͬ��MnO2�ֱ���뵽5mL 5%��˫��ˮ�У����ô����ǵ�ľ�����ԡ��ⶨ������£�
������MnO2�� | ������� | �۲��� | ��Ӧ��������ʱ�� |
��ĩ״ | ��ϲ��� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5���� |
��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
��д��H2O2�����Ļ�ѧ��Ӧ����ʽ _______________ ______��
��ʵ����˵���������õĴ�С��________ _________ �йء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ�������Ԫ��֮��ԭ�������Ĺ�ϵ��ȷ���ǣ� ��
A.���������Ԫ�ص�ԭ������֮��һ������1
B.����������Ԫ�ص�ԭ������֮��ֻ��1��11��25
C.��������Ԫ�ص�ԭ������֮��һ������8
D.��������Ԫ�ص�ԭ������֮�������2��8��18��32
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH=13����Һ�У��ܴ���������������ǣ�
A. Na+��NH4+��Cl����SO42�� B. K+��Na+��AlO2����Cl��
C. Mg2+��K+��NO3����Cl�� D. K+��Na+��Al3+��SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ1�Ǽ״�ȼ�ϵ�ع�����ʾ��ͼ������A��B��D��Ϊʯī�缫��CΪͭ�缫������һ��ʱ��Ͽ�K����ʱA��B�����ϲ��������������ͬ��

��1�����и����ĵ缫��ӦʽΪ____________��
��2������B��Ϊ_____����������������������õ����������������ڱ�״���µ����Ϊ____��
��3����װ����Һ�н��������ӵ����ʵ�����ת�Ƶ��ӵ����ʵ����仯��ϵ��ͼ2����ͼ�Т��߱�ʾ����_________________�����������ţ��ı仯����Ӧ������Ҫʹ��װ���н���������ǡ����ȫ��������Ҫ___________ mL 2. 0 mol/L NaOH��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ֹ��2013��12��ĩ���й������������װ�������ﵽ10.66GW����������ۼ�װ�������ﵽ17.I6GW��ͼΪ�����������װ�õ������[CO(NH2)2]�ļ�����Һ�����װ��ʾ��ͼ(�����и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫)��������������ȷ����

A�� N�Ͱ뵼��Ϊ������P�Ͱ뵼��Ϊ����
B������װ����Һ�е�������B������A��
C��X2����
D������ʱ��A���ĵ缫��ӦʽΪCO(NH2) 2+8OH--6e-�TCO32-+N2��+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ���Ȼ�ѧ����ʽ:
(1)1 mol C2H5OH(l)��ȫȼ������CO2(g)��H2O(l),�ų�1 366.8 kJ����: ��
(2)1 mol C(ʯī)������H2O(g)��Ӧ����CO(g)��H2(g),����131.3 kJ����: ��
(3)1.7 g NH3(g)������������Ӧ������̬����,�ų�22.67 kJ������: ��
����֪���з�Ӧ�ķ�Ӧ��Ϊ
��CH3COOH(l)��2O2(g)��2CO2(g)��2H2O(l) ��H1����870.3kJ/mol
��C(s)��O2(g)��CO2(g) ��H2����393.5kJ/mol
��H2(g)��1/2O2(g)��H2O(l) ��H3����285.8kJ/mol
�Լ���������Ӧ�ķ�Ӧ�ȣ�2C(s)��2H2(g)��O2(g)��CH3COOH(l) ��H=_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO2ͨ��BaCl2��Һ�����ͣ�δ���������ɣ�����ͨ����һ�����壬���������tͨ������������
A. CO2 B. NH3 C. NO2 D. Cl2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com