
ΓΨΧβΡΩΓΩ»ιΥα‘Ύ…ζΟϋΜ·―ß÷–Τπ÷Ί“ΣΉς”ΟΘ§“≤ «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§“ρ¥Υ≥…ΈΣΫϋΡξά¥ΒΡ―–ΨΩ»»ΒψΓΘœ¬ΆΦ «ΜώΒΟ»ιΥαΒΡΝΫ÷÷ΖΫΖ®Θ§Τδ÷–A «“Μ÷÷≥ΘΦϊΒΡΧΰΘ§ΥϋΒΡ≤ζΝΩΩ…“‘”Οά¥ΚβΝΩ“ΜΗωΙζΦ“ΒΡ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΓΘ
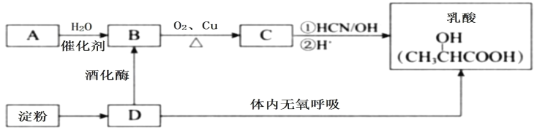
(1)…œ ω”–ΜζΈο÷–”–“Μ÷÷Ω…ΉςΈΣΥ°ΙϊΒΡ¥Ώ λΦΝΘ§ΤδΫαΙΙΦρ Ϋ «___________ΓΘΒμΖέΆξ»ΪΥ°ΫβΒΟΒΫDΘ§DΒΡΟϊ≥Τ «__________Θ§Φλ―ι «ΖώΜΙ”–ΒμΖέΒΡ ‘ΦΝ «_________________________ΓΘ
(2)AΓζBΒΡΖ¥”Πάύ–Ά «_______ΘΜBΓζCΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «__________________________________ΓΘ
(3)BΩ…“‘±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΜρΥα–‘÷ΊΗθΥαΦΊ»ή“Κ÷±Ϋ”―θΜ·ΈΣ”–ΜζΈοEΘ§B”κEΩ…‘Ύ≈®ΝρΥα¥ΏΜ·Ής”Οœ¬Ζ¥”Π…ζ≥…θΞ(C4H8O2)ΓΘ“―÷Σ Β―ι÷–60gE”κΉψΝΩBΖ¥”ΠΚσ…ζ≥…66 gΗΟθΞΘ§‘ρΗΟθΞΒΡ≤ζ¬ ( ΒΦ ≤ζΝΩ’Φάμ¬έ≤ζΝΩΒΡΑΌΖ÷ ΐ)ΈΣ______________ΓΘ
(4)ΈΣΦλ―ιΒμΖέΥ°Ϋβ≤ζΈοΘ§–ΓΟςœρΒμΖέ»ή“Κ÷–Φ”»κœΓΝρΥα≤ΔΦ”»»“ΜΕΈ ±ΦδΘ§ά以ΚσΒΡ»ή“Κ÷–÷±Ϋ”Φ”»κ–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΘ§Φ”»»Θ§ΈόΉ©Κλ…Ϊ≥ΝΒμ≥ωœ÷Θ§Ρψ»œΈΣ–ΓΟς Β―ι ßΑήΒΡ÷ς“Σ‘≠“ρ «_______
(5)»ιΥα”κΧζΖ¥”ΠΩ…÷Τ±Η“Μ÷÷≤ΙΧζ“©ΈοΘ§ΖΫ≥Χ ΫΈΣ(Έ¥≈δΤΫ)ΘΚ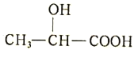 +FeΓζ
+FeΓζ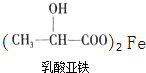 +XΘΜ‘ρ45g»ιΥα”κΧζΖ¥”Π…ζ≥… X ΒΡΧεΜΐΈΣ_______L(±ξΉΦΉ¥Ωω)ΓΘ
+XΘΜ‘ρ45g»ιΥα”κΧζΖ¥”Π…ζ≥… X ΒΡΧεΜΐΈΣ_______L(±ξΉΦΉ¥Ωω)ΓΘ
(6)ΝΫΖ÷Ή”»ιΥα‘Ύ“ΜΕ®ΧθΦΰœ¬Ά®ΙΐθΞΜ·Ζ¥”ΠΩ……ζ≥…“ΜΖ÷Ή”Νυ‘ΣΜΖθΞ(C6H8O4)ΚΆΝΫΖ÷Ή”Υ°Θ§ΗΟΜΖθΞΒΡΫαΙΙΦρ Ϋ «________________________ΓΘ
ΓΨ¥πΑΗΓΩCH2=CH2 ΤœΧ―Χ« ΒβΥ° Φ”≥…Ζ¥”Π 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 75% Έ¥”ΟΦν÷–ΚΆΉς¥ΏΜ·ΦΝΒΡΝρΥα 5.6
2CH3CHO+2H2O 75% Έ¥”ΟΦν÷–ΚΆΉς¥ΏΜ·ΦΝΒΡΝρΥα 5.6 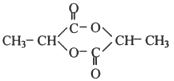
ΓΨΫβΈωΓΩ
A «“Μ÷÷≥ΘΦϊΒΡΧΰΘ§ΥϋΒΡ≤ζΝΩΩ…“‘”Οά¥ΚβΝΩ“ΜΗωΙζΦ“ΒΡ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΘ§‘ρA «CH2=CH2Θ§CH2=CH2”κΥ°ΖΔ…ζΦ”≥…Ζ¥”Π≤ζ…ζB «CH3CH2OHΘ§CH3CH2OH¥ΏΜ·―θΜ·≤ζ…ζC «CH3CHOΘ§CH3CHO”κHCNΖΔ…ζΦ”≥…Ζ¥”ΠΘ§»ΜΚσΥαΜ·Ω…ΒΟ»ιΥαΘΜΒμΖέΥ°Ϋβ≤ζ…ζD «ΤœΧ―Χ«Θ§Ζ÷Ή” Ϋ «C6H12O6Θ§ΤœΧ―Χ«‘ΎΨΤΜ·ΟΗΉς”Οœ¬Ζ¥”Π≤ζ…ζ““¥ΦΘΚCH3CH2OHΘΜΤœΧ―Χ«‘ΎΧεΡΎ‘ΎΈό―θΚτΈϋΡήΙΜ―θΜ·≤ζ…ζ»ιΥαΘΜ““¥ΦΩ…“‘±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΜρΥα–‘÷ΊΗθΥαΦΊ»ή“Κ÷±Ϋ”―θΜ·ΈΣ”–ΜζΈοE «CH3COOHΘ§»ΜΚσΗυΨίΈ Χβ÷π“ΜΖ÷ΈωΫβ¥πΓΘ
ΗυΨί…œ ωΖ÷ΈωΩ…÷ΣΘΚA «CH2=CH2Θ§B «CH3CH2OHΘ§C «CH3CHOΘ§D «ΤœΧ―Χ«Θ§Ζ÷Ή” Ϋ «C6H12O6Θ§E «CH3COOHΓΘ
(1)““œ© «“Μ÷÷÷≤ΈοΦΛΥΊΘ§ΡήΙΜ¥ΌΫχ÷≤ΈοΒΡ…ζ≥ΛΓΔΖΔ”ΐΘ§Ω…ΉςΈΣΥ°ΙϊΒΡ¥Ώ λΦΝΘ§ΤδΫαΙΙΦρ Ϋ «CH2=CH2ΘΜΒμΖέΆξ»ΪΥ°ΫβΒΟΒΫΤœΧ―Χ«Θ§Ι Έο÷ DΒΡΟϊ≥Τ «ΤœΧ―Χ«ΘΜ”…”ΎΒμΖέ”ωΒβΒΞ÷ Μα±δΈΣάΕ…ΪΘ§“ρ¥ΥΦλ―ι «ΖώΜΙ”–ΒμΖέΒΡ ‘ΦΝ «ΒβΥ°ΘΜ
(2)CH2=CH2”κΥ°ΖΔ…ζΦ”≥…Ζ¥”Π≤ζ…ζCH3CH2OHΘ§Ι AΓζBΒΡΖ¥”Πάύ–Ά «Φ”≥…Ζ¥”ΠΘΜ““¥Φ”κO2‘ΎCuΉς¥ΏΜ·ΦΝΧθΦΰœ¬Θ§Φ”»»Θ§ΖΔ…ζ―θΜ·Ζ¥”Π≤ζ…ζCH3CHOΘ§ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ2CH3CH2OH+O2![]() 2CH3CHO+2H2OΘΜ
2CH3CHO+2H2OΘΜ
(3)B «CH3CH2OHΘ§Ω…“‘±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΜρΥα–‘÷ΊΗθΥαΦΊ»ή“Κ÷±Ϋ”―θΜ·ΈΣ”–ΜζΈοE «CH3COOHΘ§CH3CH2OH”κCH3COOHΩ…‘Ύ≈®ΝρΥα¥ΏΜ·Ής”Οœ¬Ζ¥”Π…ζ≥…““Υα““θΞ(C4H8O2)Θ§ΤδΫαΙΙΦρ Ϋ «CH3COOC2H5ΓΘ‘Ύ Β―ι÷–60 g ““ΥαΒΡΈο÷ ΒΡΝΩ «1 molΘ§»τΆξ»ΪΖ¥”Π≤ζ…ζΒΡ““Υα““θΞΒΡ÷ ΝΩ «88 gΘ§ ΒΦ …œ1 mol““Υα”κΉψΝΩBΖ¥”ΠΚσ…ζ≥…66 gΗΟθΞΘ§‘ρ≤ζ…ζΗΟθΞΒΡ≤ζ¬ ΈΣ![]() ΓΝ100%=75%ΘΜ
ΓΝ100%=75%ΘΜ
(4)ΒμΖέΥ°Ϋβ–η‘ΎœΓΝρΥα¥ΏΜ·œ¬Ϋχ––Θ§“ΣΦλ―ιΒμΖέΥ°Ϋβ≤ζΈοΤœΧ―Χ«ΒΡ¥φ‘Ύ”ΠΗΟ‘ΎΦν–‘ΜΖΨ≥÷–Ϋχ––Θ§“ρ¥Υ–ηœ»”ΟΦνΫΪ¥ΏΜ·ΦΝΝρΥα÷–ΚΆΓΘΕχ–ΓΟςœρΒμΖέ»ή“Κ÷–Φ”»κœΓΝρΥα≤ΔΦ”»»“ΜΕΈ ±ΦδΘ§ά以ΚσΒΡ»ή“Κ÷–÷±Ϋ”Φ”»κ–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΘ§≤ΔΟΜ”–Φ”»κΦν÷–ΚΆΝρΥαΘ§ΨΆ÷±Ϋ”Φ”»»Θ§Υυ“‘ΈόΉ©Κλ…Ϊ≥ΝΒμ≥ωœ÷Θ§‘ρ–ΓΟς Β―ι ßΑήΒΡ÷ς“Σ‘≠“ρ «Έ¥”ΟΦν÷–ΚΆΉς¥ΏΜ·ΦΝΒΡΥαΘΜ
(5)»ιΥα”κFeΖ¥”Π≤ζ…ζ»ιΥα―«ΧζΚΆ«βΤχΘ§Εΰ’ΏΖ¥”ΠΒΡΈο÷ ΒΡΝΩΒΡ±» «2ΘΚ1Θ§2 mol»ιΥαΖ¥”ΠΜα≤ζ…ζ1 mol H2Θ§45 g»ιΥαΒΡΈο÷ ΒΡΝΩ «n(»ιΥα)=45 gΓ¬90 g/mol=0.5 molΘ§‘ρΤδΆξ»Ϊ”κFeΖ¥”Π≤ζ…ζH2ΒΡΈο÷ ΒΡΝΩn(H2)=![]() n(»ιΥα)=
n(»ιΥα)=![]() ΓΝ0.5 mol=0.25 molΘ§Τδ‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐV(H2)=0.25 molΓΝ22.4 L/mol=5.6 LΘΜ
ΓΝ0.5 mol=0.25 molΘ§Τδ‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐV(H2)=0.25 molΓΝ22.4 L/mol=5.6 LΘΜ
(6)ΝΫΖ÷Ή”»ιΥα‘Ύ“ΜΕ®ΧθΦΰœ¬Ά®ΙΐθΞΜ·Ζ¥”ΠΩ……ζ≥…“ΜΖ÷Ή”Νυ‘ΣΜΖθΞ(C6H8O4)ΚΆΝΫΖ÷Ή”Υ°Θ§ΗυΨίθΞΜ·Ζ¥”ΠΆ―Υ°ΖΫ ΫΘΚΥαΆ―τ«ΜυΘ§¥ΦΆ―«βΘ§Ω…÷Σ≤ζ…ζΒΡΗΟΜΖθΞΒΡΫαΙΙΦρ Ϋ « ΓΘ
ΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΝΉΨΪΩσ ΣΖ®÷Τ±ΗΝΉΥαΒΡ“Μ÷÷ΙΛ“’Νς≥Χ»γœ¬ΘΚ

“―÷ΣΘΚΝΉΨΪΩσ÷ς“Σ≥…Ζ÷ΈΣCa5(PO4)3(OH)Θ§ΜΙΚ§”–Ca5(PO4)3FΚΆ”–ΜζΧΦΒ»ΓΘ»ήΫβΕ»ΘΚCa5(PO4)3(OH)<CaSO4ΓΛ0.5H2O
Θ®1Θ©…œ ωΝς≥Χ÷–ΡήΦ”ΩλΖ¥”ΠΥΌ¬ ΒΡ¥κ ©”–___ΓΘ
Θ®2Θ©ΝΉΨΪΩσΖέΥαΫΰ ±ΖΔ…ζΖ¥”ΠΘΚ2Ca5(PO4)3(OH)+3H2O+10H2SO4![]() 10CaSO4ΓΛ0.5H2O+6H3PO4
10CaSO4ΓΛ0.5H2O+6H3PO4
ΔΌΗΟΖ¥”ΠΧεœ÷≥ωΥα–‘ΙΊœΒΘΚH3PO4___H2SO4Θ®ΧνΓΑ>Γ±ΜρΓΑ<Γ±Θ©ΓΘ
ΔΎΫαΚœ‘ΣΥΊ÷ήΤΎ¬…Ϋβ ΆΔΌ÷–Ϋα¬έΘΚPΚΆSΒγΉ”≤ψ ΐœύΆ§Θ§___ΓΘ
Θ®3Θ©ΥαΫΰ ±Θ§ΝΉΨΪΩσ÷–Ca5(PO4)3FΥυΚ§ΖζΉΣΜ·ΈΣHFΘ§≤ΔΫχ“Μ≤ΫΉΣΜ·ΈΣSiF4≥ΐ»ΞΓΘ–¥≥ω…ζ≥…HFΒΡΜ·―ßΖΫ≥Χ ΫΘΚ__ΓΘ
Θ®4Θ©H2O2ΫΪ¥÷ΝΉΥα÷–ΒΡ”–ΜζΧΦ―θΜ·ΈΣCO2Ά―≥ΐΘ§Ά§ ±Ή‘…μ“≤ΜαΖΔ…ζΖ÷ΫβΓΘœύΆ§ΆΕΝœ±»ΓΔœύΆ§Ζ¥”Π ±ΦδΘ§≤ΜΆ§Έ¬Ε»œ¬ΒΡ”–ΜζΧΦΆ―≥ΐ¬ »γΆΦΥυ ΨΓΘ80ΓφΚσΆ―≥ΐ¬ ±δΜ·ΒΡ‘≠“ρΘΚ___ΓΘ
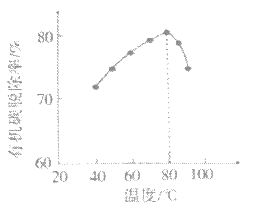
Θ®5Θ©Ά―Νρ ±Θ§CaCO3…‘ΙΐΝΩΘ§≥δΖ÷Ζ¥”ΠΚσ»‘”–SO42Θ≠≤–ΝτΘ§Φ”»κBaCO3Ω…Ϋχ“Μ≤ΫΧαΗΏΝρΒΡΆ―≥ΐ¬ Θ§ΤδάκΉ”ΖΫ≥Χ Ϋ «__ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥τ―θ‘Ύ―ΧΤχΆ―œθ÷–ΒΡΖ¥”ΠΈΣ2NO2(g)+O3(g)![]() N2O5(g)+O2(g)ΓΘ»τ¥ΥΖ¥”Π‘ΎΚψ»ίΟή±’»ίΤς÷–Ϋχ––Θ§œ¬Ν–―Γœν÷–”–ΙΊΆΦœσΕ‘”ΠΒΡΖ÷Έω’ΐ»ΖΒΡ «Θ® Θ©
N2O5(g)+O2(g)ΓΘ»τ¥ΥΖ¥”Π‘ΎΚψ»ίΟή±’»ίΤς÷–Ϋχ––Θ§œ¬Ν–―Γœν÷–”–ΙΊΆΦœσΕ‘”ΠΒΡΖ÷Έω’ΐ»ΖΒΡ «Θ® Θ©
A.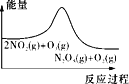 ΤΫΚβΚσ…ΐΈ¬Θ§NO2Κ§ΝΩΫΒΒΆ
ΤΫΚβΚσ…ΐΈ¬Θ§NO2Κ§ΝΩΫΒΒΆ
B.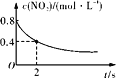 0ΓΪ2 sΡΎΘ§v(O3)ΘΫ0.2 molΓΛLΘ≠1ΓΛsΘ≠1
0ΓΪ2 sΡΎΘ§v(O3)ΘΫ0.2 molΓΛLΘ≠1ΓΛsΘ≠1
C.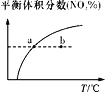 v’ΐΘΚbΒψ>aΒψΘ§bΒψΘΚvΡφ > v’ΐ
v’ΐΘΚbΒψ>aΒψΘ§bΒψΘΚvΡφ > v’ΐ
D.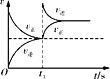 ΚψΈ¬Θ§t1 ±‘Ό≥δ»κO3
ΚψΈ¬Θ§t1 ±‘Ό≥δ»κO3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩXΓΔYΓΔZ»ΐ÷÷ΤχΧεΕΦΡήΕ‘¥σΤχ‘λ≥…Έέ»ΨΘ§‘ΎΙΛ“Β…œΕΦΩ…“‘”ΟΦν“ΚΈϋ ’ΓΘ“―÷ΣX «Μ· ·»ΦΝœ»Φ…’≤ζΈο÷°“ΜΘ§ «–Έ≥…Υα”ξΒΡ÷ς“ΣΈο÷ ΘΜY «“Μ÷÷ΒΞ÷ Θ§ΥϋΒΡΥ°»ή“ΚΨΏ”–Τ·ΑΉΉς”ΟΘΜZ «œθΥαΙΛ“ΒΚΆΤϊ≥ΒΈ≤Τχ÷–ΒΡ”–ΚΠΈο÷ ÷°“ΜΘ§Ρή”κΥ°Ζ¥”ΠΓΘ«κ–¥≥ωœ¬Ν–Έο÷ Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΘ
(1)X‘Ύ“ΜΕ®ΧθΦΰœ¬”κ―θΤχΖ¥”Π____________________________________ΘΜ
(2)Y”κ«β―θΜ·ΡΤ»ή“ΚΒΡΖ¥”Π______________________________________ΘΜ
(3)Z”κΥ°ΒΡΖ¥”Π________________________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ1905ΡξΙΰγξΩΣΖΔ Βœ÷ΝΥ“‘ΒΣΤχΚΆ«βΤχΈΣ‘≠ΝœΚœ≥…Α±ΤχΘ§…ζ≤ζΒΡΑ±÷Τ‘λΒΣΖ ΖΰΈώ”Ύ≈©“ΒΘ§―χΜνΝΥΒΊ«ρ»ΐΖ÷÷°“ΜΒΡ»ΥΩΎΘ§Ιΰγξ“≤“ρ¥ΥΜώΒΟΝΥ1918ΡξΒΡ≈Β±¥ΕϊΜ·―ßΫ±ΓΘ
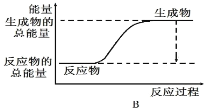
(1)ΙΛ“ΒΚœ≥…Α±ΒΡΖ¥”Π»γœ¬ΘΚN2+3H2 2NH3ΓΘ“―÷ΣΕœΝ―1 mol N2÷–ΒΡΙ≤ΦέΦϋΈϋ ’ΒΡΡήΝΩΈΣ946 kJΘ§ΕœΝ―1 mol H2÷–ΒΡΙ≤ΦέΦϋΈϋ ’ΒΡΡήΝΩΈΣ436 kJΘ§–Έ≥…1 mol N-HΦϋΖ≈≥ωΒΡΡήΝΩΈΣ391 kJΘ§‘ρ”…N2ΚΆH2…ζ≥…2 mol NH3 ΒΡΡήΝΩ±δΜ·ΈΣ__________kJΓΘ œ¬ΆΦΡή’ΐ»Ζ±μ ΨΗΟΖ¥”Π÷–ΡήΝΩ±δΜ·ΒΡ «__________(ΧνΓΑAΓ±ΜρΓΑBΓ±)ΓΘ
2NH3ΓΘ“―÷ΣΕœΝ―1 mol N2÷–ΒΡΙ≤ΦέΦϋΈϋ ’ΒΡΡήΝΩΈΣ946 kJΘ§ΕœΝ―1 mol H2÷–ΒΡΙ≤ΦέΦϋΈϋ ’ΒΡΡήΝΩΈΣ436 kJΘ§–Έ≥…1 mol N-HΦϋΖ≈≥ωΒΡΡήΝΩΈΣ391 kJΘ§‘ρ”…N2ΚΆH2…ζ≥…2 mol NH3 ΒΡΡήΝΩ±δΜ·ΈΣ__________kJΓΘ œ¬ΆΦΡή’ΐ»Ζ±μ ΨΗΟΖ¥”Π÷–ΡήΝΩ±δΜ·ΒΡ «__________(ΧνΓΑAΓ±ΜρΓΑBΓ±)ΓΘ

(2)Ζ¥”Π2NH3(g)![]() N2(g)+3H2(g)‘Ύ»ΐ÷÷≤ΜΆ§ΧθΦΰœ¬Ϋχ––Θ§N2ΓΔH2ΒΡΤπ Φ≈®Ε»ΈΣ 0Θ§Ζ¥”ΠΈοNH3ΒΡ≈®Ε»(mol/L)Υφ ±Φδ(min)ΒΡ±δΜ·«ιΩω»γœ¬±μΥυ ΨΓΘ
N2(g)+3H2(g)‘Ύ»ΐ÷÷≤ΜΆ§ΧθΦΰœ¬Ϋχ––Θ§N2ΓΔH2ΒΡΤπ Φ≈®Ε»ΈΣ 0Θ§Ζ¥”ΠΈοNH3ΒΡ≈®Ε»(mol/L)Υφ ±Φδ(min)ΒΡ±δΜ·«ιΩω»γœ¬±μΥυ ΨΓΘ
Β―ι–ρΚ≈ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
ΔΌ | 400Γφ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
ΔΎ | 400Γφ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
Δέ | 500Γφ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
ΗυΨί…œ ω ΐΨίΜΊ¥πΘΚ Β―ιΔΌΔΎ÷–Θ§”–“ΜΗω Β―ι Ι”ΟΝΥ¥ΏΜ·ΦΝΘ§Υϋ « Β―ι_____(Χν–ρΚ≈)ΘΜ Β―ιΔΌΔέΕ‘±»ΥΒΟςΝΥ_________________________________ΓΘ‘ΎΚψΈ¬Κψ»ίΧθΦΰœ¬Θ§≈–ΕœΗΟΖ¥”Π¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§ΒΡ±ξ÷Ψ «_________(Χν–ρΚ≈)ΓΘ
a. NH3ΒΡ’ΐΖ¥”ΠΥΌ¬ Β»”ΎΡφΖ¥”ΠΥΌ¬ b.ΜλΚœΤχΧεΒΡΟήΕ»≤Μ±δ
c.ΜλΚœΤχΧεΒΡ―Ι«Ω≤Μ±δ d.c(NH3)=c(H2)
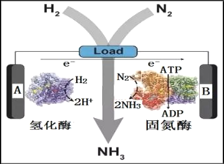
(3)Ϋϋ»’ΟάΙζ”ΧΥϊ¥σ―ß MinteerΫΧ Ύ≥…ΙΠΙΙ÷ΰΝΥH2ΓΣN2…ζΈο»ΦΝœΒγ≥ΊΓΘΗΟΒγ≥ΊάύΥΤ»ΦΝœΒγ≥Ί‘≠άμΘ§“‘ΒΣΤχΚΆ«βΤχΈΣ‘≠ΝœΓΔ«βΜ·ΟΗΚΆΙΧΒΣΟΗΈΣΝΫΦΪ¥ΏΜ·ΦΝΓΔ÷ Ή”ΫΜΜΜΡΛ(ΡήΙΜ¥ΪΒίH+)ΈΣΗτΡΛΘ§‘Ύ “Έ¬ΧθΦΰœ¬Φ¥ Βœ÷ΝΥΑ±ΒΡΚœ≥…Ά§ ±ΜΙΡήΧαΙ©ΒγΡήΓΘ‘ρAΒγΦΪΈΣ_____ΦΪ(ΧνΓΑ’ΐΓ±ΓΔΓΑΗΚΓ±)Θ§ΗΟΒγ≥ΊΖ≈Βγ ±»ή“Κ÷–ΒΡH+œρ______ΦΪ“ΤΕ·(ΧνΓΑAΓ±ΓΔΓΑBΓ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΖά…ΙΥΣ÷°Υυ“‘Ρή”––ßΒΊΦθ«αΉœΆβœΏΕ‘»ΥΧεΒΡ…ΥΚΠΘ§ «“ρΈΣΥϋΥυΚ§ΒΡ”––ß≥…Ζ÷ΒΡΖ÷Ή”÷–Κ§”–Π–ΦϋΘ§’β–©”––ß≥…Ζ÷ΒΡΖ÷Ή”÷–ΒΡΠ–ΒγΉ”Ω…‘ΎΈϋ ’ΉœΆβœΏΚσ±ΜΦΛΖΔΘ§¥”ΕχΉηΒ≤≤ΩΖ÷ΉœΆβœΏΕ‘ΤΛΖτΒΡ…ΥΚΠΓΘœ¬Ν–Έο÷ ÷–ΟΜ”–Ζά…Ι–ßΙϊΒΡ «Θ® Θ©
A.Ε‘Α±Μυ±ΫΦΉΥα
B.τ«Μυ±ϊΆΣ![]()
C.»βΙπΥα(C6H5-CH=CH-COOH)
D.““¥Φ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A.»»ΒΡ¥ΩΦν“Κ»Ξ”ΆΈέ–ßΙϊΚΟΘ§“ρΈΣΦ”»»Ω… ΙCO32Θ≠ΒΡΥ°Ϋβ≥ΧΕ»‘ω¥σΘ§»ή“ΚΦν–‘‘ω«ΩΘ§»ΞΈέΝΠ‘ω«Ω
B.Χζ‘Ύ≥± ΣΒΡΜΖΨ≥œ¬…ζ–β“‘ΦΑMg”κNH4Cl»ή“ΚΖ¥”Π…ζ≥…H2ΕΦ”κ―ΈάύΥ°Ϋβ”–ΙΊ
C.ΫΪAl2(SO4)3»ή“ΚΦ”»»ΓΔ’τΗ…ΓΔΉΤ…’Θ§Ω…ΒΟΒΫΙΧΧεAl2(SO4)3
D.ΫΪ±ΞΚΆFeCl3»ή“ΚΒΈ»κΖ–Υ°÷–÷ΤΫΚΧεΘ§άκΉ”ΖΫ≥Χ ΫΘΚFe3+ΘΪ3H2O![]() Fe(OH)3(ΫΚΧε) ΘΪ3HΘΪ
Fe(OH)3(ΫΚΧε) ΘΪ3HΘΪ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»ΦΝœΒγ≥Ί «»ΦΝœ(»γ«βΤχΓΔΦΉΆιΓΔ“Μ―θΜ·ΧΦΒ»)Ηζ―θΤχ(ΜρΩ’Τχ)ΤπΖ¥”ΠΫΪΜ·―ßΡήΉΣ±δΈΣΒγΡήΒΡΉΑ÷ΟΘ§ΒγΫβ÷ »ή“Κ ««ΩΦν»ή“ΚΓΘœ¬ΟφΙΊ”ΎΦΉΆι»ΦΝœΒγ≥ΊΒΡΥΒΖ®’ΐ»ΖΒΡ «(ΓΓΓΓ)
A. ΗΚΦΪΖ¥”Π ΫΘΚO2ΘΪ2H2OΘΪ4eΘ≠![]() 4OHΘ≠
4OHΘ≠
B. ΗΚΦΪΖ¥”Π ΫΘΚCH4ΘΪ8OHΘ≠Θ≠8eΘ≠![]() CO2ΘΪ6H2O
CO2ΘΪ6H2O
C. ΥφΉ≈Ζ≈ΒγΒΡΫχ––Θ§»ή“Κ÷–«β―θΗυάκΉ”ΒΡ≈®Ε»≤Μ±δ
D. Ζ≈Βγ ±»ή“Κ÷–ΒΡ“θάκΉ”œρΗΚΦΪ“ΤΕ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“άΨίΆΦ÷–ΒΣ‘ΣΥΊΦΑΤδΜ·ΚœΈοΒΡΉΣΜ·ΙΊœΒΘ§≈–Εœœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©

A. X «N2O5
B. Ω…”Ο≈≈Υ°Ζ® ’Φ·NOΓΔNO2ΤχΧε
C. ΙΛ“Β…œ“‘NH3ΓΔΩ’ΤχΓΔΥ°ΈΣ‘≠Νœ…ζ≤ζœθΥα
D. ”…NH3ΓζN2Θ§¥”‘≠άμ…œΩ¥Θ§NH3Ω…”κNO2Ζ¥”Π Βœ÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com