
【题目】某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
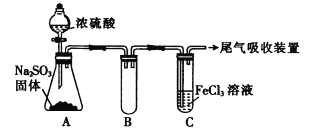
(1) 反应开始一段时间后,装置C中的现象为__________。
(2) 根据以上现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
① 写出SO2与FeCl3溶液反应的离子方程式:____________。
② 向装置C中通入足量SO2发生反应后,检验生成的Fe2+的方法是__________。
③该小组同学向反应后的装置C的试管中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,则证明反应生成了SO42-。该做法不合理的理由是__________________。
(3)若将装置C中FeCl3溶液更换为Fe(NO3)3和BaCl2的混合液,可观察到装置C中出现白色沉淀,该小组对装置C中产生沉淀的原因提出下列假设(不考虑各因素的叠加):
假设1:装置A中白雾进入装置C中参与反应。
假设2: _______________________。
假设3:在酸性条件下NO3-能氧化SO2。
(4)请你设计实验验证上述假设3,写出实验步骤、预期现象和结论。
实验步骤(简述操作过程) | 预期现象和结论 |
① ② ③ |
【答案】
(1)溶液由棕黄色变为浅绿色;
(2)①2Fe3+ +SO2 +2H2O =SO42- +4H+ +2Fe2+ ;
②取少量反应后的溶液于试管中,向其中滴人KSCN溶液,不变红,再滴加适量新制的氯水(或H2O2溶液等),溶液变红;
③硝酸可以将溶解的SO2氧化为H2SO4,干扰实验;
(3)SO2被 Fe3+氧化为SO42- ;
(4)
实验步骤(简述操作过程) | 预期现象和结论 |
①取适量Ba(NO3)2溶液于试管中; ②向试管中通入过量SO2气体; ③再向试管中加入过量盐酸 | 若先有白色沉淀生成,加入盐酸后沉淀不消失,则假设3成立 |
【解析】
试题分析:(1)通入足量SO2时C中发生二氧化硫与氯化铁的氧化还原反应,生成硫酸亚铁,则观察到溶液由棕黄色变为浅绿色,故答案为:溶液由棕黄色变为浅绿色;
(2)①发生氧化还原反应,生成硫酸根离子、亚铁离子,离子反应为2Fe3++SO2+2H2O=SO42-+4H++2Fe2+,故答案为:2Fe3++SO2+2H2O=SO42-+4H++2Fe2+;
②检验有Fe2+生成的实验方法为:取C中反应后的溶液,向其中滴入KSCN溶液,不变红,再加入新制的氯水,溶液变红,故答案为:取C中反应后的溶液,向其中滴入KSCN溶液,不变红,再加入新制的氯水,溶液变红;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,硝酸具有强氧化性,则硝酸可以将溶解的SO2氧化为 H2SO4,干扰试验,故做法不合理,故答案为:不合理;硝酸可以将溶解的SO2氧化为 H2SO4,干扰试验;
(3)假设1:装置A中白雾进入装置C中参与反应。假设2: SO2被Fe3+氧化了生成了SO42-。假设3:在酸性条件下NO3-能氧化SO2。故答案为:SO2被Fe3+氧化了生成了SO42-;
(4)假如SO2与NO3-反应,则可设计如下实验进行验证:①取适量Ba(NO3)2溶液于试管中;②向试管中通入过量SO2气体;③再向试管中加入过量盐酸,若先有白色沉淀生成,加入盐酸后沉淀不消失,则假设3成立,故答案为:
实验步骤(简述操作过程) | 预期现象和结论 |
①取适量Ba(NO3)2溶液于试管中; ②向试管中通入过量SO2气体; ③再向试管中加入过量盐酸 | 若先有白色沉淀生成,加入盐酸后沉淀不消失,则假设3成立 |


科目:高中化学 来源: 题型:
【题目】已知:KClO3 + 6HCl(浓)→ KCl + 3Cl2 + 3H2O,氧化产物与还原产物物质的量之比为( )
A. 5 : 1 B. 1 : 5 C. 6 : 1 D. 1 : 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的恒容两个密闭容器中分别 加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
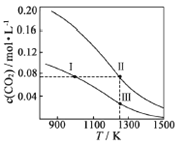
A.化学平衡常数K:K(状态I) < K(状态II) <K(状态III)
B.CO2的平衡转化率α:α(状态I) <α(状态Ⅱ)=α(状态III)
C.体系中c(CO):c (CO,状态Ⅱ) < 2c (CO,状态Ⅲ)
D.逆反应速率v逆:v逆(状态Ⅰ)> v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:H2(g) + I2(g) ![]() 2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深
D.容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中,按熔点由高到低的顺序排列正确的是( )
A. CH4>SiH4>GeH4>SnH4
B. KCl>NaCl>MgCl2>MgO
C. Rb>K>Na>Li
D. 石墨>金刚石>SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种固态物质熔化或升华时,克服的微粒间相互作用力属于同种类型的是( )
A. 碘和氯化钾 B. 金刚石和重晶石
C. 二氧化硅和干冰 D. 二氧化碳和甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的( )
①钠比水轻②钠的熔点较低③钠与水反应时要放出热量④钠与水反应后溶液呈碱性
A.①④ B.①②④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是
A. 爆竹燃放后,硫燃烧生成SO3 B. 硅胶可用作商品包装袋的干燥剂
C. 次氯酸钠溶液可用作环境的杀菌消毒 D. 施肥时,草木灰不能与铵态氮肥混合使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Al、C12、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
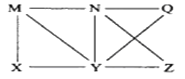
A.N一定是HCl(aq) B.X可能为Al或C12
C.Y一定为NaOH(aq) D.Q、Z中的一种必定为Al2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com