
【题目】人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用酸性KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品小Ca2+的浓度。
[配制酸性KMnO4标准溶液]如图是配制250mL酸性KMnO4标准溶液的过程示意图。
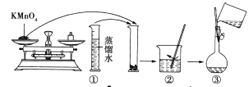
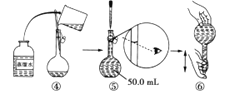
(1)请你观察图示判断其中不正确的操作有(填序号)_____。
(2)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测得的实验结果将____(填“偏大”或“偏小”或“无影响”)。
[测定血液样品中Ca2+的浓度]抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL酸性KMnO4溶液。
(3)已知草酸跟酸性KMnO4溶液反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则式中的x=___。
(4)滴定时,根据现象___,即可确定反应达到终点。
(5)经过计算,血液样品中Ca2+的浓度为____mg/cm3。
【答案】①⑤ 偏大 2 溶液由无色变为紫红色,且半分钟内不褪色 1.2
【解析】
(1)根据配制一定物质的量浓度的溶液的操作方法分析;
(2)仰视刻度线,会使溶液体积偏大,导致标准液浓度偏低;
(3)滴定时,用高锰酸钾滴定草酸,反应达到终点时,滴入的高锰酸钾溶液不褪色,据此判断;
(4)根据滴定数据及钙离子与高锰酸钾的关系式计算出血液样品中Ca2+的浓度。
(1)量筒不能用于溶解固体,视线应该与凹液面的最低点相平读数,所以①⑤操作错误;
(2)仰视定容时,所加的水超过刻度线,体积偏大,所以浓度偏小,滴定草酸消耗体积大,所以会使实验结果偏大。
(3)滴定时,用高锰酸钾滴定草酸,反应达到终点时的现象为溶液由无色变为紫红色,且半分钟内不褪色;
(4)血样20.00mL经过上述处理后得到草酸,草酸消耗的高锰酸钾的物质的量为:0.020mol/L×0.012L=2.4×10-4mol;根据反应方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,及草酸钙的化学式CaC2O4,可知:n(Ca2+)=n(H2C2O4)=![]() n(MnO4-)=2.5×2.4×10-4mol=6×10-4mol,Ca2+的质量为:40g/mol×6×10-4mol=0.024g,则钙离子的浓度为:c(Ca2+)=
n(MnO4-)=2.5×2.4×10-4mol=6×10-4mol,Ca2+的质量为:40g/mol×6×10-4mol=0.024g,则钙离子的浓度为:c(Ca2+)=![]() =1.2mg/cm3。
=1.2mg/cm3。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】异丁酸-3-苯丙酯(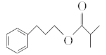 )是一种香料,下图是这种香料的一种合成路线:
)是一种香料,下图是这种香料的一种合成路线:
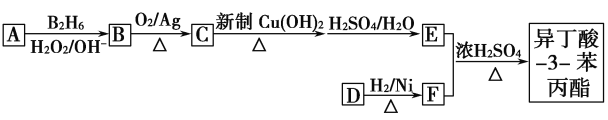
已知以下信息:
①有机物E的摩尔质量为88 g·mol-1,其核磁共振氢谱表明含有3种不同环境的氢原子。
②有机物F是苯甲醇的同系物。
③R—CH==CH2![]() R—CH2CH2OH。
R—CH2CH2OH。
请回答下列问题:
(1)异丁酸-3-苯丙酯的分子式为________________。
(2)A分子中的官能团名称为________________。
(3)C的结构简式为________________。
(4)一定条件下,1 mol D与2 mol H2能够完全反应生成F,D能够发生银镜反应,因此D生成F的反应类型为________________。
(5)E、F反应生成异丁酸-3-苯丙酯的化学方程式为________________________。
(6)已知有机化合物甲符合下列条件:
①与F是同分异构体;②苯环上有3个支链;③核磁共振氢谱显示其含有5种不同环境的氢原子,且不同环境的氢原子个数比为6∶2∶2∶1∶1;④与FeCl3溶液不能发生显色反应。
写出符合上述条件的有机物甲的结构简式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。“茶倍健”牙膏中就添加有某种茶多酚——没食子儿茶素(EGC),其结构如图所示。下列关于没食子儿茶素(EGC)的叙述中不正确的是( )
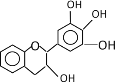
A. 遇FeCl3溶液能发生显色反应
B. 1molEGC与4molNaOH恰好完全反应
C. 1molEGC与3molNa2CO3恰好完全反应
D. 易发生氧化反应和取代反应,难发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2广泛用于造纸工业、污水处理等,其漂白能力是漂白粉的4~5倍。工业上用ClO2气体制NaClO2的工艺流程如图:
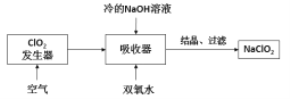
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,高于38℃时析出NaClO2。
下列说法不正确的是( )
A. 吸收器中生成NaClO2的离子方程式:2ClO2+2OHˉ+H2O2=2ClO2ˉ+O2+2H2O
B. 提高吸收器中的反应温度可以提高反应速率,也提高反应物的利用率
C. 流程中的结晶、过滤操作应该是蒸发结晶、趁热过滤
D. 发生器中反应结束后,向其中通入一定量空气的目的是驱赶出ClO2,使其被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Na2O2因能发生下列反应被用作补氧剂:2Na2O2+2CO2=2Na2CO3+O2,上述反应中,氧化剂与还原剂的物质的量之比为:___。
(2)某潜艇上有50人,每人每分钟消耗1.12LO2(标况),则一天需___molNa2O2。如用KO2作补氧剂,写出它和CO2反应的化学方程式_____。
①1kgNa2O2和1kgKO2分别和足量的CO2反应,生成O2的体积(同温同压)比为_____。
②等量的CO2分别和足量的Na2O2、KO2反应,生成O2的分子数(同温同压)比为____。
③你认为选用____作补氧剂更为合适,理由是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应,同时获得副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下:

根据要求填空:
(1)导管a的作用是______________________。B装置有三种功能;①干燥混合气体;②将气体混合均匀;③___________________________。
(2)C装置中CH4与Cl2反应生成一氯代物的化学反应方式是_______________________。
D装置中的石棉上均匀附着潮湿的KI,写出反应的离子方程式是____________________。
(3)E装置中除了有盐酸生成外,还含有有机物。从E中分离出盐酸的最佳方法为___________
(4)E装置的作用是____________。(填序号)。
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
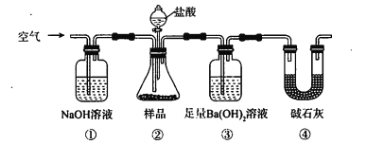
下列说法不正确的是
A. 必须在②③间添加吸收HCl的装置
B. ④的作用是防止空气中的气体影响实验的精确度
C. 通入空气的作用是保证②中产生的气体完全转移到③中
D. 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在最新的家用汽车的调查中发现,新车中气体的质量不符合标准.汽车污染主要来源于汽车配件及材料,它们都会产生大量的有毒有机物.其中一种有毒物质A,为了测定有机物A的结构,做如下实验:
①将9.2g该有机物完全燃烧,生成标况下15.68L的CO2和7.2g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
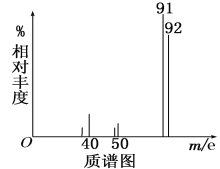
(1)则由图可知该分子的相对分子质量是________,有机物A的分子式为_________。
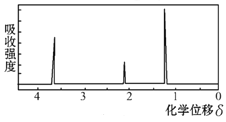
(2)用核磁共振仪处理该化合物,得到如下图所示图谱,图中四个峰的面积之比是1∶2∶2:3,则有机物的名称为________,其苯环上的一氯代物有_______种。若将有机物A与氢气完全加成,则加成后的有机物的一氯代物共有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com