
【题目】金属钠与水的反应是中学化学中的一个重要反应。高一化学教材中该实验曾出现过几种不同的演示方法。分别如下图中(A)(B)(C)所示:

(1)现按图(A)所示的方法,在室温时,向盛有饱和Na2CO3溶液(滴有几滴酚酞)的烧杯中,加入一小块金属钠。
①不可能观察到的现象是___________(填字母代号)。
A.钠浮在液面上,并四处游动,最后消失
B.反应过程中钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色
D.恢复到室温时,烧杯底部有固体物质析出
②按图(B)所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体,在相同条件下体积最大的是______(填字母代号)。
A.用扎有小孔的铝箔包住钠
B.用扎有小孔的铜箔包住钠
C.直接将钠投人水中
(2)按图(C)所示的方法进行该实验,若500mL的矿泉水瓶开始时装有477.6mL水,用手挤压矿泉水瓶至水刚好充满矿泉水瓶并塞紧带有钠的塞子,要使倒置的矿泉水瓶正好恢复原状,假设矿泉水瓶内外均为标准状况,则大头针上扎着的钠粒质量约为_______g。
(3)1998年全国高考试题中的实验题就是根据图(B)的原理设计的。题目及部分答案如下:测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:800毫升烧杯、10毫升量筒、短颈玻离漏斗、长颈漏斗、玻璃棒、铜网、铝锌合金样品、浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应产生的气体体积不超过100毫升。)
I、补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):

①将称量后的合金样品用铜网小心包裹好,放在800毫升烧杯底部,把短颈漏斗倒扣在样品上面。……
[答案]
②往烧杯中注入水,直至水面没过漏斗颈。[评分标准,凡加水改为加酸者,不论其他后续步骤是否正确,本小题一律0分]
③在100毫升量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中。烧杯中水面到杯口至少保留约100毫升空间。
④将“仪器A”插入烧杯并接近烧杯底部,通过它慢慢加入浓盐酸,至有气体产生。
回答下列问题:
a.合金样品用用铜网包裹的目的是______________。
b.为什么在“②往烧杯中注入水,直至水面没过漏斗颈”这一步中改加水为加酸会得0分(请写出两条原因):_____________________。
c. “仪器A”可以是_________________。
【答案】 C A 0.046 使样品在反应时能保持在烧杯底适当的位置(或答避免反应时样品漂浮,即起镊子夹持的作用) ①先加酸会导致有部分 H2 逸出而无法收集,影响测定准确度;②不安全或实验者没有自我保护意识(因将盛水的量筒倒插入烧杯中时,手会与烧杯中的酸接触);③酸的用量太大,浪费试剂。 长颈漏斗
【解析】(1)①将钠投入到饱和的碳酸钠溶液中,钠先和水反应,呈现的现象是:钠浮在水面上,熔化成一个光亮的小球,并四处游动,最后消失,溶剂水减少,且氢氧根的浓度增大,所以恢复到室温时,烧杯底部有固体物质析出,由于碱性增强,溶液颜色加深,答案选C。②钠和水反应生成氢气和氢氧化钠,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,铜和氢氧化钠溶液不反应,所以生成氢气体积最大的是用铝箔包住钠,答案选A;(2)若500mL的矿泉水瓶开始时装有477.6mL水,用手挤压矿泉水瓶至水刚好充满矿泉水瓶并塞紧带有钠的塞子,要使倒置的矿泉水瓶正好恢复原状,则反应中产生的氢气体积是500mL-477.6mL=22.4mL,在标准状况下的物质的量是0.001mol,根据方程式2Na+2H2O=H2↑+2NaOH可知消耗金属钠是0.002mol,质量是0.002mol×23g/mol=0.046g。(3)a.由于钠与水反应时钠会四处游动,所以合金样品用用铜网包裹的目的是使样品在反应时能保持在烧杯底适当的位置。b.由于先加酸会导致有部分H2逸出而无法收集,影响测定准确度;其次不安全或实验者没有自我保护意识;最后酸的用量太大,浪费试剂,所以不能改加水为加酸;c. 向烧杯中加入盐酸可以用长颈漏斗,则“仪器A”可以是长颈漏斗。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如图K8﹣4所示.将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.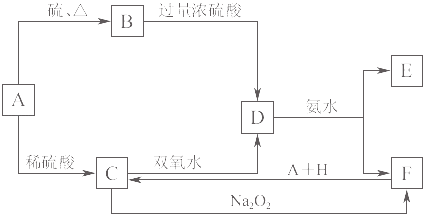
请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围: .
(2)A,B,H的化学式:A、B、H .
(3)①H2O2分子的电子式为 .
②写出C的酸性溶液与双氧水反应的离子方程式: .
(4)写出鉴定E中阳离子的实验方法和现象: .
(5)在C溶液中加入与C等物质的量的Na2O2 , 恰好使C转化为F,写出该反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去).
已知:2NO+CaO2═Ca(NO2)2;2NO2+CaO2═Ca(NO3)2 .
请回答下列问题:
a.向装置中通入N2 b.向三颈烧瓶中滴加稀硝酸 c.点燃酒精灯 d.熄灭酒精灯 e.停止通入氮气 f.关闭分液漏斗旋塞
(1)上述操作的正确排序为、c、、f、、 .
(2)B中盛放的试剂是 , 作用是除去(填化学式).
(3)装置E中,酸性K2Cr2O7溶液的作用:可将剩余的NO氧化成NO ![]() ,溶液由橙色变为绿色(Cr3+),反应的离子方程式是 .
,溶液由橙色变为绿色(Cr3+),反应的离子方程式是 .
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体.设计实验证明D中有亚硝酸钙生成 .
(5)整个过程持续通入氮气的作用 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2CO3溶液中存在如下反应:CO ![]() +H2O═HCO
+H2O═HCO ![]() +OH﹣下列说法中正确的是( )
+OH﹣下列说法中正确的是( )
A.溶液中加水, ![]() 增大
增大
B.加入Na2CO3固体, ![]() 减小
减小
C.升高温度,平衡常数减小
D.通入CO2 , 溶液pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列叙述中不正确的是( )
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是基本有机化工原料,由乙炔制备聚乙烯醇和顺式聚异戊二烯的合成路线(部分反应条件略去)如图所示:

回答下列问题:
(1)按系统命名法命名异戊二烯:________________________________________。
(2)X分子中含有的官能团名称是________________________________________。
(3)反应①~③中,__________(填反应序号)的反应类型与反应④不同,反应⑤属于__________反应。
(4)与乙炔具有相同官能团的异戊二烯的同分异构体共有__________种。
(5)X的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是__________(选填字母)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(6)顺式聚异戊二烯的结构式是(选填字母)__________。
a. b.
b.
c. d.
d.
(7)参照异戊二烯的上述合成路线,设计一条由乙烯和乙醛为起始原料制备1,3-丁二烯的合成路线:_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像均为实验过程中产生沉淀的物质的量(Y)与加入试剂的量(X)之间的关系图,则其中正确的是( )


A B C D
A. 向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡
B. 向NaAlO2溶液中逐滴滴加稀盐酸至过量且边滴边振荡
C. 向NH4Al(SO4)2溶液中逐滴加入NaOH溶液直至过量
D. 向等物质的量浓度的NaOH、Ba(OH)2、NaAlO2的混合溶液中逐渐通入CO2至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列5种有机物: ①CH2═CH2②CH3CH2OH ③CH3﹣C≡C﹣CH3
④ ![]() ⑤
⑤ ![]()
(1)其中,属于炔烃的是(填序号,下同),属于烃的衍生物的是 , 与①互为同系物的是 .
(2)用系统命名法给④命名,其名称为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com