
【题目】下列离子方程式能用来解释相应实验现象的是( )
实验现象 | 离子方程式 | |
A | 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 |
|
B | 向沸水中滴加饱和氯化铁溶液得到红褐色液体 |
|
C | 二氧化硫使酸性高锰酸钾溶液褪色 |
|
D | 氧化亚铁溶于稀硝酸 |
|
A. AB. BC. CD. D
【答案】A
【解析】
A、氢氧化镁碱性强于氨水;
B、制氢氧化铁胶体条件是加热,在化学式后注明胶体,得不到沉淀;
C、电荷不守恒;
D、硝酸具有强氧化性,将亚铁氧化成铁离子;
A、氢氧化镁碱性强于氨水,故A能用来解释相应实验现象;
B、制氢氧化铁胶体条件是加热,在化学式后注明胶体,得不到沉淀,离子方程式为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,故B不能用来解释相应实验现象;
Fe(OH)3(胶体)+3H+,故B不能用来解释相应实验现象;
C、电荷不守恒,正确的离子方程式为:5SO2+2MnO4-+2H2O=2Mn2++4H++5SO42-,故C不能用来解释相应实验现象;
D、硝酸具有强氧化性,其可将亚铁氧化成铁离子,正确的离子方程式为:3FeO+10H++NO3-=3Fe3++NO↑+5H2O,故D不能用来解释相应实验现象;
故选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】离子交换法净化水过程如图所示。下列说法中错误的是

A. 经过阳离子交换树脂后,水中阳离子的总数不变
B. 水中的![]() 、
、![]() 、Cl通过阴离子树脂后被除去
、Cl通过阴离子树脂后被除去
C. 通过净化处理后,水的导电性降低
D. 阴离子树脂填充段存在反应H++OH![]() H2O
H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu2微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要村料。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是____________(填标号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是__________、__________。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是__________,其中与乙二胺形成的化合物稳定性相对较高的是__________(填“Mg2+”或“Cu2+”)。
(3)一些氧化物的熔点如下表所示:
氧化物 | Li2O | MgO | P4O6 | SO2 |
熔点/°C | 1570 | 2800 | 23.8 | 75.5 |
解释表中氧化物之间熔点差异的原因__________。
(4)图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=__________pm,Mg原子之间最短距离y=__________pm。设阿伏加德罗常数的值为NA,则MgCu2的密度是__________g·cm3(列出计算表达式)。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
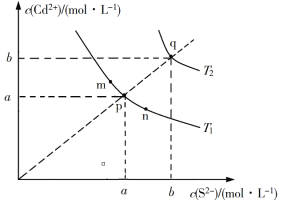
A. 图中a和b分别为T1、T2温度下CdS在水中的溶解度
B. 图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C. 向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D. 温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定的溶液中,能大量共存的是( )
A.使pH试纸显蓝色的溶液:Cu2+、NO![]() 、Fe3+、SO
、Fe3+、SO![]()
B.与铁粉反应放出H2的无色溶液:NO![]() 、Fe2+、Na+、SO
、Fe2+、Na+、SO![]()
C.使红色石蕊试纸变蓝的溶液:SO![]() 、CO
、CO![]() 、Na+、K+
、Na+、K+
D.Na2CO3溶液:Al3+、SO![]() 、Cl-、K+
、Cl-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。

回答下列问题:
Ⅰ.硅粉与![]() 在300℃时反应生成
在300℃时反应生成![]() 气体和
气体和![]() ,放出
,放出![]() 热量,该反应的热化学方程式为________________________。
热量,该反应的热化学方程式为________________________。![]() 的电子式为__________________。
的电子式为__________________。
Ⅱ.将![]() 氢化为
氢化为![]() 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①![]()
![]()
②![]()
![]()
③![]()
![]()
(1)氢化过程中所需的高纯度![]() 可用惰性电极电解
可用惰性电极电解![]() 溶液制备,写出产生
溶液制备,写出产生![]() 的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。
的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。

(2)已知体系自由能变![]() ,
,![]() 时反应自发进行。三个氢化反应的
时反应自发进行。三个氢化反应的![]() 与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的
与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的![]() 小,主要原因是________________________。
小,主要原因是________________________。
(3)不同温度下反应②中![]() 转化率如图2所示。下列叙述正确的是______(填序号)。
转化率如图2所示。下列叙述正确的是______(填序号)。
a.B点:![]() b.
b.![]() :A点
:A点![]() 点 c.反应适宜温度:
点 c.反应适宜温度:![]() ℃
℃
(4)反应③的![]() ______(用
______(用![]() ,
,![]() 表示)。温度升高,反应③的平衡常数
表示)。温度升高,反应③的平衡常数![]() ______(填“增大”、“减小”或“不变”)。
______(填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除![]() 、
、![]() 和
和![]() 外,还有______(填分子式)。
外,还有______(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加HSO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v2 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________。
(2)Ⅰ中发生反应的离子方程式是_______________________________。
(3)Ⅲ中发生反应的化学方程式是_________________________________。
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是______________________________。
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是________。
(6)Ⅴ中滴定至终点的现象是_____________________________。
(7)废水中苯酚的含量为___________g·L1(苯酚摩尔质量:94 g·mol 1)。
(8)由于Br2具有____________性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果偏高。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列判断正确的是
A. 标准状况下,2.24L苯中含有碳碳双键数为0.3NA
B. 6.4gS2、S4和S8的混合物中所含硫原子数为0.2NA
C. 1L0.1mol·L-1的氢碘酸中含碘化氢分子数为0.1NA
D. 60g乙酸与足量乙醇发生酯化反应时断裂的C-O键数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com