
【题目】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下: 
(1)气体A中的大气污染物可选用下列试剂中的吸收. a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在(填离子符号),检验溶液中还存在Fe2+的方法是(注明试剂、现象).
(3)由泡铜冶炼粗铜的化学反应方程式为 .
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4 , 若将该反应设计为原电池,其正极电极反应式为 .
【答案】
(1)cd
(2)Fe3+;另取少量所得溶液,滴加KMnO4溶液,KMnO4溶液紫红色褪去
(3)3Cu2O+2Al ![]() ?Al2O3+6Cu
?Al2O3+6Cu
(4)4H++O2+4e﹣=2H2O
【解析】解:(1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,a.浓H2SO4不能吸收二氧化硫,故a错误;b.稀HNO3可以吸收二氧化硫,但生成NO污染大气,故b错误;c.NaOH溶液与二氧化硫反应生成亚硫酸钠和水,不产生新的污染气体,故c正确;d.氨水与二氧化硫反应生成亚硫酸铵,不产生新的污染气体,故d正确;故答案为:c、d;(2)Fe3+遇KSCN溶液变为血红色,用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验,取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去,故答案为:Fe3+;取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去,则溶液中存在Fe2+;(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu,反应方程式为3Cu2O+2Al ![]() Al2O3+6Cu,故答案为:3Cu2O+2Al
Al2O3+6Cu,故答案为:3Cu2O+2Al ![]() Al2O3+6Cu;(4)原电池正极发生的是化合价降低得电子的反应,根据方程式可知是O2得电子,另外,由于H2SO4存在,所以发生的O2酸性条件下的电极反应:4H++O2+4e﹣═2H2O,故答案为:4H++O2+4e﹣═2H2O. (1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,二氧化硫是酸性氧化物,结合选项中各物质的性质判断;(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验;(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu;(4)根据原电池原理,正极发生的是化合价降低得电子的反应.
Al2O3+6Cu;(4)原电池正极发生的是化合价降低得电子的反应,根据方程式可知是O2得电子,另外,由于H2SO4存在,所以发生的O2酸性条件下的电极反应:4H++O2+4e﹣═2H2O,故答案为:4H++O2+4e﹣═2H2O. (1)由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,二氧化硫是酸性氧化物,结合选项中各物质的性质判断;(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验;(3)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu;(4)根据原电池原理,正极发生的是化合价降低得电子的反应.


科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.电负性的大小顺序为Cl>S>P
B.由于NO3﹣和SO3互为等电子体,所以可以推断NO3﹣的空间构型为平面三角形
C.根据晶格能的大小可以判断MgCl2的熔点比CaCl2高
D.液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯的下列叙述中,正确的是( ) ①能使酸性KMnO4溶液褪色;
②可发生加成反应;
③可溶于水;
④可溶于苯中;
⑤能与浓硝酸在浓H2SO4作用下发生取代反应;
⑥所有的原子可能共平面.
A.①②③④⑤
B.①②⑤⑥
C.①②④⑤⑥
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验。请回答下列问题:
编号 | 实验操作 | 实验现象 |
① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入2滴1mol/LFeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡; 试管B中产生的气泡量增多。 |
② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2溶液。 | 两支试管中均未明显见到有气泡产生。 |
(1)实验①的目的是其它条件相同时,探究______条件对H2O2分解速率的影响。
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,请你用实验中所提供的几种试剂,对上述操作进行的改进是____________________________________。
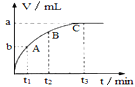
(3)某同学在50mL一定浓度的H2O2溶液中加入适量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是____(填字母代号)。
(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该化学兴趣小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

①定性分析:如图甲可通过观察________________________,定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是______________________。
②定量分析:用图乙所示装置做对照试验,实验时均以3min时间为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是________________,所需仪器为_______。
(5)通过对上述实验过程的分析,在实验设计时,要考虑_________思想方法的应用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的分子式为C9H10O2 , A在光照条件下生成一溴代物B,B分子的核磁共振氢谱中有4组峰,峰面积比为2:2:2:3,B可发生如下转化关系(无机产物略):
已知:①K与氯化铁溶液发生显色反应,且环上的一元取代物只有两种结构;
②当羟基与双键碳原子相连时,会发生如下转化:RCH=CHOH→RCH2CHO;
请回答下列问题:
(1)B中含氧官能团的名称是:
(2)反应⑤属于反应类型.
(3)写出结构简式:A , J
(4)写出下列反应的化学方程式:反应②:
反应④:
(5)同时符合下列要求的K的同分异构体有种;写出其中任意两种的结构简式:、 . Ⅰ.苯环上的一元取代物只有两种结构
Ⅱ.能发生银镜反应
Ⅲ.与氯化铁溶液发生显色反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下: 
(1)气体A中的大气污染物可选用下列试剂中的吸收. a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在(填离子符号),检验溶液中还存在Fe2+的方法是(注明试剂、现象).
(3)由泡铜冶炼粗铜的化学反应方程式为 .
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4 , 若将该反应设计为原电池,其正极电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下,在三个干燥的圆底烧瓶中分别充满:①混有少量空气的HCl,②混有少量NO的NO2,③NO2和O2[V(NO2)∶V(O2)=4∶3]分别和水进行喷泉实验,经充分反应后,所各溶液的物质的量浓度之比为()。
A. 1∶1∶1 B. 3∶2∶3 C. 5∶5∶4 D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验现象的反应方程式正确的是( )
A.在CH3COONa溶液中,滴加酚酞变红:CH3COO﹣+H2O═CH3COOH+OH﹣
B.在H2O2溶液中,滴加FeCl3溶液产生气泡:2H2O2+2Cl﹣═2H2O+O2↑+Cl2↑
C.将相互接触的铜片和锌片置于稀硫酸中,铜片表面有气泡产生:Cu+2H+═Cu2++H2↑
D.向Cu(OH)2悬浊液中滴加Na2S溶液,蓝色沉淀变黑色:Cu(OH)2(s)+S2﹣ (aq)CuS(s)+2OH﹣ (aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com